全球首创!阿里联合顶尖三甲,肠癌无感检测来了
发布时间:2026-04-28来源:医学界
肠癌的早期治愈率超90%,但多数患者确诊时已错过最佳治疗时机,导致了大量肠癌相关死亡。
如今,一项发表在《肿瘤学年鉴》(Annals of Oncology,影响因子65.4)上的中国研究,为这一领域带来了全新希望。
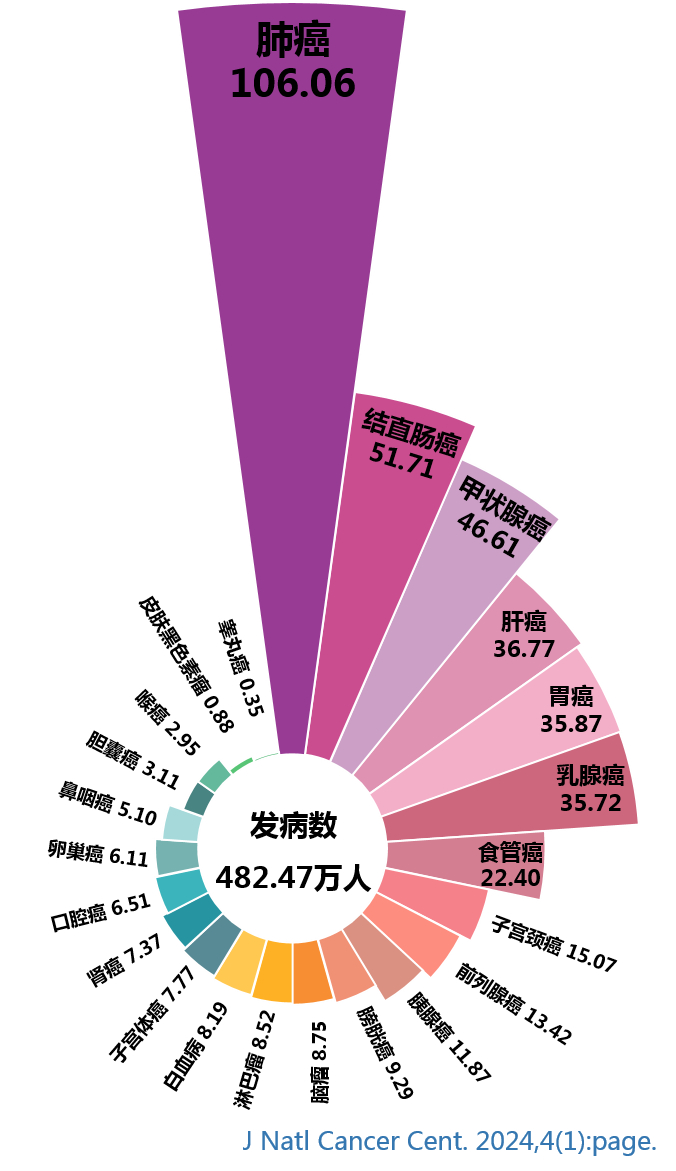
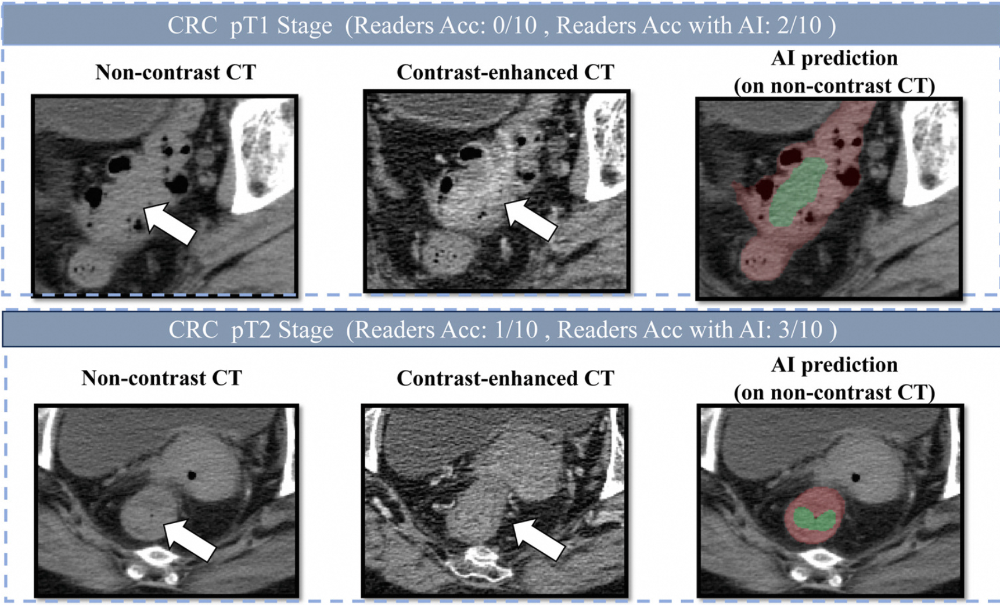
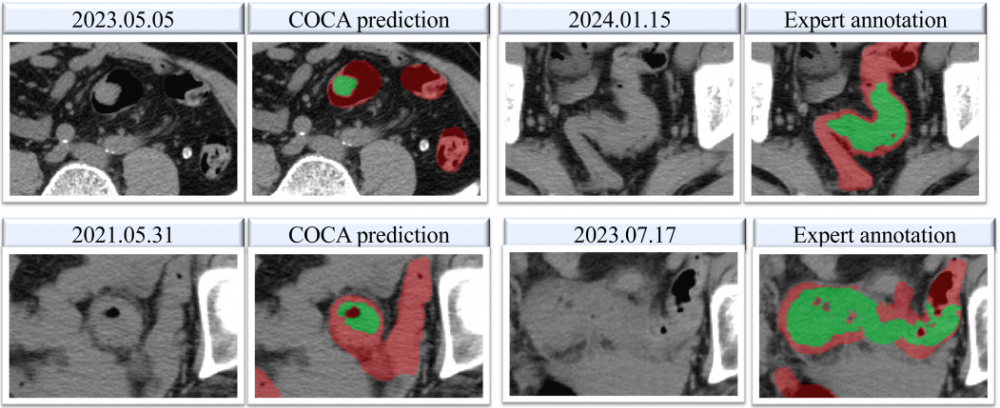
2023年,一位患者在医院拍了一张腹部CT,报告未提及有任何肠道异常。直到2024年被确诊为肠癌时,回溯当初那张CT,才发现癌灶其实早已存在。类似的悲剧并不少见。肠癌是全球第三大高发恶性肿瘤,但早期的筛查检出率长期偏低。研究显示,既往有超过七成的肠癌相关死亡,都发生在未能及时发现的患者身上。如今,由中国科学家开发的一个AI模型,正在试图改变这件事。4月21日,阿里巴巴达摩院联合广东省人民医院、广州市第一人民医院等机构在《肿瘤学年鉴》发文,通过自主研发的AI模型COCA,全球首次证明:仅凭一张普通的平扫CT,就能实现大规模结直肠癌筛查,敏感性86.6%,特异性99.8%。据了解,这是达摩院继胰腺癌模型PANDA、胃癌模型GRAPE之后,在“平扫CT+AI”路线上的又一突破。目前,团队已构建覆盖消化系统多个高发癌种的AI筛查体系,正向“一张CT、筛多种癌”的目标推进。在上海交通大学医学院附属新华医院,结直肠肛门外科副主任医师吴庭玉经常会在门诊碰到让他惋惜的肠癌患者。结直肠癌也被称为“懒癌”。从肠道息肉开始,发展成恶性肿瘤通常需要5到10年,如果在这个窗口期内发现并干预,早期患者的手术治愈率超过90%。“但实际临床中,出现便血征兆后,很多患者以为只是痔疮,并不重视。等到肿瘤进一步增大,发展成肠梗阻,甚至出现肝肺转移才想到来医院检查。此时,治疗已经变得非常棘手,有些人甚至需要进行肠造口。”吴庭玉表示。根据国家癌症中心的数据,2022年,我国新发结直肠癌约51.71万例,死亡约24万人,超越胃癌成为中国第二大高发癌症。另有研究显示,超过七成的结直肠癌相关死亡,都发生在未能及时筛查的人群中。吴庭玉介绍,目前,结直肠癌最常用的筛查手段是社区粪便隐血筛查,如果阳性,则进一步推荐来医院做“金标准”的肠镜检查。“但即使在上海这样医疗资源相对充裕的城市,社区粪便初筛覆盖率超过60%,重点人群的肠镜检查率也只有约30%–40%。”“此外,粪便隐血检测敏感性较高,但特异性不足,需要再通过肠镜最终确诊。但做肠镜需要提前预约、服泻药清肠、过程有创且不适,很多人因此一拖再拖。”吴庭玉表示,从粪便初筛阳性到进一步接受肠镜检查,转化率仍然有限。达摩院资深算法专家、多癌筛查技术负责人张灵告诉“医学界”,大约在2022年,团队关注到了肠癌。“那时,我们刚在胰腺癌的‘平扫CT+AI’筛查上取得突破。我们也开始思考,肠癌的早筛困境,是不是也能通过这种方法得到解决?”要知道,中国各级医院每年要完成数千万次腹部和胸部CT扫描,这些影像中也记录有结直肠的轮廓。如果能直接“二次利用”,就能在不增加任何负担的情况下,实现对结直肠癌的大规模筛查“平扫CT的对比度较低,肉眼极难辨认早期的肠癌病灶,但这恰恰是AI可以发挥优势的地方。”张灵表示,在和不少临床专家详细沟通后,团队进一步坚定了这一想法,并正式启动了COCA肠癌筛查模型的研发。从医学的角度,开发基于“平扫CT+AI”的肠癌筛查系统,存在不小的挑战。张灵告诉“医学界”,肠癌CT筛查的独特挑战,一方面是结直肠的范围太大了,几乎横跨了整个腹部,弯弯绕绕,平扫CT中关于肠道结构的识别和检测分割,本身就是一大难题。另一方面,患者日常做平扫CT,并不会进行肠道准备,他们的肠腔内充满各种内容物,影像表现极其复杂。而肠道肿瘤的形状也没有规律,什么形态都有可能,进一步增加了鉴别的难度。张灵表示,针对一系列难题,团队采用了“定位+诊断”的双阶段框架:先通过AI定位结直肠区域,再在定位范围内检测肿瘤。同时,针对直径小于3厘米的肿瘤,团队还引入专门的训练模型,使得AI能精细分割形态复杂的肠道部位,并克服内容物干扰,提高了对小病灶的检出能力。经过三四年的研发,COCA模型的成果最终问世。根据此次发布在《肿瘤学年鉴》的研究结果,在六个国际中心,涵盖2053例患者的验证中,COCA的AUC(衡量整体判别能力的指标)达到0.967至0.996。与10名放射科医师的CT对照阅片研究显示,COCA的肠癌检出敏感度,比医生平均水平高出20.4%,特异度高出5.4%。当医生在AI辅助下重新阅片,其诊断准确率显著提升——一位经验丰富的普通放射科医师,准确率从75.6%跃升至90.3%。不仅仅是腹部CT。张灵告诉“医学界”,在临床中,胸部CT的使用量往往更大,但其图像通常只覆盖少部分肠道区域。而即便如此,若肠癌在胸部CT扫描范围内,COCA识别敏感度仍达到81.8%,特异度99.9%。这意味着,一个可能只是来做肺结节检查的患者,也有机会“顺带”完成肠癌筛查。更进一步,研究团队开展了两轮大规模真实世界回顾性验证,覆盖27433名连续就诊患者。结果显示,COCA保持了86.6%的敏感性和99.8%的特异性,并从中识别出5例此前被临床漏诊的肠癌。其中有一名患者,此前已连续两年进行过平扫CT检查,但后来才通过肠镜确诊肠癌,此时肿瘤已出现进一步发展。而若当时就有COCA介入,这两年间的任何一张CT,都可能成为发现肿瘤的契机。值得一提的是,面对不同人群,COCA还准备了两个版本——“高特异度”和“高灵敏度”。高特异度指的是阳性误报率低,适用于全人群的大规模肠癌筛查。“大部分人是健康的,如果出现太多假阳性,不仅会引起公众的恐慌,也会给医疗系统增加不必要的负担。”张灵说。高灵敏度版本则面向数量有限的高风险人群,其核心是追求尽可能不漏诊。研究结果显示,COCA高灵敏度版本,对I期肠癌的检出率达到83%至92%,甚至能检出尚未癌变的进展期腺瘤,其检出能力优于目前文献报道的其他技术路线。据张灵介绍,目前,COCA模型可以无缝嵌入临床医生的工作流,“它能在后台对CT影像进行自动筛查,一旦发现可疑病灶立刻发出提示,并标注出疑似肿瘤的位置、大小及概率,提醒医生进行详细的评估。”事实上,这已经不是达摩院团队第一次在“平扫CT+AI”的技术路线上取得突破。2023年,团队率先发布了胰腺癌早筛模型PANDA,登上《自然·医学》,后获得了美国FDA的“突破性医疗器械”认定。《自然·医学》同期发布评论文章题为:基于影像AI的癌症筛查即将进入黄金时代。2025年6月,全球首个胃癌影像筛查AI模型GRAPE再次发表于《自然·医学》。它瞄准了胃镜在中国普及率不高的短板,首次利用平扫CT在大规模多中心研究中发现了多例漏诊胃癌患者。如今COCA的发布,意味着达摩院团队“平扫CT+AI”的技术路线,已经在多个高发癌种上得到了系统验证。事实上,目前国际上最火热的多癌筛查研发赛道是“液体活检”。它瞄准血液检测,希望通过分析血液中的肿瘤标志物,来一次性实现多癌筛查。“最开始,我们一定程度上也受到了液体活检的启发。”张灵告诉“医学界”,“但它终归需要患者去主动抽血,专门做检查。平扫CT不同,它在我国的日常用量非常大,这些图像本身就在后台,我们只需要用AI跑一下。”此外,目前国际上最主流的液体活检多癌筛查产品,单次检测费用约为1000美元。“而结合平扫CT的AI诊断策略,不需要额外检查、不产生额外费用,甚至不需要患者主动配合。”张灵表示。而站在更宏观的公共卫生视角,这一技术路线的意义则更为深远。尤其是在基层,张灵表示,如今,中国有大量基层医院配备了CT设备,但仍缺乏足够的专科医生来系统性阅片。如果AI能先行筛查,就相当于给基层配备了一位“癌症检测专家”,提示高风险的第一时间转诊至上级医院,大量患者也将从中获益。据张灵介绍,除了胰腺癌、胃癌、肠癌,团队还在同步推进食管癌、肝癌诊断工具的开发,并希望最终能将“消化系统五癌”整合为联合筛查系统。“同时,我们在乳腺癌、肾癌等癌种上的研发也取得了阶段性的进展。”张灵表示,“我们的最终目标,是希望只要患者做了CT,不管胸部还是腹部,系统都能把里面的癌症筛查出来,让多数癌症患者,都能在早期得到及时的治疗。”
来源:医学界
校对:蔡 菜
运营:莉 莉
责编:汪 航
*“医学界”力求所发表内容专业、可靠,但不对内容的准确性做出承诺;请相关各方在采用或以此作为决策依据时另行核查。 ↓↓↓点击阅读原文上医学界医生站App看更多医疗信息
↓↓↓点击阅读原文上医学界医生站App看更多医疗信息
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。



 ↓↓↓点击阅读原文上医学界医生站App看更多医疗信息
↓↓↓点击阅读原文上医学界医生站App看更多医疗信息


