患者死亡,Revolution怒斥三宗罪!Erasca内忧外患


精鼎医药研讨会 | 全球研发引擎:从中国高质创新到全球临床卓越
合作机会来了!


![]()
国内上市药企寻找临床阶段妇科(肿瘤除外)或抗感染创新药,小分子优先。希望成熟靶点,风险低。
欢迎感兴趣的药企立即联系药时代BD团队!
BD@drugtimes.cn
合作机会来了!


![]()
国内上市药企寻找临床阶段妇科(肿瘤除外)或抗感染创新药,小分子优先。希望成熟靶点,风险低。
欢迎感兴趣的药企立即联系药时代BD团队!
BD@drugtimes.cn
合作机会来了!


国内上市药企寻找临床阶段妇科(肿瘤除外)或抗感染创新药,小分子优先。希望成熟靶点,风险低。
欢迎感兴趣的药企立即联系药时代BD团队!
BD@drugtimes.cn

跨试验比较,数据惊艳却难服众
此次公布的数据来自两项Ⅰ期剂量递增研究:在美国开展的AURORAS‑1试验,以及由嘉越医药在中国执行的JYP0015M101研究。
在KRAS G12X突变非小细胞肺癌(NSCLC)患者中,Erasca采用uORR₈wk(第8周未经确认的总缓解率)作为评价指标,对标《Journal of Thoracic Oncology》2025年发表的daraxonrasibⅠ期NSCLC数据:
在16–32mg的药理活性剂量(PAD)下,所有接受二线及以上(2L+)治疗的患者(N=37)的uORR₈wk周为62%,较daraxonrasib数据高出24%。
在免疫检查点抑制剂/铂类经治后线(2/3L)患者中(N=16),uORR₈wk提升至75%,领先daraxonrasib达37%。
在胰腺导管腺癌(PDAC)患者中,Erasca采用uORR₁₄wk(第14周未经确认的总缓解率)作为评价指标,对标daraxonrasib在2024年EORTC‑NCI‑AACR会议上展示的Ⅰ期数据:
在16–32mgPAD下,所有接受二线治疗的患者(N=20)的uORR₁₄wk为40%,较daraxonrasib高出11%。
在扩展期推荐剂量(RDE)24–32mg的合并分析中(N=12),uORR₁₄wk为42%,较daraxonrasib高出13%。
在RDE 32mg剂量组的2例患者中,uORR₁₄wk达到50%,较daraxonrasib的领先幅度扩大至15%。
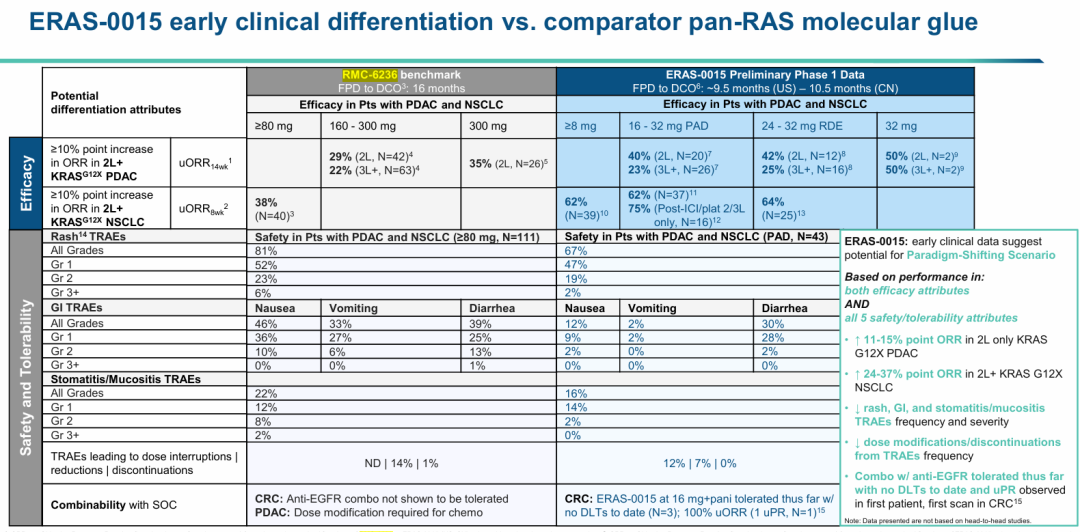
来源:Erasca公告
Revolution的律师对Erasca将ERAS‑0015与daraxonrasib进行直接对比的做法提出强烈异议。跨试验比较好比“关公战秦琼”:患者基线、入组标准、评估频率、数据截点均不相同,尤其对于样本量小、处于早期阶段的肿瘤临床试验,直接相减得出的“领先百分点”缺乏科学依据,不能得出优效结论。
面对这一尖锐质疑,Erasca首席执行官Jonathan Lim在接受《Endpoints News》采访时坦承:“跨试验比较总有其局限性。”但他同时强调,ERAS‑0015“在早期临床活性方面展现出了非常有前景的信号”,与Revolution药物的对比仅旨在“提供更多参考背景”。然而,这一解释并未平息方法学上的质疑,反而为后续的法律冲突埋下了伏笔。

Revolution一纸诉状,怒斥三宗罪
就在数据发布前夕的4月24日,Erasca收到了Revolution Medicines律师发出的重磅信函;该信函随后于数据发布当天在被正式披露。两者在时间上的高度重叠,令人怀疑这场“法律战役”的战术安排,有意识地将上市公司的焦点从临床数据转向法律风险。

来源:8-K文件
Revolution依据美国专利法及商业秘密法,向Erasca抛出了三项核心指控。
指控一:专利侵权。Revolution认为,ERAS‑0015与其美国第12,409,225号专利(‘225专利)中声明的某些组合物属于“实质等同”。根据美国专利法的等同原则:“以实质相同之方式,行实质相同之功能,得实质相同之结果,则为等同侵权”,ERAS‑0015侵犯了该专利。
从机制上看,daraxonrasib通过与亲环蛋白A(CypA)结合形成二元复合物,进而与RAS(ON)蛋白形成高亲和力三元复合物,阻断下游信号传导;而ERAS‑0015同样作为pan‑KRAS分子胶,通过与CypA及RAS形成复合物来发挥抑制作用。双方在作用方式、功能和结果上的高度相似,为Revolution的“等同原则”主张提供了事实基础。
指控二:商业秘密盗用。Revolution指控第三方在涉及ERAS‑0015的专利申请中盗用了其商业秘密,而Erasca作为被许可方,依据商业秘密法应承担相应责任。这一指控的矛头,直接指向ERAS‑0015的原始技术来源:中国广州嘉越医药。

来源:Erasca公告
2024年,Erasca从嘉越获得JYP0015(即ERAS‑0015)的全球独家授权,并在2026年3月行使选择权,将大中华区权益也纳入全球版图。这种涉及跨境技术来源的指控,不仅增加了诉讼的复杂性,更在国际地缘合规层面为Erasca蒙上了一层阴影。一旦技术源头的知识产权瑕疵被证实,Erasca不仅可能面临巨额赔偿,其全球独家权利亦将岌岌可危。
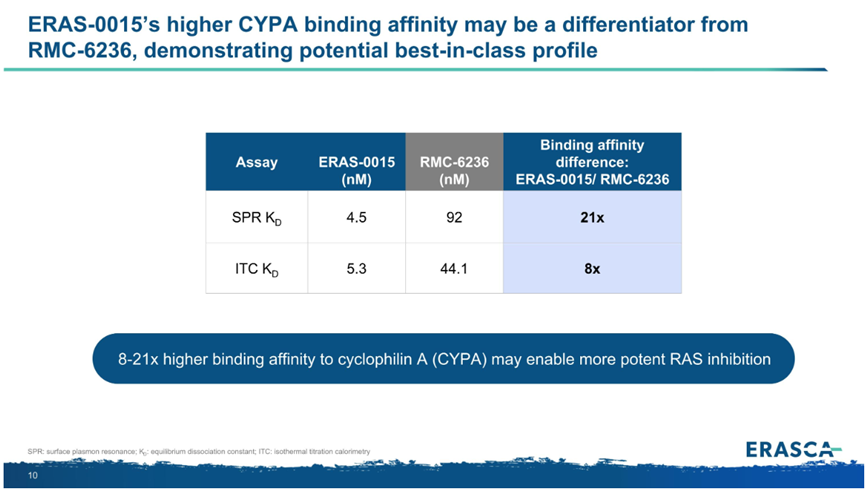
指控三:不当数据对比。Revolution要求Erasca立即停止将ERAS‑0015与RMC‑6236进行 “欺骗性和不真实的比较宣传”。事实上,在此次临床数据对比之前,Erasca在临床前数据中就已宣称ERAS‑0015对CypA的亲和力较daraxonrasib高出8–21倍,且半衰期更长,自诩“同类最佳”。
来源:Erasca公告
基于上述三项指控,Revolution更进一步要求Erasca立即停止在美国继续开发该在研药物。作为回应,Erasca在文件中表示,所有主张“毫无根据”,公司将积极应诉。
法律层面的外部压力已经足够令投资者不安,更令人担忧的阴影来自临床本身。

一例患者死亡,安全性存疑
在Erasca披露的安全性数据中,一名66岁的转移性胰腺癌患者,在接受24mg ERAS‑0015治疗期间出现了3级肺炎,后因持续进展,在患者主动放弃支持性治疗后不幸去世。
对此,Erasca首席执行官Jonathan Lim强调:患者死亡的关键原因在于其选择停止支持性治疗,而非药物本身所致。他同时指出,ERAS‑0015展现的皮疹、胃肠道反应和口腔炎等不良事件频率和严重程度都较低,这为未来与抗EGFR单抗Vectibix(帕尼单抗)等标准治疗联合使用提供了良好基础。
然而,这一回应并未让分析人士和投资者放心。这种不信任,恰恰源于药物本身所展现出的临床特征:尤其是其强大的药代动力学表现。
在药代动力学维度上,ERAS‑0015表现出的线性暴露特征直至40mg仍未触达平台期,这意味着疗效挖掘潜力充足,但同时也意味着在更高剂量下,不良事件发生率可能随之增加。如果泛RAS抑制在产生极高ORR的同时,对正常组织产生“脱靶”毒性(或靶向肺组织的特异性毒性)导致5级致死性不良事件,那么其治疗窗口将被极大压缩。
FDA对于出现5级不良事件的Ⅰ期项目,通常会启动严格审查机制,甚至可能下达“部分临床暂停”指令,要求补充安全性数据后方可继续推进。若肺炎事件在后续入组患者中再次复现,ERAS‑0015的安全性局面将更加严峻。
尽管遭遇法律指控与安全性事件的双重压力,Erasca管理层并未动摇对ERAS‑0015的信心。Lim在采访中称:“我们正在开发一款具备同类最佳潜力的药物。该领域内其他公司注意到并试图干扰我们按计划进行的临床数据披露,这并不令人意外。我们认为Revolution的指控毫无根据。”
对于Erasca而言,多个关键决策点将接踵而至:
ERAS‑4001(pan‑KRAS抑制剂)的Ⅰ期单药数据预计于2026下半年读出;
ERAS‑0015单药扩张队列与联合治疗数据预计于2027上半年披露。
而在此之前,公司必须在专利诉讼辩解、安全数据补充与投资人信心重建之间寻找微妙的平衡。
小结:
当低垂的果实被摘尽后,创新药玩家之间的竞争早已从单纯的“临床数据比拼”升级为涵盖临床优势、知识产权、注册路径乃至商业模式的立体博弈。任何单维度的“数据惊艳”都无法确保一家创新型生物科技公司的成功。
参考资料:
1.https://endpoints.news/erasca-reports-ras-cancer-drug-data-after-legal-threat-from-revolution/
2.https://investors.erasca.com/news-releases/news-release-details/erasca-announces-positive-preliminary-phase-1-dose-escalation
3.https://investors.erasca.com/static-files/698b7907-165a-482b-b2ee-2696ba0c6138
4.https://www.sec.gov/Archives/edgar/data/1761918/000119312526179214/eras-20260427.htm
5.https://www.sec.gov/Archives/edgar/data/1761918/000095017025004613/eras-ex99_1.htm
6.https://investors.erasca.com/news-releases/news-release-details/erasca-exercises-option-secure-worldwide-rights-eras-0015-pan
7.其他公开资料

2026-04-25

2026-04-24

2026-04-24

2026-04-23

版权声明/免责声明
本文为原创文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn

![]()
![]()
![]()
![]()

![]()
![]()
![]()
![]() 点击查看更多精彩内容!
点击查看更多精彩内容!
版权声明/免责声明
本文为原创文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn

![]()
![]()
![]()
![]()

![]()
![]()
![]()
![]() 点击查看更多精彩内容!
点击查看更多精彩内容!
版权声明/免责声明
本文为原创文章。
本文仅作信息交流之目的,不提供任何商用、医用、投资用建议。
文中图片、视频、字体、音乐等素材或为药时代购买的授权正版作品,或来自微信公共图片库,或取自公司官网/网络,部分素材根据CC0协议使用,版权归拥有者,药时代尽力注明来源。
如有任何问题,请与我们联系。
衷心感谢!
药时代官方网站:www.drugtimes.cn
联系方式:
电话:13651980212
微信:27674131
邮箱:contact@drugtimes.cn