一份没有胸痛的“心梗”心电图:24岁年轻人的心脏里为何长满“石头”?丨医起推理吧

来源 | 医脉通
作者 | 阿圆
一位24岁的年轻人,心电图却显示着典型的完全性左束支传导阻滞,更引人注目的是,在I、aVL、V5、V6这些高侧壁和侧壁导联上,竟然出现了病理性Q波。
这是急性心肌梗死(心梗)吗?患者如此年轻,冠脉血管真的出问题了?还是另有隐情?

这是发布在Front Cardiovasc Med上的一个病例,最终病因藏在这位年轻人厚厚一沓、跨越近十年的病史中。
第1幕
一份没有胸痛的“心梗”心电图
小陈(化名)被送进急诊室时,主诉是左上肢肿胀2个月。他面色苍白,但神情平静,否认有任何胸痛、胸闷、呼吸困难。
“没有胸痛?一点都没有?”急诊医生再次确认。
“没有,就是胳膊肿!”小陈回答得很肯定。
查体:生命体征平稳,体温36.6℃,血压93/75mmHg,心率95次/分。左上肢的动静脉瘘侧肢体确实肿胀明显。心肺腹查体未见特殊异常。
但心电图的结果,却让大家沉默了(图1)。
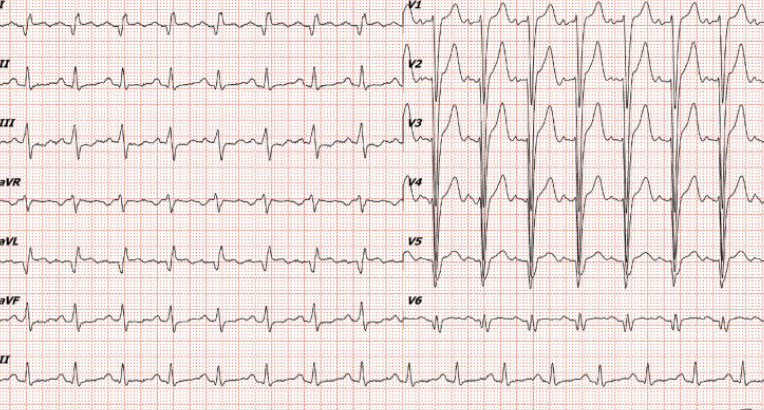
图1 患者心电图
心血管内科医生被紧急会诊。面对这份心电图,大家的第一反应是:年轻男性,新发病理性Q波,首先要排除急性冠脉综合征。但患者没有胸痛,心肌酶结果也回来了:肌钙蛋白I仅轻度升高(0.216 ng/ml),CK-MB正常(2.35 ng/ml)。
这个心肌酶谱模式,不符合典型的急性心肌梗死——肌钙蛋白升高幅度与心电图的严重程度不匹配。
第2幕
超声与CT揭开谜底,心尖部的“石头”
如果不是心梗,那这些病理性Q波从何而来?
心脏彩超的结果让超声科医生倒吸一口凉气:心脏整体显著扩大,左心室舒张末期内径(LVEDD)达到惊人的80mm,左心室射血分数(LVEF)仅剩22%,提示严重的心功能不全。更诡异的是,在心尖部,超声发现了一个不规则的强回声团块,大小约3.0cm×4.0cm,后方伴有声影,高度提示钙化灶。
为了进一步明确,医生安排了胸部增强CT。结果证实了超声的发现:
➤心脏呈球形显著增大。
➤高侧壁可见条状钙化。
➤心尖部可见一枚半球形的巨大钙化灶,大小与超声测量相符。
谜底揭晓了:这些“石头”一样的钙化灶,压迫和取代了正常的心肌组织,尤其是在心尖部,形成了一个巨大的电静止区。
这完美地解释了心电图的异常:心尖部和侧壁的大面积心肌被钙盐取代,失去了正常的除极能力,导致对应导联(I、aVL、V5、V6)出现病理性Q波。它们并非由冠脉堵塞、心肌坏死所致,而是心肌被“钙化”掏空后,电信号传导的“死角”。
第3幕
追问病因,8年透析埋下的“伏笔”
病因找到了,但心血管医生必须追问:一个24岁的年轻人,心脏为何会严重钙化?
追问病史,一个关键信息浮出水面:小陈是一名维持性血液透析患者,因先天性孤立肾、泌尿系统畸形,他自2017年起就开始接受血液透析,透析龄长达8年。
回顾他历年的化验单,真相更加清晰。作为一名长期透析患者,他有着严重的慢性肾脏病-矿物质和骨异常(CKD-MBD):
➤血磷:最高达3.27mmol/L(参考值0.85-1.15mmol/L),严重超标。
➤血钙:曾在1.88mmol/L(参考值2.11-2.52mmol/L),偏低。
➤甲状旁腺激素(iPTH):曾高达2000pg/ml(参考值18.5-88.0pg/ml),极度升高。
➤25-羟维生素D:仅13.05ng/ml(参考值>30ng/ml),严重不足。
这些数字揭示了一条清晰的病理生理链条:
肾脏功能丧失导致磷排泄障碍,引发高磷血症;高血磷刺激甲状旁腺,导致继发性甲状旁腺功能亢进,大量释放iPTH,将骨骼中的钙和磷释放入血,导致血钙磷乘积急剧升高;升高的钙磷产物,加上尿毒症毒素环境、体内钙化抑制剂(如胎球蛋白A)的减少,共同构成了一个促钙化环境;钙和磷无处可去,最终异位沉积在血管壁、心脏瓣膜、心肌组织,而心肌细胞被钙盐取代,形成肉眼可见的钙化灶,即转移性心肌钙化。
小陈的心脏,就这样在8年的透析历程中,被一点一点地“石化”了。
明确诊断后,小陈在住院期间接受了血管通路修整术,解决了上肢肿胀问题。心血管内科团队评估后认为,既往冠脉CTA未见明显狭窄,本次无急性心梗证据,因此未进行冠脉介入治疗。
出院后,小陈继续接受规律透析,并由肾内科团队强化CKD-MBD的管理。但他的心脏已经留下了不可逆转的损伤,未来发生心力衰竭、恶性心律失常的风险极高。
病例思考
1.病理性Q波的鉴别诊断,必须拓宽思路
对于心血管医生而言,看到病理性Q波,第一反应确实是急性心肌梗死。但病理性Q波≠心肌梗死。任何可以导致局部心肌电活动消失或显著减弱的疾病,都可能模拟出Q波。
尤其是在透析患者这一特殊人群中,鉴别诊断还应包括:
➤转移性心肌钙化:由CKD-MBD所致,是透析患者的特有并发症。
➤浸润性心肌病:如心肌淀粉样变、结节病等。
➤心肌纤维化:各种原因导致的局灶性心肌瘢痕。
2.如何鉴别诊断?
当心电图异常与临床表现不符时,心脏超声和心脏CT是不可或缺的工具。
➤超声:可发现异常的高回声团块。本例心尖部的巨大钙化灶,超声清晰可见。
➤心脏CT:是诊断心肌钙化的金标准。不仅能清晰显示钙化的位置、范围、形态,还能进行钙化积分定量,评估整体钙化负荷。
对于透析患者,即使没有心脏相关症状,心血管医生也应考虑定期进行心脏超声筛查,以早期发现心肌病变。
3.心肌钙化如何产生病理性Q波?
本例最值得关注的学术问题在于:局灶性心肌钙化是否可能通过非缺血性机制产生病理性Q波?结合现有影像学证据与电生理理论,作者提出了以下几点可能的机制假说:
➤占位效应与心肌替代:心尖部巨大的钙化灶(约3.0cm×4.0cm)占据了大范围心肌空间,钙化组织作为电惰性物质替代了具有电活性的心肌细胞,导致局部心室肌在除极过程中无法产生有效的电活动,形成局灶性电静止区。
➤除极向量丧失:由于钙化灶累及的区域(心尖部、高侧壁)在正常生理情况下参与QRS波的初始除极向量构成,当这些区域的心肌被钙盐取代后,指向该方向的除极向量消失,在对应导联(I、aVL、V5、V6)表现为起始负向波,即病理性Q波。
➤机械压迫与继发性改变:钙化灶可能对周围心肌组织产生慢性机械压迫,导致局部微循环障碍、心肌细胞缺血、纤维化,进一步扩大电异常区域。
➤电重构的潜在影响:钙化灶周围的炎症微环境、心肌细胞间连接蛋白的改变等因素,也可能参与局部传导异常的形成。
从机制类比的角度看,这一过程与心肌梗死后瘢痕形成导致病理性Q波的原理具有相似性:均为具有电活性的心肌组织被电惰性组织(瘢痕或钙化)取代。其根本区别在于,前者的病因是缺血性坏死,后者的病因是钙磷代谢紊乱导致的转移性钙化沉积。
参考文献:
[1] Li D,Huang Q,Situ X,Gao W, Li D.Case Report: A case of myocardial calcification combined with abnormal Q waves on electrocardiogram. Front Cardiovasc Med[J].2026,12:1745357.
[2] Hoang K,Bravo-Jaimes K,Ocazionez D.Myocardial calcifications: thinking beyond the heart.Am J Med[J].2020,133(10):e591–592.
[3] Pawa A,Savani S,Chammany M,Mukherjee S,Gayle K.An intriguing case of myocardial deposits. Cureus[J].2024),16(8):e67226.
责编|Zelda
封面图来源|视觉中国

出院又住院!老人的肺炎不断反复,没想到隐匿的“元凶”竟藏在这种药中……丨医起推理吧

医生将2粒药打成21粒致患者身体不适,官方通报
医脉通是专业的在线医生平台,“感知世界医学脉搏,助力中国临床决策”是平台的使命。医脉通旗下拥有「MedSeeker」「临床指南」「用药参考」「医学文献王」「医知源」「e研通」「e脉播」等系列产品,全面满足医学工作者临床决策、获取新知及提升科研效率等方面的需求。

☟戳这里,更有料!
