聚焦 | 《国家药品不良反应监测年度报告(2025年)》(全文)
4月27日,国家药品不良反应监测中心发布《国家药品不良反应监测年度报告(2025年)》(以下简称《报告》)。《报告》显示,2025年全国药品不良反应监测网络收到《药品不良反应/事件报告表》272.8万份,我国每百万人口平均报告数为1935份,全国97.9%的县级地区报告了药品不良反应/事件。
全文如下
↓↓
《国家药品不良反应监测年度报告(2025 年)》
第 1 章 药品不良反应监测工作情况
2025 年,国家药品不良反应监测中心在国家药品监督管理局的领导下,坚持以习近平新时代中国特色社会主义思想为指导,全面贯彻党的二十大和二十届历次全会精神,认真落实国家药品监督管理局决策部署,按照 “讲政治、强监管、保安全、促发展、惠民生” 的工作思路,统筹推进药品不良反应监测评价工作高质量发展,为药品安全全链条监管提供了强有力支撑,切实保护和促进公众健康。
一是筑牢制度根基,法规制度体系更加健全。发布《药品上市后安全性评价技术指导原则》《药品上市后风险沟通技术指导原则》《真实世界数据支持药品安全性主动监测的一般原则》等技术指南,配合《药品不良反应报告和监测管理办法》《药物警戒检查要点和检查细则》等修订,推动药物警戒制度建立健全。
二是坚持深化改革,监测评价体系更加完善。开展国家和省级中心一体化监测评价协作平台建设与应用。加强国家药品不良反应监测哨点警戒能力建设,联合监测哨点探索开展上市后主动监测研究。开展药品上市许可持有人药物警戒检查,指导督促持有人建立完善药物警戒体系,主动监测、报告和分析不良反应。
三是强化风险防控,技术支撑能力全面加强。关注重点领域、重点品种风险,强化创新药、国家集采药品监测评价。完成炎琥宁注射剂、人纤维蛋白原等药品安全性评价,根据评价结果,国家药品监督管理局发布药品说明书修订公告 19 期、注销药品注册证书公告 1 期。
四是坚持开放发展,国际交流合作持续深化。参加人用药品技术要求国际协调理事会(ICH)、国际药品监管机构联盟(ICMRA)相关国际工作组会议,推动新发布的 ICH E2D(R1)指导原则在我国转化实施。牵头 ICH M1 工作,2025 年国家药品监督管理局当选为 ICH 监管活动医学词典(MedDRA)指导委员会成员,深度参与国际规则制定和 ICH 管理工作。
五是坚持协同共治,社会共治格局更加优化。以 “科学认知,安全用药” 为主题开展全国 “携手共建药品安全防线” 活动,面向各省征集优秀科普作品,在中心官网、“中国药物警戒” 微信公众号发布,进一步提升公众的安全意识和科学素养,营造良好的社会共治氛围。
第 2 章 药品不良反应 / 事件报告情况
2.1 报告总体情况
2.1.1 2025 年度药品不良反应 / 事件报告情况
2025 年全国药品不良反应监测网络收到《药品不良反应 / 事件报告表》272.8 万份。1999 年至 2025 年,全国药品不良反应监测网络累计收到《药品不良反应 / 事件报告表》2860.0 万份(图1)。
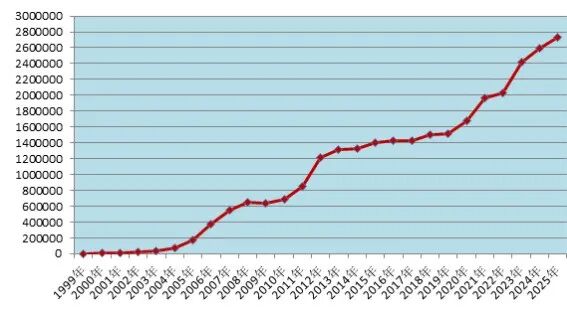
图1 1999年—2025年全国药品不良反应/事件报告数量增长趋势
2.1.2 新的和严重药品不良反应 / 事件报告情况
2025 年全国药品不良反应监测网络收到新的和严重药品不良反应 / 事件报告 93.7 万份;新的和严重药品不良反应 / 事件报告占同期报告总数的 34.3%。
2025 年全国药品不良反应监测网络收到严重药品不良反应 / 事件报告 50.8 万份,严重药品不良反应 / 事件报告占同期报告总数的 18.6%(图2)。
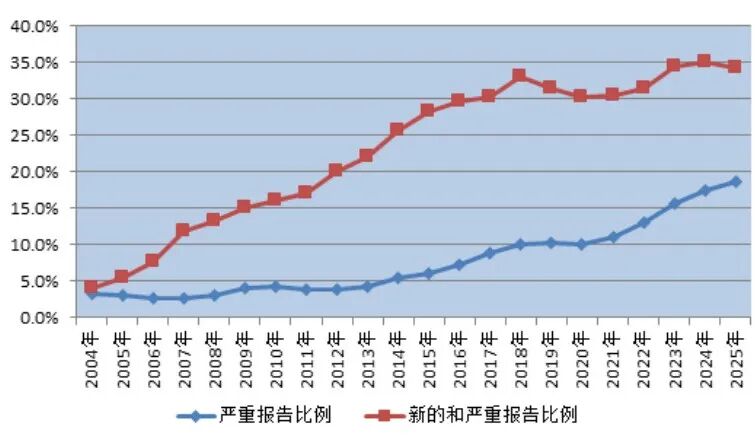
图2 2004年一2025年新的和严重以及严重药品不良反应/事件报告比例
2.1.3 每百万人口平均报告情况
每百万人口平均报告数量是衡量一个国家药品不良反应监测工作水平的重要指标之一。2025 年我国每百万人口平均报告数为 1935 份。
2.1.4 药品不良反应 / 事件县级报告比例
药品不良反应 / 事件县级报告比例是衡量我国药品不良反应监测工作均衡发展及覆盖程度的重要指标之一。2025 年全国 97.9% 的县级地区报告了药品不良反应 / 事件。
2.1.5 报告来源情况
持有人、经营企业和医疗机构是药品不良反应报告的责任单位。按照报告来源统计,2025 年来自医疗机构的报告占 91.5%、来自经营企业的报告占 4.4%、来自持有人的报告占 4.0%、来自其他报告者的报告占 0.1%(图3)。
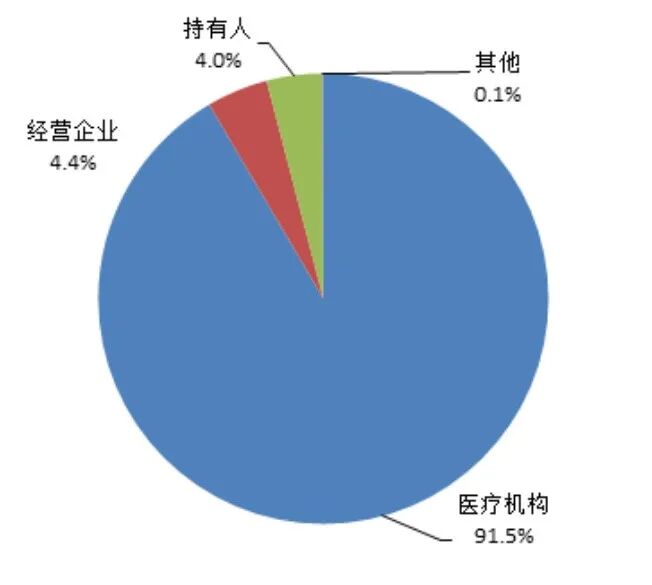
图3 2025年药品不良反应/事件报告来源
按照报告数量统计,2025 年持有人报送药品不良反应 / 事件报告共计 108030 份,同比增长 13.7%。其中,新的和严重药品不良反应 / 事件报告占持有人报告总数的 55.2%。
2.1.6 报告人职业情况
按照报告人职业统计,医生占 56.9%、药师占 25.3%、护士占 11.9%、其他职业占 5.9%(图4)。
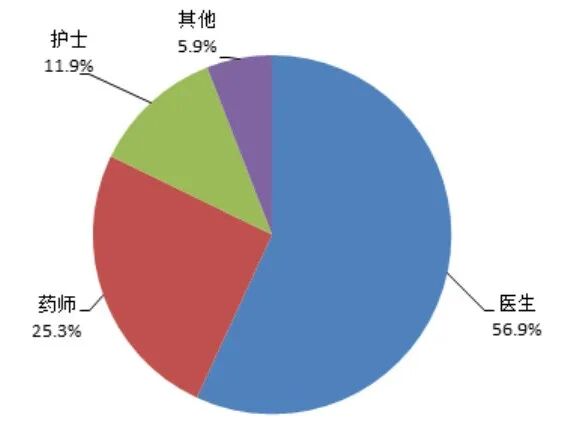
图4 2025年报告人职业构成
2.1.7 涉及患者情况
2025 年药品不良反应 / 事件报告中,男女性别比为 0.84∶1。从年龄分布看,14 岁及以下儿童患者占 7.6%,65 岁及以上老年患者占 35.0%(图5)。
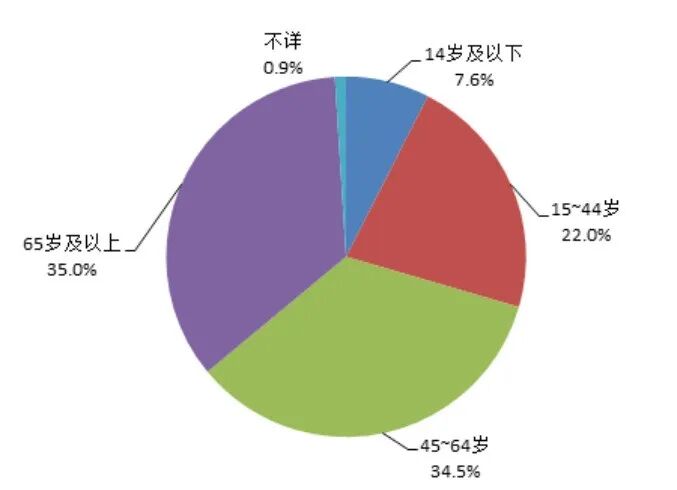
图5 2025年药品不良反应/事件报告涉及患者年龄
2.1.8 涉及药品情况
按照怀疑药品类别统计,化学药品占 79.5%、中药占 11.8%、生物制品占 4.3%、无法分类占 4.4%(图6)。
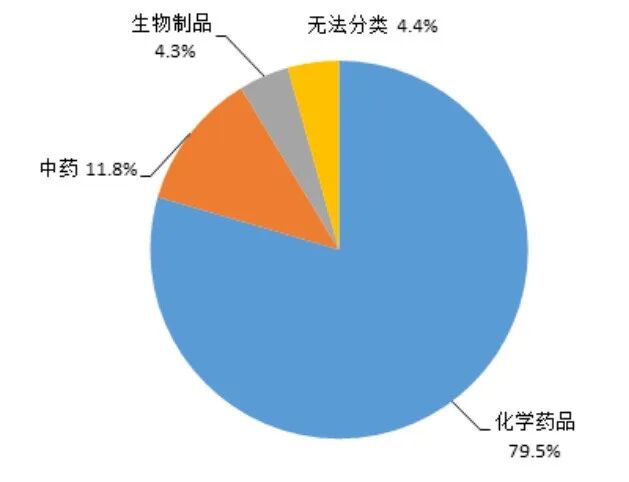
图6 2025年药品不良反应/事件报告涉及药品类别
按照给药途径统计,2025 年药品不良反应 / 事件报告中,注射给药占 56.0%、口服给药占 32.6%、其他给药途径占 11.4%;注射给药中,静脉注射给药占 90.3%、其他注射给药占 9.7%(图7)。
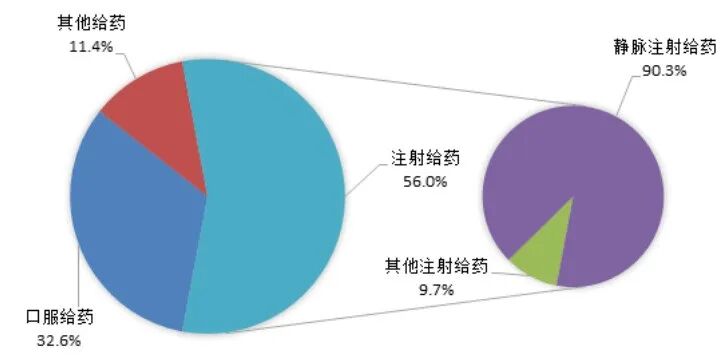
图7 2025年药品不良反应/事件报告涉及给药途径
2.1.9 累及器官系统情况
2025 年药品不良反应 / 事件报告中,累及器官系统排名前 3 位依次为胃肠系统疾病、皮肤及皮下组织类疾病、各类检查(图8)。
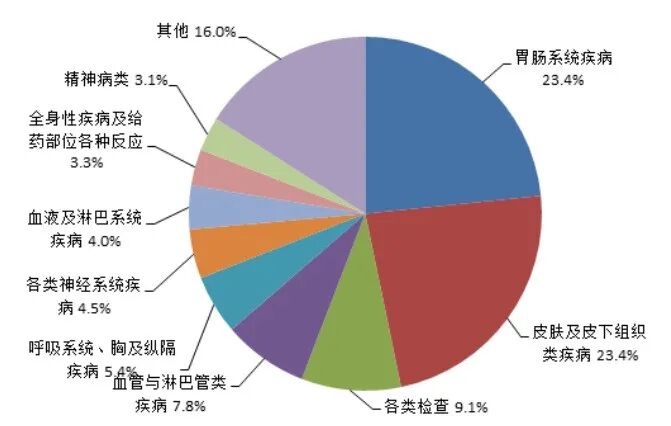
图8 2025年药品不良反应/事件累及器官系统
2.2 化学药品监测情况
2.2.1 总体情况
2025 年药品不良反应 / 事件报告中,涉及怀疑药品 305.4 万例次,其中化学药品占 79.5%。2025 年严重不良反应 / 事件报告涉及怀疑药品 67.0 万例次,其中化学药品占 83.2%。
2.2.2 涉及患者情况
2025 年化学药品不良反应 / 事件报告中,男女性别比为 0.84∶1。14 岁及以下儿童患者占 7.9%,65 岁及以上老年患者占 34.9%。
2.2.3 涉及药品情况
2025 年药品不良反应 / 事件报告涉及的化学药品中,例次数排名前 5 位的类别依次为抗感染药、肿瘤用药、心血管系统用药、镇痛药、神经系统用药。2025 年严重药品不良反应 / 事件涉及化学药品中,报告数量最多的为肿瘤用药,占 35.6%;其次是抗感染药,占 28.3%。
按剂型统计,2025 年化学药品不良反应 / 事件报告中,注射剂、口服制剂所占比例分别为 61.8% 和 31.9%,其他剂型占 6.3%。
2.2.4 总体情况分析
2025 年化学药品不良反应 / 事件报告情况与 2024 年相比未出现显著变化。从不良反应涉及患者年龄看,应持续加强 14 岁及以下儿童、65 岁及以上老年患者的安全用药管理。从化学药品类别上看,抗感染药报告数量仍居首位,其占比呈现小幅下降。
小贴士
如何提高老年患者的安全用药?
临床用药评价公众号:随着年龄的增加,老年人罹患多种疾病和接受多种药物治疗的机会明显增加,多重用药可能存在药物相互作用,增加用药安全风险。因此,应提高老年患者及家属安全用药的意识和能力,保障老年患者的用药安全。
鼓励老年患者按时门诊随访,知晓自己健康状况,一旦出现药物治疗相关的异常反应,及时就诊。建议老年患者设立个人专用药物记录本记录用药及不良反应。老年人由于记忆力减退,容易漏服、多服、误服药物,以致难以获得疗效或加重病情,家属需定时检查老年患者用药情况,做到按时、按医嘱规定剂量服药,协助老年患者提高用药依从性和用药管理。
此外,建议老年人及其家属避免随意用药,不宜凭自己的经验自作主张,随便联合用药,不轻信民间 “偏方”、“秘方” 等。
2.3 中药监测情况
2.3.1 总体情况
2025 年药品不良反应 / 事件报告中,涉及怀疑药品 305.4 万例次,其中中药占 11.8%;2025 年严重不良反应 / 事件报告涉及怀疑药品 67.0 万例次,其中中药占 4.7%。
2.3.2 涉及患者情况
2025 年中药不良反应 / 事件报告中,男女性别比为 0.78∶1。14 岁及以下儿童患者占 6.0%,65 岁及以上老年患者占 33.5%。
2.3.3 涉及药品情况
2025 年药品不良反应 / 事件报告涉及的中药中,例次数排名前 5 位的类别分别是理血剂中活血化瘀药、清热剂中清热解毒药、祛湿剂中清热除湿药、补益剂中益气养阴药、祛湿剂中祛风胜湿药。2025 年中药严重不良反应 / 事件报告中,例次数排名前 5 位的类别分别是理血剂中活血化瘀药、清热剂中清热解毒药、补益剂中益气养阴药、开窍剂中凉开药、祛湿剂中清热除湿药。
2025 年中药不良反应 / 事件报告中,注射剂和口服制剂所占比例分别为 24.4% 和 64.1%。
2.3.4 总体情况分析
与 2024 年相比,2025 年中药不良反应 / 事件报告数略有增加,严重不良反应 / 事件报告占比为 8.6%,低于总体药品不良反应 / 事件报告中严重不良反应 / 事件报告占比。从药品类别上看,活血化瘀药的报告数量仍居首位。从总体情况看,2025 年中药占总体不良反应 / 事件报告比例呈下降趋势,但仍需要注意安全用药。
小贴士
如何看待中药的不良反应?
临床用药评价公众号:“是药三分毒”,中药和其他药品一样,在发挥治疗作用的同时,也可能会产生不良反应。辨证论治是中医认识疾病和治疗疾病的基本原则,严格按照说明书规定的功能主治使用中药,有助于减少和避免不良反应 / 事件的发生。如果不遵循中医辨证论治的原则或者辨证不当、超说明书功能主治用药,可能增加中药不良反应 / 事件发生风险。随着中药临床使用日趋广泛,应提高中药安全使用的意识。
2.4 生物制品监测情况
2.4.1 总体情况
2025 年药品不良反应 / 事件报告中,涉及怀疑药品 305.4 万例次,其中生物制品占 4.3%。2025 年严重不良反应 / 事件报告涉及怀疑药品 67.0 万例次,其中生物制品占 7.3%。
2.4.2 涉及患者情况
2025 年生物制品不良反应 / 事件报告中,男女性别比为 1.06∶1。14 岁及以下儿童患者占 6.4%,65 岁及以上老年患者占 33.5%。
2.4.3 涉及药品情况
2025 年药品不良反应 / 事件报告涉及的生物制品中,例次数排名前 5 位的类别依次为抗肿瘤药和免疫机能调节药、消化道及代谢用药、血液和造血器官用药、系统用抗感染药、非性激素和胰岛素类的激素类系统用药。2025 年严重药品不良反应 / 事件涉及生物制品中,报告数量最多的为抗肿瘤药和免疫机能调节药,占 79.8%;其次是消化道及代谢用药,占 7.4%。
2.4.4 报告来源情况
2025 年生物制品不良反应 / 事件报告中,医疗机构报告占 74.6%、持有人报告占 25.2%、经营企业和其他机构报告占 0.2%。严重报告中,医疗机构报告占 78.1%、持有人报告占 21.8%、经营企业和其他机构报告占 0.1%。
2.4.5 总体情况分析
2025 年生物制品不良反应 / 事件报告中,从涉及患者年龄看,14 岁及以下儿童患者和 65 岁及以上老年患者占比同药品总体不良反应的情况基本一致。从生物制品类别上看,抗肿瘤药和免疫机能调节药居于首位,排名前 5 位的药品以单克隆抗体类抗肿瘤药居多。从报告来源上看,来自持有人报告占生物制品报告总数的 25.2%,高于总体报告中持有人报告的占比。
小贴士
什么是生物制品?
临床用药评价公众号:依据《中华人民共和国药典》(2025 年版),生物制品是指以微生物、细胞、动物或人源组织和体液等为起始原材料,用生物学技术制成,用于预防、治疗和诊断人类疾病的制剂。
2.5 基本药物监测情况
2.5.1 国家基本药物监测总体情况
2025 年全国药品不良反应监测网络共收到《国家基本药物目录(2018 年版)》收载品种的不良反应 / 事件报告 121.3 万份,其中严重报告 24.8 万份,占 20.4%。报告涉及化学药品和生物制品占 87.9%,中成药占 12.1%。
2.5.2 国家基本药物化学药品和生物制品情况分析
《国家基本药物目录(2018 年版)》化学药品和生物制品部分共 417 个(类)品种。2025 年全国药品不良反应监测网络共收到国家基本药物化学药品和生物制品药品不良反应 / 事件报告 116.9 万例次,其中严重报告 28.9 万例次,占 24.7%。
2025 年国家基本药物化学药品和生物制品不良反应 / 事件报告按照药品类别统计,报告数量排名前 5 位的分别是抗微生物药、抗肿瘤药、心血管系统用药、激素及影响内分泌药、治疗精神障碍药;累及器官系统排名前 5 位的是皮肤及皮下组织类疾病、胃肠系统疾病、各类检查、血管与淋巴管类疾病、各类神经系统疾病。
2.5.3 国家基本药物中成药情况分析
《国家基本药物目录(2018 年版)》中成药共涉及 268 个(类)品种。2025 年全国药品不良反应监测网络共收到国家基本药物中成药不良反应 / 事件报告 15.6 万例次,其中严重报告 14571 例次,占 9.3%。2025 年国家基本药物 7 大类中成药中,药品不良反应 / 事件报告总数由多到少依次为内科用药、骨伤科用药、妇科用药、外科用药、耳鼻喉科用药、儿科用药、眼科用药。
监测数据表明,2025 年国家基本药物监测总体情况基本保持平稳。
第 3 章 相关风险控制措施
根据 2025 年药品不良反应监测数据和分析评价结果,国家药品监督管理局对发现存在安全隐患的药品及时采取相应风险控制措施,以保障公众用药安全。
发布人血白蛋白注射剂、炎琥宁注射剂、小活络制剂等药品说明书修订公告共 19 期,增加或完善 26 个(类)品种说明书中的警示语、不良反应、注意事项、禁忌等安全性信息。发布《国家药监局关于注销安喘片等 5 个品种药品注册证书的公告》。
发布《药物警戒快讯》12 期,报道国外药品安全信息 50 条。
第 4 章 各论
4.1 抗感染药不良反应监测情况
本报告中的抗感染药是指具有杀灭或抑制各种病原微生物作用的化学药品,包括抗生素、合成抗菌药、抗真菌药、抗病毒药等,是临床应用最为广泛的药品类别之一,其不良反应 / 事件报告数量一直居于首位,是药品不良反应监测工作关注的重点。
2025 年全国药品不良反应监测网络共收到抗感染药不良反应 / 事件报告 77.8 万份,其中严重报告 14.5 万份,占 18.6%。抗感染药不良反应 / 事件报告数量占 2025 年总体报告数量的 28.5%。
4.1.1 涉及药品情况
2025 年抗感染药不良反应 / 事件报告数量排名前 3 位的药品类别分别是头孢菌素类、喹诺酮类、青霉素类,严重不良反应 / 事件报告数量排名前 3 位的药品类别分别是头孢菌素类、喹诺酮类、β- 内酰胺酶抑制药。
2025 年抗感染药不良反应 / 事件报告中,注射剂占 78.9%、口服制剂占 18.3%、其他剂型占 2.8%,与药品总体报告剂型分布相比注射剂比例偏高;严重不良反应 / 事件报告中,注射剂占 80.6%、口服制剂占 18.1%、其他剂型占 1.3%。
4.1.2 累及器官系统情况
2025 年抗感染药不良反应 / 事件报告中,与抗感染药的总体报告相比,严重报告的血管与淋巴管类疾病,呼吸系统、胸及纵隔疾病,各类检查构成比偏高。
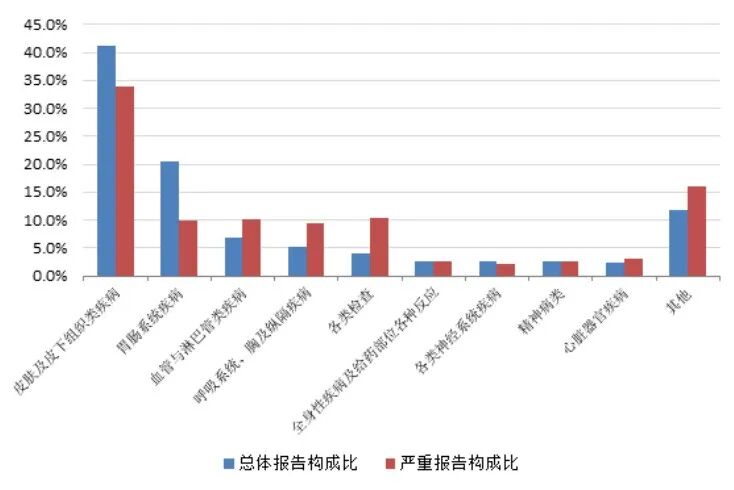
图9 2025年抗感染药不良反应/事件累及器官系统
抗感染药不良反应 / 事件报告中,口服制剂累及器官系统的前 5 位是胃肠系统疾病、皮肤及皮下组织类疾病、各类检查、血管与淋巴管类疾病、精神病类;注射剂累及器官系统前 5 位是皮肤及皮下组织类疾病,胃肠系统疾病,血管与淋巴管类疾病,呼吸系统、胸及纵隔疾病,各类检查。
抗感染药严重药品不良反应 / 事件报告中,口服制剂累及器官系统排名前 5 位的是皮肤及皮下组织类疾病、各类检查、胃肠系统疾病、肝胆系统疾病、代谢及营养类疾病;注射剂累及器官系统排名前 5 位的是皮肤及皮下组织类疾病,血管与淋巴管类疾病,呼吸系统、胸及纵隔疾病,胃肠系统疾病,各类检查。
4.1.3 监测情况分析及安全风险提示
2025 年抗感染药不良反应 / 事件报告数量以及占总体报告比例均呈现下降趋势,但其严重不良反应报告数量和严重报告构成比均出现了增长,提示抗感染药的用药风险仍需继续关注。
小贴士
甲磺酸吉米沙星片使用时应注意些什么?
临床用药评价公众号:吉米沙星为第四代氟喹诺酮类药物,甲磺酸吉米沙星片临床主要用于由肺炎链球菌、流感嗜血杆菌、黏膜炎莫拉菌等敏感菌引起的社区获得性肺炎等的治疗。接受甲磺酸吉米沙星片治疗的患者有发生严重皮肤过敏反应的风险,如多形性红斑、中毒性表皮坏死松解症和史蒂文斯 - 约翰逊综合征。皮疹更常见于 40 岁以下的患者,特别是女性及接受激素替代疗法的女性。皮疹的发生率在治疗时间超过 5 天,尤其是超过 7 天的患者中更高,有的患者可在停药治疗后数天发生。建议患者若发生皮疹,应停用本品并及时就医。
4.2 生物制品抗肿瘤药不良反应监测情况
生物制品抗肿瘤药包括单克隆抗体、抗体偶联药物、细胞治疗药物等。2025 年全国药品不良反应监测网络共收到生物制品抗肿瘤药不良反应 / 事件报告 66187 份,其中严重报告 32566 份,占 49.2%。生物制品抗肿瘤药占 2025 年总体报告数量的 2.4%。
4.2.1 涉及患者情况
2025 年生物制品抗肿瘤药不良反应报告 / 事件中,男女患者比为 1.09∶1。45~64 岁年龄组报告例数最多,占 41.9%。
4.2.2 涉及药品情况
2025 年生物制品抗肿瘤药不良反应报告 / 事件中,数量排名前 3 位的类别为细胞程序性死亡蛋白 1 / 细胞程序性死亡配体 1(PD-1/PDL1)抑制剂、血管内皮生长因子 / 血管内皮生长因子受体(VEGF/VEGFR)抑制剂、人表皮生长因子受体 2(HER-2)抑制剂,严重不良反应报告 / 事件数量排名前 3 位的类别为 PD-1/PD-L1 抑制剂、VEGF/VEGFR 抑制剂、CD20 抑制剂。
4.2.3 累及器官系统情况
2025 年生物制品抗肿瘤药不良反应 / 事件报告中,与生物制品抗肿瘤药的总体报告相比,严重报告的各类检查、血液及淋巴系统疾病构成比偏高。
4.2.4 监测情况分析及安全风险提示
2025 年生物制品抗肿瘤药不良反应 / 事件报告数量约占总体报告数量的 2.4%,严重报告占比高于 2025 年药品不良反应 / 事件总体情况。医务人员和患者均应重视可能的不良反应 / 事件,合理用药、适当预防、及时干预,尽量避免因严重不良反应 / 事件影响治疗。
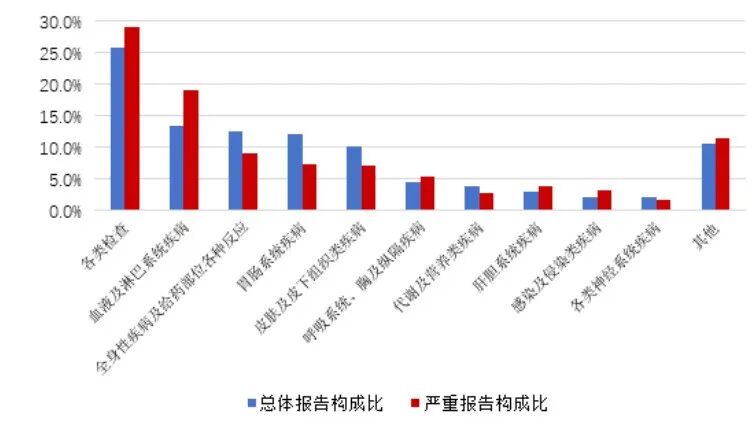
图10 2025年生物制品抗肿瘤药不良反应/事件累及器官系统
4.3 心血管系统用药不良反应监测情况
本报告中的心血管系统用药是指用于心脏疾病治疗、血管保护、血压和血脂调节的化学药品,包括降血压药、抗心绞痛药、血管活性药、抗动脉粥样硬化药、抗心律失常药、强心药、其他心血管系统药等。
2025 年全国药品不良反应监测网络共收到心血管系统用药的不良反应 / 事件报告 19.0 万份,占总体报告的 7.0%;其中严重报告 21821 份,占心血管系统用药的 11.5%。
4.3.1 涉及患者情况
2025 年心血管系统用药不良反应 / 事件报告中,男女性别比为 0.95∶1;严重报告中,男女性别比为 1.09∶1。
2025 年心血管系统用药不良反应 / 事件报告中,45~64 岁与 65 岁及以上年龄组分别占 39.7% 和 50.7%,远高于其他年龄组比例;严重报告中,65 岁及以上年龄组占 54.8%。
4.3.2 涉及药品情况
2025 年心血管系统用药不良反应 / 事件报告数量排名前 3 位的药品类别是降血压药、抗心绞痛药、抗动脉粥样硬化药;心血管系统用药严重报告数量排名前 3 位的药品类别是抗动脉粥样硬化药、降血压药、抗心绞痛药。
2025 年心血管系统用药不良反应 / 事件报告中,注射剂占 27.5%、口服制剂占 70.1%、其他剂型占 2.4%;严重报告中,注射剂占 35.7%、口服制剂占 61.5%、其他剂型占 2.8%。
4.3.3 累及器官系统情况
2025 年心血管系统用药不良反应 / 事件报告中,口服制剂累及器官系统排名前 5 位是胃肠系统疾病、各类神经系统疾病、血管与淋巴管类疾病、皮肤及皮下组织类疾病、代谢及营养类疾病;注射剂累及器官系统前 5 位是胃肠系统疾病、各类神经系统疾病、皮肤及皮下组织类疾病、血管与淋巴管类疾病、心脏器官疾病。
2025 年心血管系统用药严重不良反应 / 事件报告中,口服制剂累及器官系统排名前 5 位的是各类检查、肝胆系统疾病、皮肤及皮下组织类疾病、血管与淋巴管类疾病、代谢及营养类疾病;注射剂累及器官系统排名前 5 位的是血管与淋巴管类疾病,皮肤及皮下组织类疾病,呼吸系统、胸及纵隔疾病,胃肠系统疾病,心脏器官疾病。
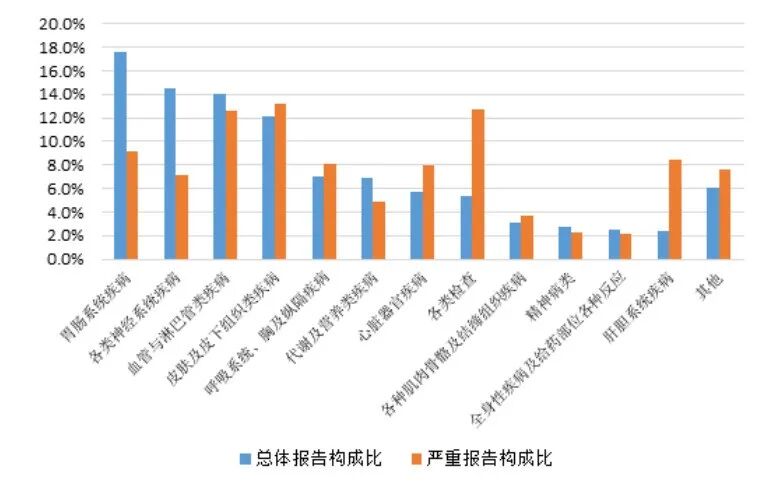
图11 2025年心血管系统用药不良反应/事件累及器官系统
4.3.4 监测情况分析及安全风险提示
2025 年心血管系统用药不良反应 / 事件报告中,降血压药为报告数最多的心血管类药物,这与高血压的治疗药物种类较多有关,还与高血压的发病率较高、用药人群基数大相关。严重不良反应 / 事件报告中,抗动脉粥样硬化药的报告占比第一,其中他汀类报告的数量最多,不良反应表现主要为肝功能异常,提示医务人员和患者应关注抗动脉粥样硬化药的肝损害风险。
4.4 儿童用药不良反应监测情况
2025 年全国药品不良反应监测网络共收到 14 岁及以下儿童患者报告占总报告数 7.6%。儿童患者严重报告占儿童患者总报告数 16.5%。
4.4.1 涉及患者情况
2025 年儿童患者药品不良反应 / 事件报告中,男女性别比为 1.27∶1。2025年儿童患者药品不良反应/事件报告年龄分组情况见图12。
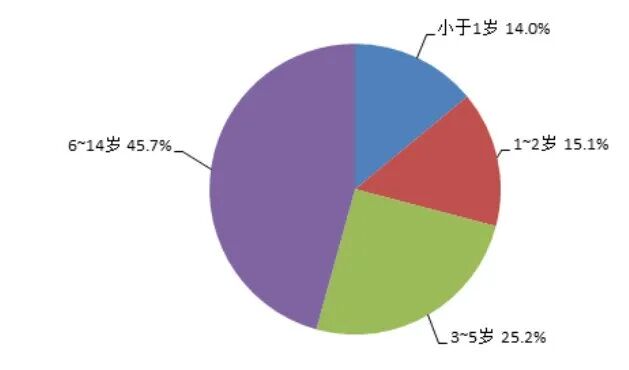
图12 2025年儿童患者药品不良反应/事件报告涉及患者年龄
4.4.2 涉及药品情况
按照药品类别统计,化学药品占 87.0%、中药占 9.8%、生物制品占 3.2%。化学药品排名前 5 位的是抗感染药,电解质、酸碱平衡及营养药,呼吸系统用药,代谢及内分泌系统用药,肿瘤用药。中药排名前 5 位的是清热剂、解表剂、止咳平喘剂、祛痰剂、祛湿剂。
2025 年儿童药品不良反应 / 事件报告中,注射剂占 70.0%,口服制剂占 22.6%,其他制剂占 7.4%。化学药品不良反应 / 事件报告中,注射剂、口服制剂所占比例分别为 74.9% 和 7.9%。中药不良反应 / 事件报告中,注射剂、口服制剂所占比例分别为 24.6% 和 72.0%。
4.4.3 累及器官系统情况
2025 年儿童药品不良反应 / 事件报告中,累及器官系统排名前 3 位的是皮肤及皮下组织类疾病、胃肠系统疾病、血管与淋巴管类疾病。化学药品累及系统排名前 3 位的是皮肤及皮下组织类疾病、胃肠系统疾病、血管与淋巴管类疾病。中药累及系统排名前 3 位的是胃肠系统疾病、皮肤及皮下组织类疾病、血管与淋巴管类疾病。
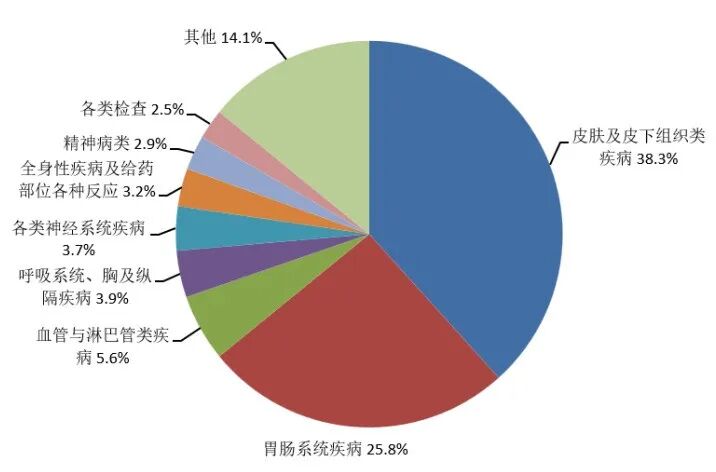
图13 2025年儿童患者药品不良反应/事件累及器官系统
4.4.4 监测情况分析及安全风险提示
2025 年儿童药品不良反应 / 事件报告占报告总数的 7.6%,较 2024 年下降 1.1 个百分点;其中严重报告占比 16.5%,较总体报告中严重报告构成比低 2.1 个百分点。药物治疗是儿童防病治病的主要手段,因儿童生长期的生理特点,对药物具有特殊的反应性和敏感性,因此应持续关注儿童人群用药安全。
2025 年统计数据显示,儿童患者用药在药品类别分布上,化学药品延续了 2024 年的分布特征,电解质、酸碱平衡及营养药、抗感染药、呼吸系统用药的构成比高于该类别在化学药品总体报告中的构成比;中药排名前 5 位的类别依次为清热剂、解表剂、止咳平喘剂、祛痰剂、祛湿剂,该分布特征与儿童常见疾病谱及生理发育特点高度一致。儿童用药要严格遵循临床用药规范,优先选择安全系数更高的给药途径,同时强化用药全程的不良反应监测,最大限度降低用药风险。
第 5 章 有关说明
5.1 本年度报告中的数据来源于国家药品不良反应监测数据库中 2025 年 1 月 1 日至 2025 年 12 月 31 日各地区上报的数据。
5.2 与大多数国家一样,我国药品不良反应报告是通过自发报告系统收集并录入到数据库中的,存在自发报告系统的局限性,如漏报、填写不规范、信息不完善、无法计算不良反应发生率等。
5.3 每种药品不良反应 / 事件报告的数量受到该药品的使用量和不良反应发生率等诸多因素的影响,故药品不良反应 / 事件报告数量的多少不直接代表药品不良反应发生率的高低或者严重程度。
5.4 本年度报告完成时,其中一些严重报告尚在调查和评价的过程中,所有统计结果均为现阶段数据收集情况的真实反映,并不代表最终的评价结果。
5.5 本年度报告相关医学术语统计采用人用药品技术要求国际协调理事会(ICH)监管活动医学词典(MedDRA)。MedDRA 是在 ICH 主办下编制的标准化国际医学术语集,用于与人用医疗产品相关的监管沟通和数据评估。各类检查是 MedDRA 中的一项系统器官分类,包括有限定词(例如:升高、降低、异常、正常)和没有限定词的检查名称。
5.6 专业人士会分析药品与不良反应 / 事件的关联性,提取药品安全性风险信息,根据风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入安全性信息,更新药品如何安全使用的信息等。当药品的获益不再大于风险时,药品会撤市。
5.7 本年度报告数据均来源于全国药品不良反应监测网络,不包含疫苗不良反应 / 事件的监测数据。目前,全国药品不良反应监测网络中的化学药品、中药、生物制品基于药品特点采用不同分类,相关表述存在不同。




来源:国家药品不良反应监测中心、临床用药评价
编辑:谯英固
审核:赵燕宜

