首款体内 CRISPR 基因编辑疗法冲刺明年上市,全球管线竞速

2026 年 4 月 29 日
医麦客新闻 eMedClub News
4 月 27 日,Intellia Therapeutics 宣布其体内 CRISPR 基因编辑疗法 lonvo-z(NTLA-2002)治疗遗传性血管性水肿(HAE)的全球 Ⅲ 期 HAELO 试验达到主要终点及所有关键次要终点,并已启动向 FDA 滚动递交 BLA,预计于 2027 年上半年在美国上市。值得一提的是,这是全球体内基因编辑疗法领域首次报告 Ⅲ 期阳性数据。
HAELO 是一项随机、双盲、安慰剂对照的 Ⅲ 期试验,共纳入 80 例 Ⅰ 型或 Ⅱ 型 HAE 患者(52 例接受单次 50 mg lonvo-z,28 例接受安慰剂)。
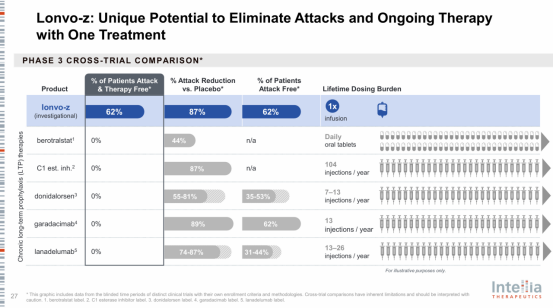
结果显示,该研究达到了主要终点。在六个月的疗效评估期(第 5-28 周)内,Lonvo-z 组患者的 HAE 发作频率相比安慰剂组降低了 87%(平均月发作率:0.26 vs 2.10,p<0.0001)。
此外,该研究达到了所有关键次要终点。其中包括 62% 的患者在六个月疗效评估期内疾病未发作且无需再接受治疗,而安慰剂组这一比例为 11%。
Lonvo-z 在该研究中展现出良好的安全性和耐受性。最常见的治疗期间不良事件为输注相关反应、头痛、疲劳等,均为轻度或中度。
lonvo-z 通过 LNP 递送 CRISPR-Cas9 系统,单次静脉输注即可永久灭活肝脏中的 KLKB1 基因,从源头降低激肽释放酶和缓激肽水平,有望成为首个一次性 HAE 治疗药物。其已获 FDA 再生医学先进疗法和孤儿药认定等多项资格。
HAE 是一种罕见的遗传性疾病,全球患病率约 1/50,000,以反复、不可预测的严重肿胀发作为特征,可危及生命。lonvo-z 的差异化优势在于其「单次给药、终身获益」的治疗范式,而现有 HAE 标准治疗——包括 Takeda 的 Takhzyro、BioCryst 的 Orladeyo 及 Ionis 新获批上市的 Dawnzera——均需长期甚至终身用药。

Intellia 另一核心管线 nex-z 同样为 LNP 递送 CRISPR/Cas9 体内基因编辑疗法 Nex-z,靶向肝细胞中的 TTR 基因。 当下,其针对转甲状腺素蛋白淀粉样变性心肌病(ATTR-CM)和遗传性转甲状腺素蛋白淀粉样变性多发性神经病(ATTRv-PN)两项适应症均已推进至 Ⅲ 期临床。
尽管该疗法曾于去年 10 月因一例严重肝毒性致死事件被 FDA 暂停临床试验,其后续重启被视为监管科学与产业研发深度协作的标志性成果。此次 lonvo-z 研究中良好的安全性在一定程度上缓解了市场对平台安全性的担忧,但也有分析师指出,lonvo-z 的 Ⅲ 期试验样本量较小,仍需更多数据验证。
全球管线竞速:
体内 CRISPR 开启竞速赛
早在 2023 年 10 月,全球首款 CRISPR 基因编辑疗法获批上市,为 CRISPR Therapeutics 与 Vertex 合作开发的 Casgevy。该疗法利用 CRISPR/Cas9 在体外编辑患者造血干细胞,使血红细胞生产高水平的胎儿血红蛋白而发挥治疗作用。但体外编辑的复杂生产流程和高昂成本限制了可及性。
相比之下,体内 CRISPR(如 lonvo-z)作为现货型单次输注产品,在生产可扩展性和患者可及性上具备潜在优势,若获批将开辟全新的市场空间。据预计,全球基于 CRISPR 的基因编辑市场规模到 2034 年将增长至约 133.9 亿美元,而体内编辑领域将以最快的速度增长。
在这一趋势下,全球多家企业的代表性体内 CRISPR 管线已进入临床验证的关键阶段,各有侧重,竞争格局日趋清晰。
CRISPR Therapeutics 进展靠前管线 CTX310 是一款基于 LNP 递送 CRISPR/Cas9 的体内基因编辑疗法,靶向 ANGPTL3 基因。Ⅰ 期临床数据显示,单次静脉输注即可实现甘油三酯与低密度脂蛋白的深度、持久降低,且安全性良好。基于该结果,该疗法已进入 Ⅰb 期临床,重点开发针对重度高甘油三酯血症及难治性高胆固醇血症。
张锋教授创立 Arbor Biotechnologies 开发的 ABO-101 由 LNP 递送表达新型 V 型 CRISPR Cas12i2 核酸酶的 mRNA 和一种优化的引导 RNA,特异性靶向人体 HAO1 基因,从源头治疗原发性高草酸尿症 1 型(PH1),后被 Chiesi Group(凯西集团)获得该管线全球独家权利。目前处于 Ⅰ/Ⅱ 期临床试验阶段。
Precision 开发 PBGENE-HBV 是进入临床阶段的首个靶向 HBV 的体内基因编辑疗法,旨在通过消除乙型肝炎病毒(HBV)的共价闭合环状 DNA(cccDNA),同时灭活整合在肝细胞中的 HBV DNA,以达到功能性治愈慢性乙型肝炎的目的。目前,正在进行 Ⅰ/Ⅱa 期试验 ELIMINATE-B。
在国内,尧唐生物 LNP 递送 CRISPR/Cas 基因编辑工具 YolCas12 HF 体内基因编辑疗法 YOLT-203 已于 2025 年 11 月获 FDA 批准,启动全球首个 PH1 体内基因编辑疗法关键性临床试验。其已获得 FDA 授予的再生医学先进疗法、孤儿药资格认定和罕见儿科疾病资格认定。
锐正基因针对转甲状腺素蛋白淀粉样变性(ATTR)的 LNP 递送的 CRISPR 体内基因编辑疗法 ART001 已经进入了 Ⅱ 期临床研究阶段。去年 5 月公布的临床数据显示,给药 72 周后,高剂量组受试者外周 TTR 蛋白较基线平均下降并稳定维持在 90% 以上,个体最高降幅达 95%。
上述管线主要采用经典的 CRISPR-Cas9 核酸酶策略,通过产生 DNA 双链断裂实现基因敲除。与此同时,以碱基编辑为代表的新一代精准编辑技术正快速迈向临床,其无需切断 DNA 双链即可实现单碱基转换,在安全性上具备理论优势。
例如,Beam Therapeutics 的 LNP 递送碱基编辑器疗法 BEAM-302 治疗 α-1 抗胰蛋白酶缺乏症(AATD)的最新 Ⅰ/Ⅱ 期临床数据已公布,支持该疗法进入关键性开发阶段;Verve Therapeutics(被礼来收购)核心管线 VERVE-102 采用单碱基编辑技术,通过 GalNAc-LNP 将编辑器靶向递送至肝脏,永久性敲低 PCSK9 基因表达,正处于 Ⅰb 期临床试验阶段。
责任编辑丨菊
校对丨菊
参考资料:
1.https://ir.intelliatx.com/news-releases/news-release-details/intellia-therapeutics-reports-positive-phase-3-results
精彩活动
长按识别二维码立即参与↓

点点“分享”、“点赞”和“在看”
给我充点儿电吧~