“戈”破困局·生存获益 | 二线治疗优选:戈沙妥珠单抗为mTNBC中带来显著生存获益


三阴性乳腺癌(TNBC)由于缺乏有效的治疗靶点,靶向治疗选择有限,以化疗为主要治疗手段,生存获益不佳。尤其是一线治疗进展的晚期TNBC(mTNBC)患者,患者预后极差,临床亟需一种新型的治疗方案,以突破疗效瓶颈、改善患者长期生存。近年来,抗体偶联药物(ADC)快速发展,为mTNBC患者带来了新的希望。戈沙妥珠单抗(SG)作为全球首个靶向Trop-2的ADC药物,凭借III期ASCENT研究的突破性数据已成为mTNBC二线治疗优选。基于此,本文将结合mTNBC的诊疗现状,深度解析ASCENT研究的主要结果,明确SG的临床应用价值,为临床决策提供循证依据。
TNBC约占所有乳腺癌的15%~20%,具有疾病进展快、侵袭性强、易复发转移的特点。超过1/3的TNBC患者会发生复发或远处转移,复发或转移性TNBC通常预后较差,5年生存率不足15%[1]。
由于雌激素受体(ER)、孕激素受体(PR)和HER2均呈阴性,mTNBC对内分泌治疗及传统抗HER2靶向治疗不敏感,治疗手段仍以化疗为主[1,2]。目前,对于既往接受过治疗的mTNBC患者,单药化疗仍是其标准方案。然而研究显示,单药化疗的疗效有限,患者的疾病缓解率较低,无进展生存期(PFS)较短[3]。因此,临床亟需一种高效的新型治疗策略以突破当前治疗瓶颈,改善患者长期生存。
近年来,随着研究的深入,新型ADC药物不断涌现,mTNBC的治疗迎来了新选择。Trop-2是一种跨膜钙信号转导蛋白,在包括乳腺癌(>90%)在内的多个肿瘤类型中高表达,是mTNBC领域研究的热门靶点[3]。SG是全球首个获批的Trop-2 ADC药物,III期ASCENT研究显示,其可为既往化疗经治的mTNBC患者带来显著生存获益,为该人群带来了新的希望[3]。
ASCENT研究是一项国际、多中心、随机、对照III期临床试验,入组了529例既往接受过至少2种标准化疗(至少1种用于晚期阶段)的mTNBC患者,旨在比较SG与医生选择化疗(TPC)在该人群中的疗效与安全性。该研究的主要研究终点是独立影像评估(RECIST 1.1标准)的基线无脑转移患者的PFS。次要研究终点包括总生存期(OS)、客观缓解率(ORR)和安全性[3]。
在PFS方面,SG在基线无脑转移人群和ITT人群中的表现均较TPC组显著更优,且在不同亚组人群中观察到一致的PFS获益。结果显示,在基线无脑转移人群中,SG组的中位PFS为5.6个月,显著高于TPC组的1.7个月(HR=0.39,P<0.0001)[4]。在ITT人群中,SG组的中位PFS达4.8个月,同样显著高于TPC组的1.7个月(HR=0.43)。亚组分析显示,无论患者年龄是否≥65岁、既往化疗线数是否>3线、是否接受过PD-1/PD-L1抑制剂治疗、是否初诊为TNBC患者、是否存在肝转移,SG组的中位PFS均优于TPC组,表明SG的疗效不受以上因素影响,能够为更广泛的mTNBC患者带来一致生存获益[3]。
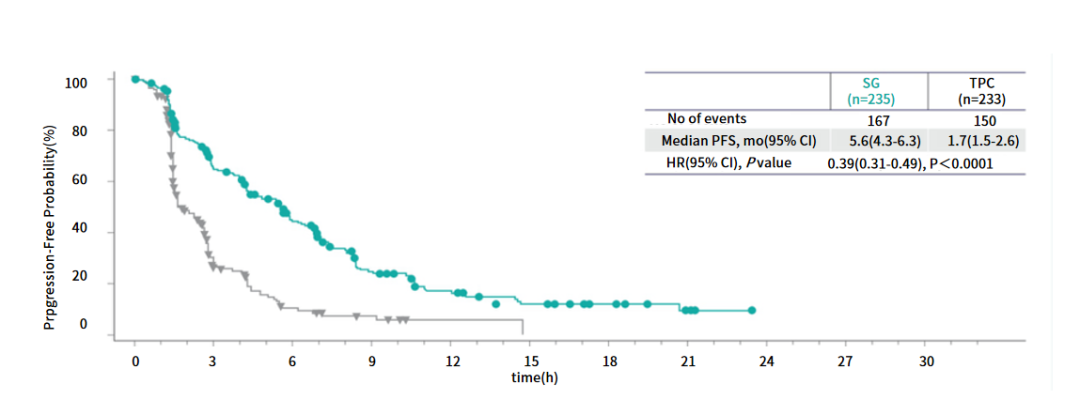
图1 基线无脑转移人群的PFS[4]
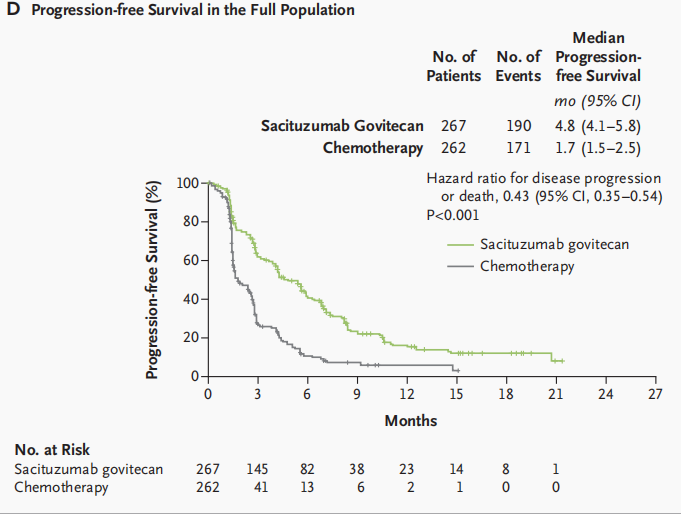
图2 ITT人群的PFS[3]
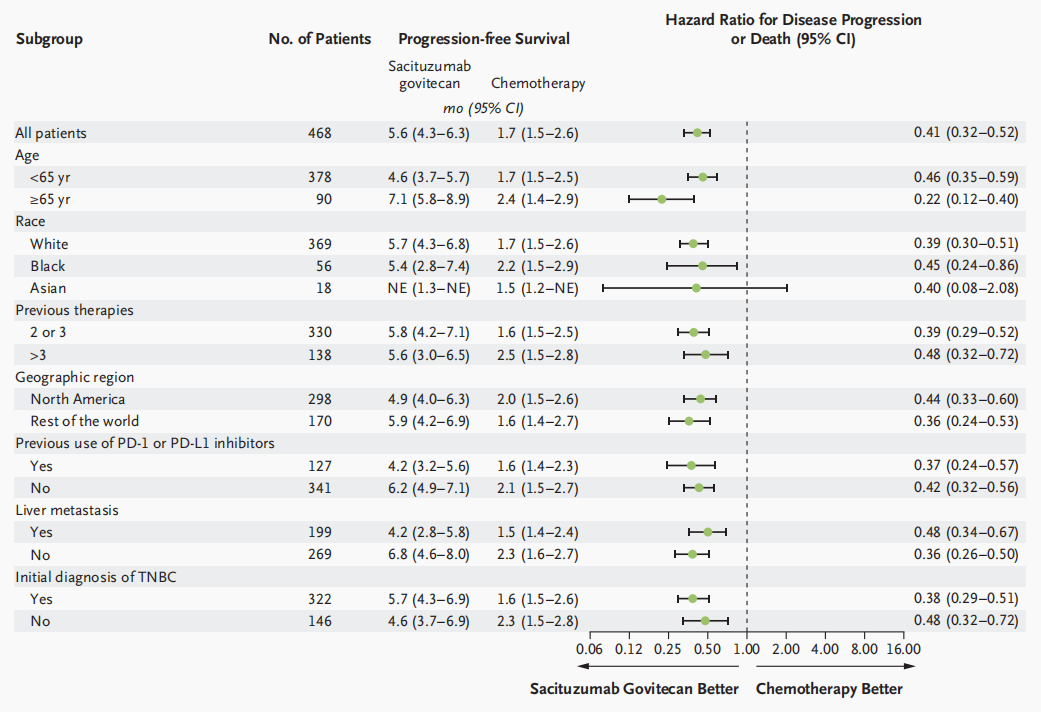
图3 亚组人群PFS分析[3]
在OS方面,SG同样在基线无脑转移人群和ITT人群中展现出显著优于TPC组的疗效。最终分析显示,在基线无脑转移人群中,SG组中位OS达12.1个月,较TPC组的6.7个月显著延长(HR=0.48;P<0.0001);在ITT人群中,SG治疗组的中位OS为11.8个月,同样显著长于TPC组的6.9个月(HR=0.51;P<0.0001)[4]。
另外,SG在ORR、缓解持续时间(DOR)等方面也表现出显著优势。在基线无脑转移的患者中,SG组的ORR达35%,而TPC组仅为5%。SG组的中位DOR为6.3个月,高于TPC组的3.6个月(HR=0.39),进一步验证了其良好的抗肿瘤活性[3]。
SG不但为TNBC患者带来了显著生存获益,同时还展现出可控的安全性。ASCENT研究中,SG组常见的治疗相关不良事件(TEAE)与既往分析结果一致,未出现新的安全信号。SG组最常见的≥3级TEAE为中性粒细胞减少症、白细胞减少症、腹泻、贫血等。在SG组中,治疗相关的任何级别皮疹(9%;其中1例为3级事件)和眼部毒性(5%;无>1级事件)发生率较低,且未观察到>2级的神经病变。SG组和TPC组因TEAE导致的停药率均较低(≤5%)。两组各有3例患者因AE死亡,均判定与SG治疗无关[3]。SG治疗相关的中性粒细胞减少症和腹泻可通过对症治疗进行管理[3]。
ASCENT研究是mTNBC治疗领域的里程碑式研究,该研究证实SG可为经治mTNBC患者带来显著生存获益,打破了mTNBC二线及后线治疗仅依赖化疗的僵局,为该人群提供了一种新型高效治疗方案。同时,ASCENT研究的成功也为后续Trop-2 ADC药物在mTNBC领域中的研发和应用提供了参考。
目前,SG已获得中国国家药品监督管理局(NMPA)批准,用于治疗既往至少接受过2种系统治疗(其中至少1种治疗针对转移性疾病)的不可切除的局部晚期或转移性三阴性乳腺癌成人患者[5],且被国内外权威指南一致推荐作为mTNBC二线治疗优选方案[6,7]。SG凭借突破性的疗效与可控安全性,改变了mTNBC二线及后线治疗格局,为患者带来了全新的治疗选择。未来,随着SG等ADC药物的不断探索,mTNBC的诊疗策略将进一步优化,为更多mTNBC患者带来长期生存获益。
审批编号:CN-TRO-0390
有效期至:2027年12月31日
撰写:ICEY
审校:Elan
排版:Atai
执行:Atai
