Science:靶向氧感知通道的再生医学新范式,靶向HIF1A或成关键
哺乳动物为何无法像两栖动物那样再生肢体,这在生物学领域一直是一个长期存在的谜题。
2026年4月9日,瑞士洛桑联邦理工学院Can Aztekin团队(KellyHu及HanrongHu等为共同第一作者)在Science 在线发表题为“Species-specific oxygen sensing governs the initiation of vertebrate limb regeneration”的研究论文,为了揭示其中的差异所在,该研究对胚胎期的小鼠(Mus musculus)和非洲爪蟾(Xenopus laevis)蝌蚪的肢体截断反应进行了比较。
降低环境中的氧气含量或稳定对氧气敏感的缺氧诱导因子 1A(HIF1A)能够促使小鼠肢体迅速愈合。这种反应伴随着细胞力学、代谢以及一种调控细胞再生状态的组蛋白景观的变化。相反,非洲爪蟾蝌蚪的肢体即使在高氧水平下仍保留了这些特征。它们对氧气的感知能力降低与 HIF1A 调控基因表达的减少有关。因此,该研究结果表明,物种特有的氧气感知能力是一种基本且可靶向的机制,能够激活哺乳动物潜在的再生程序。
一些脊椎动物,比如青蛙的蝌蚪和蝾螈,能够在肢体被截断后重新生长出新的肢体,而哺乳动物则不能。许多与再生相关的分子途径和细胞程序在不同物种之间是共有的,这表明哺乳动物可能具有潜在的肢体再生能力。然而,目前仍不清楚为什么在肢体截断后这些途径和细胞类型不会被激活,以及哺乳动物的肢体再生程序是否原则上能够被启动。
该研究发现,在胚胎小鼠肢体截断后,低于大气压的氧气环境或使对氧气敏感的转录因子——缺氧诱导因子 1A(HIF1A)保持稳定,能够促进伤口的快速愈合。氧气供应减少改变了与 YAP 激活和代谢状态(尤其是糖酵解)相关的细胞生物力学特性。同时,它还通过减少抑制性组蛋白标记 H3K27me3 并增加激活性标记 H3K4me3 来重新配置染色质景观,从而允许再生基因的表达以及形成与肢体再生相关的细胞类型。
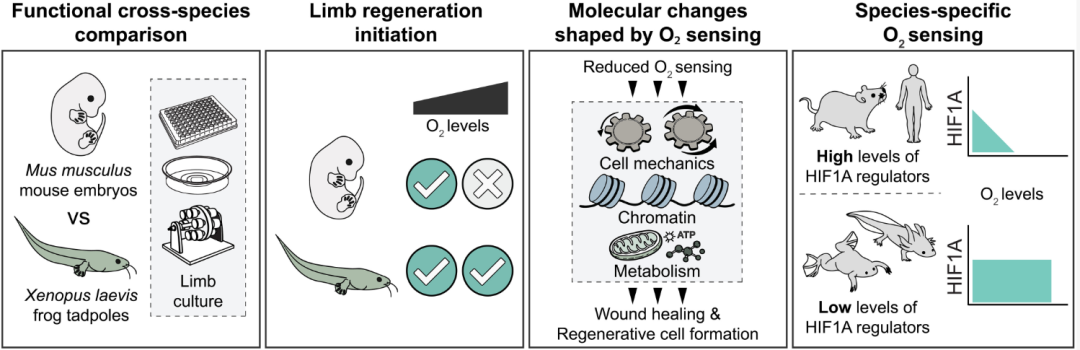
物种特异性的氧感知机制控制着脊椎动物肢体再生的启动过程(图源自Science )
相比之下,大气压下的氧气环境会阻碍这些过程在小鼠肢体中发生。
此外,青蛙蝌蚪的肢体在各种氧气条件下(包括那些远远超过大气氧含量的条件)都能表现出强大的伤口愈合能力、再生细胞类型的形成以及稳定的生物力学、表观遗传和代谢特征。这种低氧感知现象与 HIF1A 调节因子的低表达有关,从而导致相对于小鼠而言 HIF1A 活性保持稳定。进一步分析表明,
再生能力较强的蝾螈体内 HIF1A 调节因子的表达也较低,而人类则表现出与小鼠相似的更强的氧气感知特征。
总之,该研究提出,物种特异性的氧感知能力是脊椎动物四肢再生启动的关键决定因素。
氧感知能力的降低会促进有利于再生的生物力学、表观遗传和代谢程序的启动,其影响范围涵盖发育、疾病、进化以及跨物种比较等方面。最后,研究结果表明,
对氧感知途径的调节能够激活哺乳动物中潜在的四肢再生程序,为诱导成年哺乳动物的四肢再生提供了一种机制途径。
参考消息:
