突破CNV脂质纳米粒介导CRISPR-Cas9编辑实现新突破
湿性年龄相关性黄斑变性(wAMD)等脉络膜新生血管(CNV)疾病,因反复出血、瘢痕形成常导致失明,传统抗 VEGF 疗法存在应答率有限、需终身注射等痛点。近期《Science Advances》发表的一项重磅研究,开发了 H₂O₂响应型动态共价脂质纳米粒(LNPs),为 CNV 治疗提供了长效、安全的基因编辑方案。
文献标题:Dynamically covalent lipid nanoparticles mediate CRISPR-Cas9 genome editing against choroidal neovascularization in mice
发表期刊:Science Advances(IF 12.5)
DOI:10.1126/sciadv.adj0006
一、研究思路:精准靶向,破解传统疗法困局
现有 CNV 治疗面临两大核心难题:一是抗 VEGF 药物需频繁注射,易引发眼内高压、出血等并发症;二是病毒载体介导的基因编辑存在免疫原性和脱靶风险,非病毒载体则面临转染效率低、胞内释放难等问题。
针对这些痛点,研究团队提出创新解决方案:
1. 构建动态共价脂质体库:通过 “一锅法” 合成含亚胺硼酸酯键的脂质体,兼具 pH 和 H₂O₂响应性,实现病变部位精准降解;
2. 优化递送系统:筛选出高效低毒的 LNP-A₄B₃C₇,共递送 Cas9 mRNA 和 VEGFA 靶向 sgRNA,在病变 RPE 细胞内触发释放;
3. 简化给药方式:采用玻璃体腔注射,通过 Müller 细胞转胞吞作用穿透视网膜屏障,避免侵入性更强的视网膜下注射。
二、核心研究成果:长效编辑,疗效超越临床药物
(一)脂质体库筛选与性能验证
研究团队合成了系列含亚胺硼酸酯键的脂质体,经高通量筛选发现 LNP-A₄B₃C₇表现最优:
转染效率显著高于商用转染试剂 Lpf2k 和 FDA 批准的 LNP-ALC-0315(Fig.2D);
细胞毒性低,在 mRNA 浓度达 5μg/ml 时细胞存活率仍超 80%(fig.S20);
可在 CNV 病变部位高浓度 H₂O₂触发下快速降解,释放 mRNA(Fig.3)。
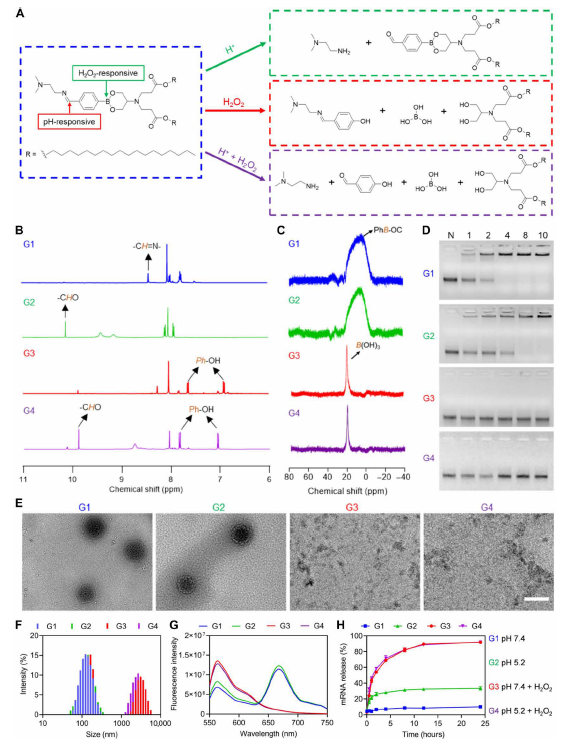
图3:酸和H₂O₂触发的脂质体降解、LNP解离及mRNA释放机制图(原文Fig.3)
(二)体内外基因编辑与治疗效果
1. 体外实验:在 H₂O₂预处理的 RPE 细胞中,LNP-A₄B₃C₇介导的 VEGFA 基因编辑效率达 70.4%,显著降低 VEGFA mRNA 和蛋白分泌(Fig.5E、F);
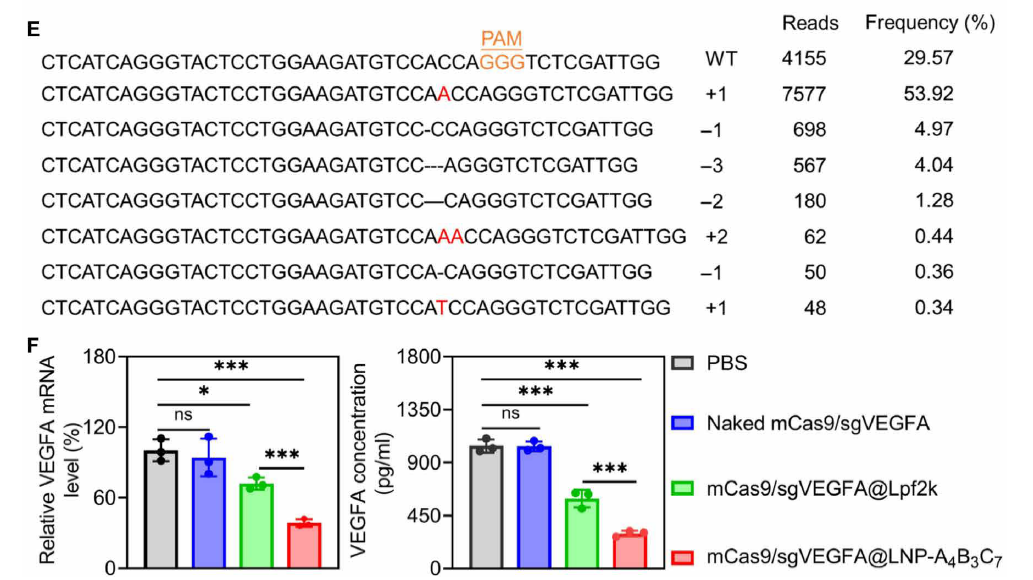
图4:体外VEGFA基因编辑效率及表达水平检测(原文Fig.5)
2. 体内穿透:玻璃体腔注射后,纳米粒可通过 Müller 细胞转胞吞作用到达 RPE 层,48 小时后
仍能检测到 mRNA 信号(Fig.6A、B);
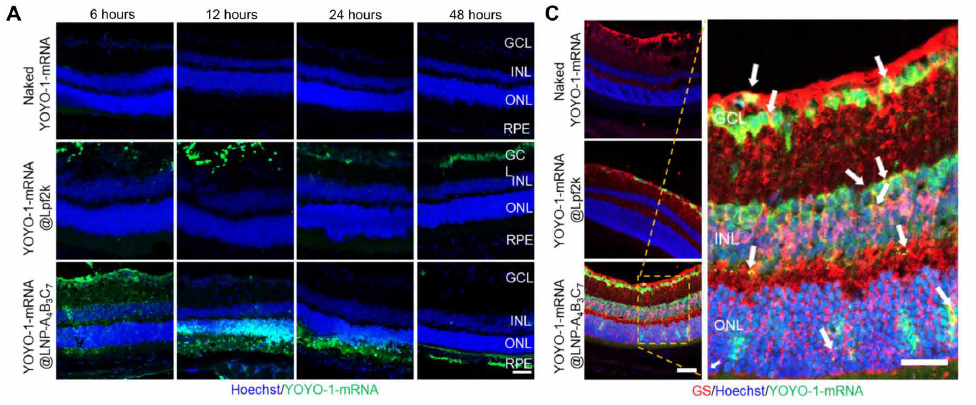
图5:纳米粒体内视网膜穿透及分布(原文Fig.6)
3. 治疗效果:在激光诱导 CNV 小鼠模型中,单次注射后 VEGFA 基因敲除效率达 57%,CNV 面积减少 76%,疗效与临床药物阿柏西普相当(Fig.8);
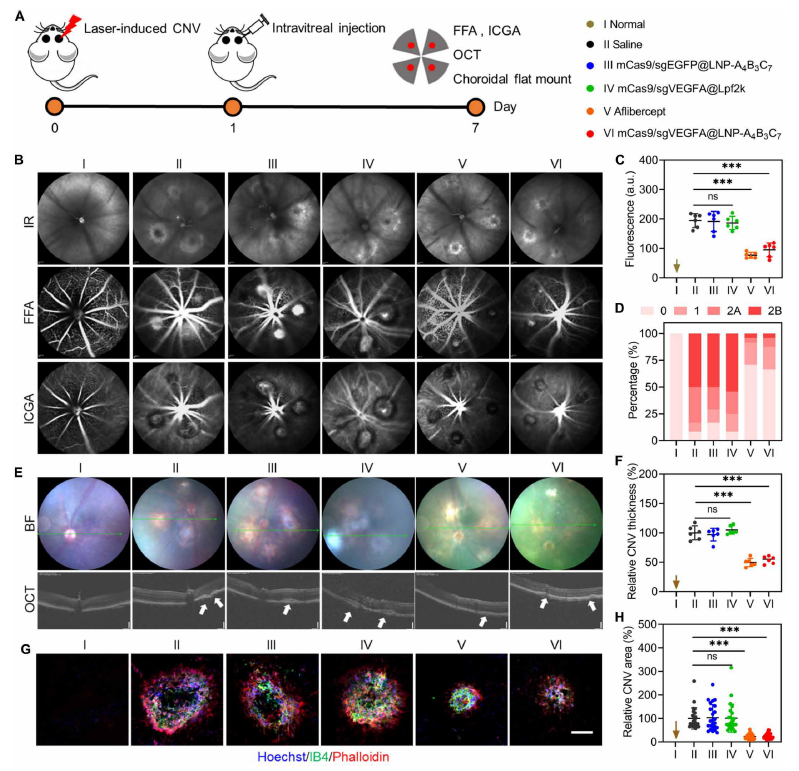
图6:CNV小鼠模型体内治疗效果评估(原文Fig.8)
4. 长效优势:二次激光损伤后,该基因编辑方案仍能有效抑制 CNV,而阿柏西普因代谢快未表现出治疗效果(Fig.9)。
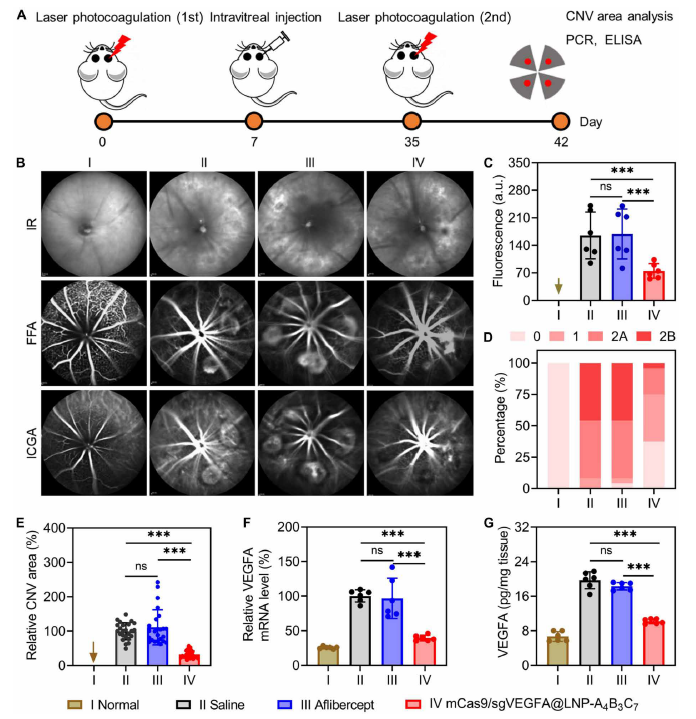
图7:二次激光损伤后的长效治疗效果(原文Fig.9)
(三)生物安全性优异
LNP-A₄B₃C₇未引发明显炎症反应,视网膜组织无病理异常,主要脏器及血液学指标均无毒性表现(fig.S49-S52),解决了传统载体免疫原性和细胞毒性问题。
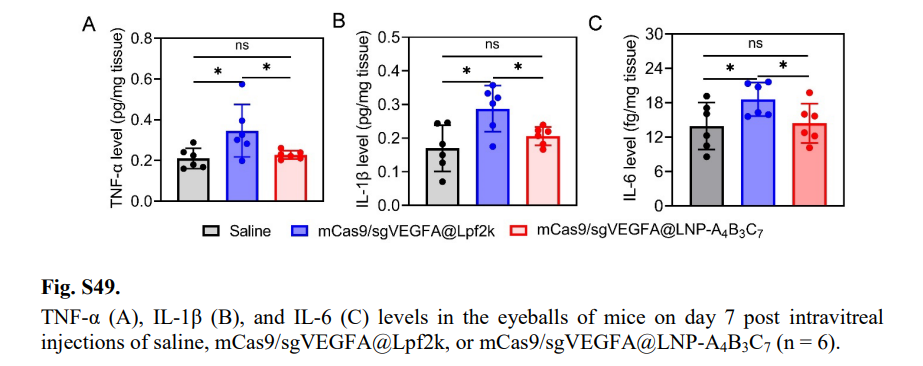
图8:小鼠眼内炎症因子水平检测(原文Fig.S49)
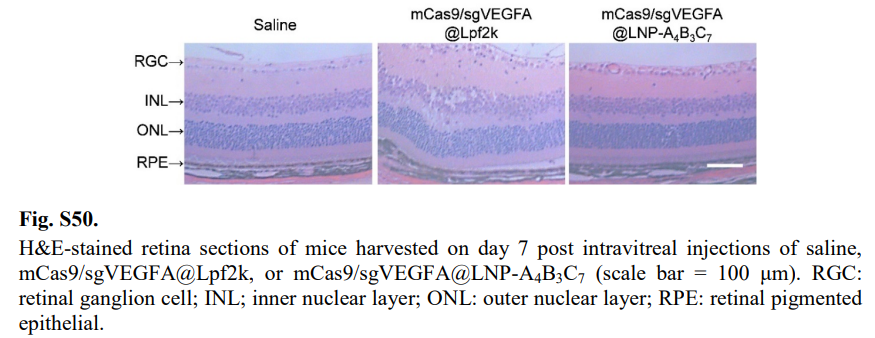
图9:视网膜组织HE染色(原文Fig.S50)
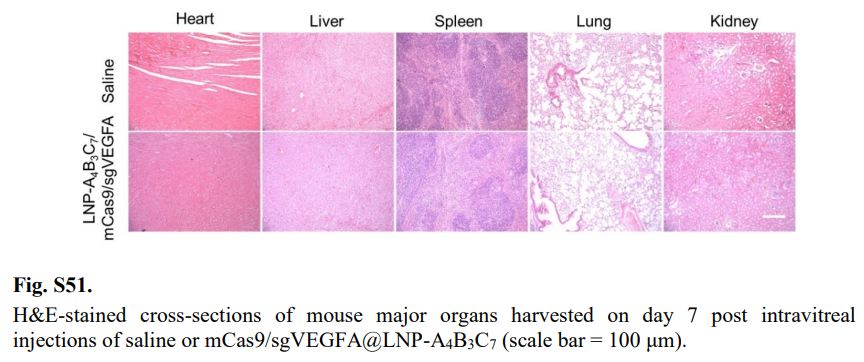
图10:主要脏器HE染色(原文Fig.S51)
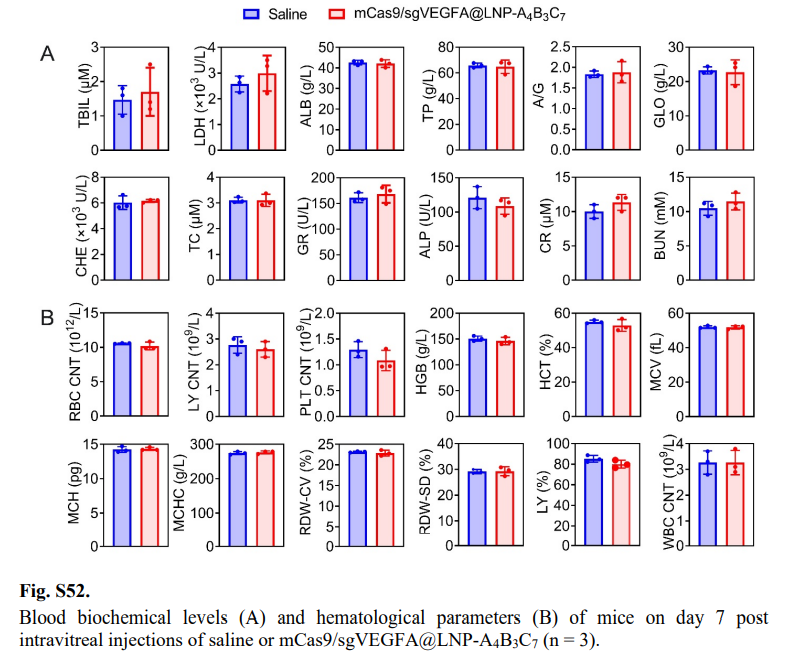
图11:血液生化和血液学指标检测(原文Fig.S52)
三、总结与展望
该研究通过创新的动态共价脂质体递送系统,结合 CRISPR-Cas9 基因编辑技术,成功实现了 CNV 的长效治疗,为 wAMD 等疾病提供了全新治疗策略。
本文内容基于《Science Advances》(DOI: 10.1126/sciadv.adj0006)原文献;文中涉及的原文献图片、数据等知识产权归原期刊及研究团队所有。若存在侵权情形,敬请及时联系我方删除,我方将积极配合处理。
