无细胞蛋白表达系统在TFL制备中的应用
摘要: eProtein Discovery系统完成了困难转录因子TF L的制备、纯化与功能验证,显示出无细胞蛋白表达技术在难表达蛋白研究中的应用潜力。
关键词: 蛋白表达系统、eProtein Discovery、无细胞蛋白表达、无细胞蛋白合成、难表达蛋白快速制备、数字微流控、转录因子制备
一、TFL的无细胞蛋白制备与筛选方案
基于上篇对eProtein Discovery无细胞系统核心技术与工作流程的解析,研究人员针对TF L这类高度无序的难表达转录因子,开展了专项无细胞蛋白表达与纯化研究,并逐步形成了较为完整的难表达蛋白快速获取方案。该方案全程遵循无细胞蛋白合成逻辑,并对实验条件进行了系统优化,以保证结果的可靠性。具体方案如下:
构建体设计与制备:
选取全长TF L、未知功能结构域L2、DNA结合结构域L3三种蛋白变体,通过系统内置的AlphaFold结构预测工具设计L2、L3,将三种变体导入系统云软件优化密码子后,添加3C和TEV序列;利用可溶性标签筛选技术,构建24个含不同可溶性标签的eGene构建体及1个无标签对照构建体,所有构建体C端均整合Strep标签和检测标签,分别用于磁珠纯化和蛋白定量。
无细胞混合体系配置:
选取8种无细胞混合体系,在核心翻译机制基础上,添加金属辅因子、分子伴侣、二硫键促进剂及3C蛋白酶;结合TF L含两个LIM结构域的特点,在体系中加入Zn²⁺,以稳定蛋白锌结合区域,为蛋白正确折叠提供适配环境。
自动化筛选与分析:
将24个eGene构建体、8种无细胞混合体系及纯化磁珠、对照样品、缓冲液等加载至微流控卡盒,系统自动生成并分析192组表达图谱,在24小时内筛选出每种蛋白变体对应的10组高表达组合并完成纯化,确定各变体的放大生产预测得率,为后续放大制备提供数据支撑。
二、TFL制备结果与功能验证
按照上述制备与筛选方案,研究人员依托eProtein Discovery系统,完成了三种TF L变体的制备与纯化。通过对筛选数据、蛋白制备结果及功能验证实验的综合分析,不仅验证了该系统在难表达蛋白制备中的应用效果,也为无细胞蛋白合成技术在转录因子研究中的进一步应用提供了实验依据,具体结果如下:
筛选数据揭示优化方向:
系统筛选的30组高得率表达条件中,所有构建体均含可溶性标签,全长TF L和L2适配P17标签,L3适配CUSF标签。与无标签构建体相比,蛋白表达量有所提升,体现了可溶性标签在蛋白可溶性筛选中的作用;无细胞混合体系中,Zn²⁺有助于稳定蛋白结构,GSSG、PDI⁺/GSSG的氧化环境配置,则可提升不同蛋白变体的表达量,为复杂蛋白无细胞表达条件优化提供了参考。
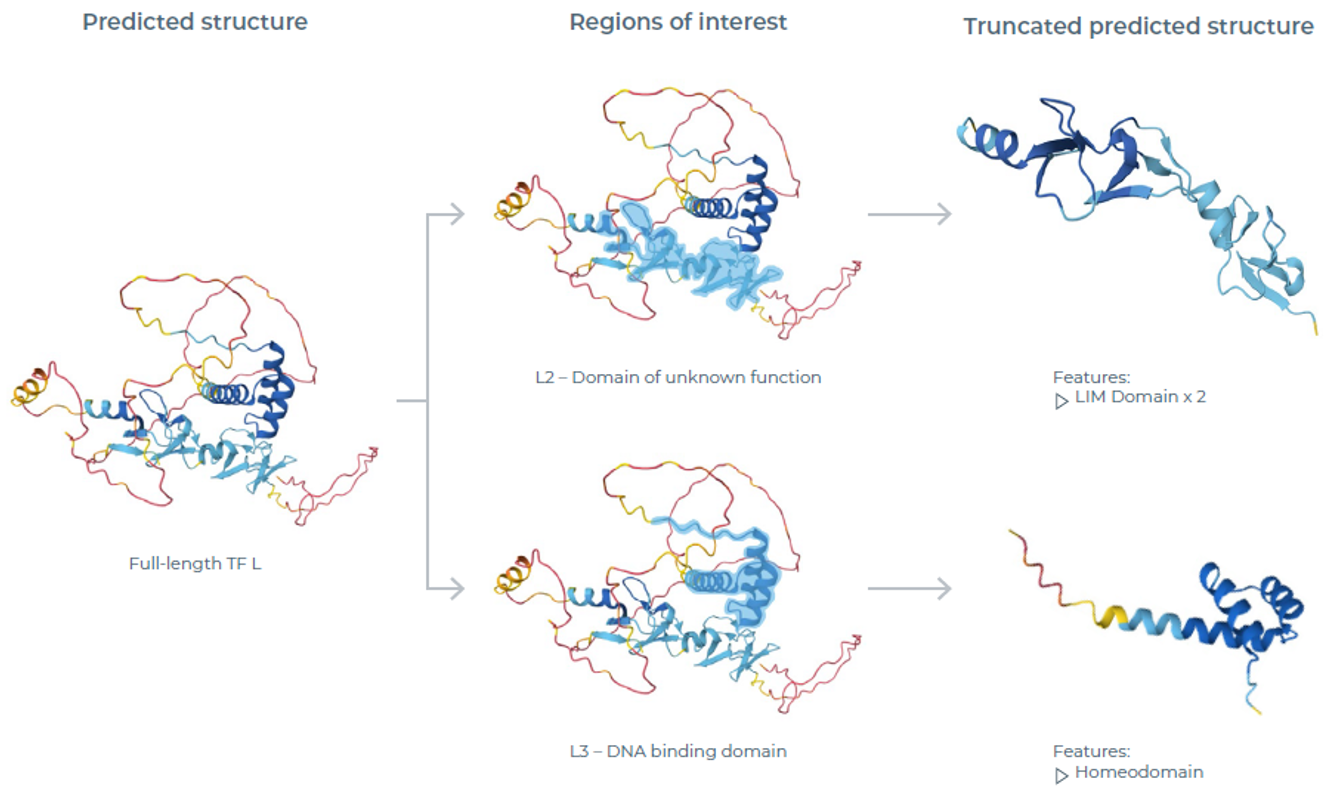
图1:TF L变体的AlphaFold结构预测。图示为全长TF L的预测结构(重点关注区域已高亮标注)。蛋白变体L2和L3基于上述区域筛选设计,同时获得了这些截短蛋白的结构预测结果。
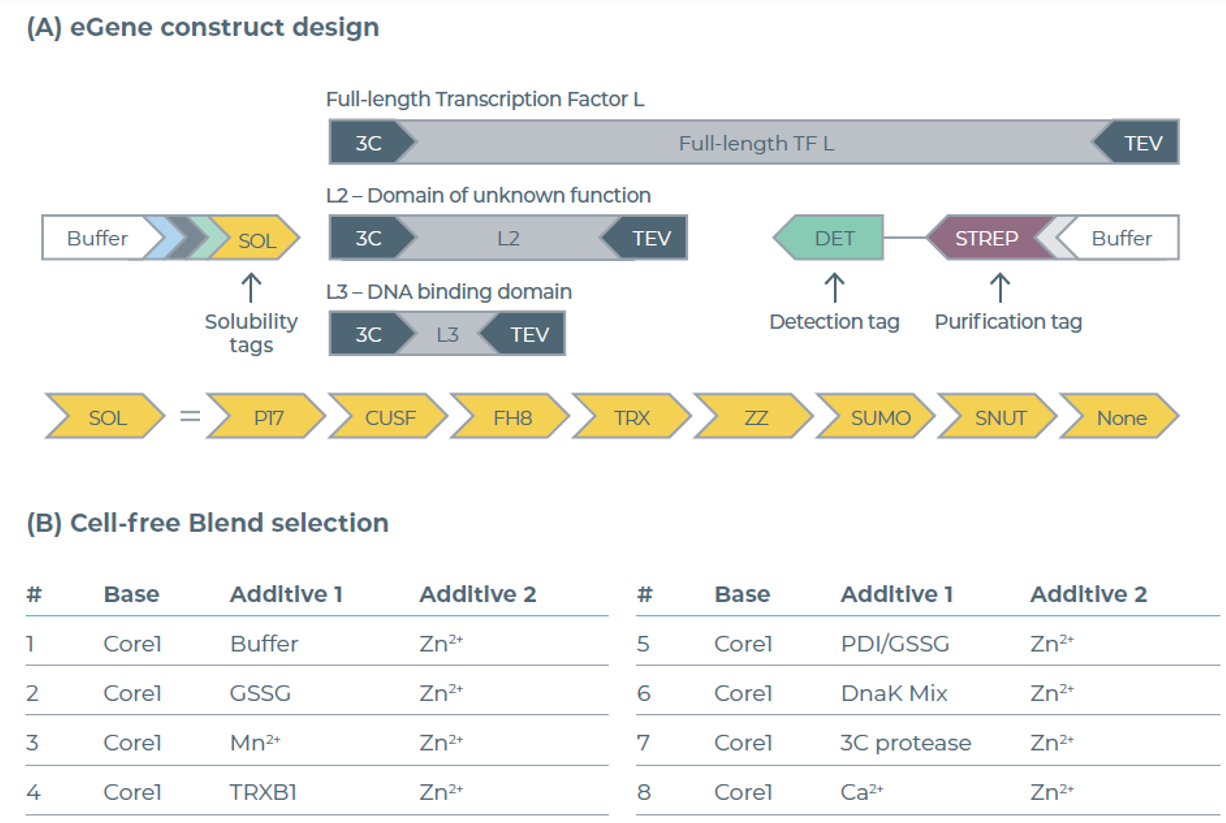
图2:eGene构建体与无细胞混合体系的筛选。(A) 含可溶性标签的TF L eGene构建体设计方案。(B) 用于提高可溶性蛋白得率的无细胞混合体系筛选结果。
TFL变体的AlphaFold结构预测
图1:TF L变体的AlphaFold结构预测。图示为全长TF L的预测结构(重点关注区域已高亮标注)。蛋白变体L2和L3基于上述区域筛选设计,同时获得了这些截短蛋白的结构预测结果。
eGene构建体与无细胞混合体系的筛选
图2:eGene构建体与无细胞混合体系的筛选。(A)含可溶性标签的TF L eGene构建体设计方案。(B)用于提高可溶性蛋白得率的无细胞混合体系筛选结果。
放大制备获得高纯度蛋白:
选取适配表达组合进行过夜放大培养,在1.5mL体系中获得了微克级三种TF L变体蛋白;SDS-PAGE分析显示,纯化后蛋白出现与预期分子量一致的单一条带,Western blot实验验证了蛋白标签的完整性,表明蛋白成功表达与纯化,可满足后续功能实验需求。
功能验证证实蛋白活性:
通过DNA结合电泳迁移率变动分析验证蛋白生物学功能。结果显示,全长TF L可与含结合位点的标记DNA发生浓度依赖性结合,L3结构域可与DNA探针形成特异性复合物,阴性对照无结合现象;L2结构域未表现出DNA结合能力,为其功能研究提供了新的线索,也说明eProtein Discovery系统制备的蛋白保留了相应的生物学功能。
三、无细胞蛋白表达技术的应用价值
结合本次TF L的制备与验证实验,eProtein Discovery系统凭借无细胞蛋白合成的技术特点,为TF L这类高度无序转录因子的制备提供了一条可行路径。研究显示,该系统可在较短时间内完成从DNA到功能性蛋白的全流程制备,在一定程度上突破了传统表达体系在复杂蛋白制备中的限制,为难表达蛋白研究提供了新的技术思路。
除转录因子制备外,该系统还整合了数字微流控、无细胞蛋白表达、荧光蛋白定量检测等技术,可实现表达条件的高通量筛选与系统优化,用于可溶性蛋白的快速制备。相关筛选结果还可与体内表达体系衔接,为后续放大制备提供参考。
在AI蛋白工程、de novo蛋白设计等前沿科研领域,无细胞蛋白表达技术也展现出一定应用潜力。对于人工设计蛋白、新型功能蛋白的制备与验证,这类系统能够为蛋白结构研究、靶向药物研发及再生医学等方向提供支持,并推动无细胞蛋白表达技术在更多科研场景中的应用探索。
围绕eProtein Discovery等系统的科研应用,国内科研人员也正在持续积累更多应用案例与方法学经验。
参考说明
本文基于eProtein Discovery无细胞系统公开资料整理,仅用于科研信息分享,不构成具体实验结论的唯一依据。相关内容供科研交流参考。
