Mol Cancer|复旦大学附属妇产科医院华克勤教授团队找到宫颈癌免疫 “刹车” 关键!CD54⁺iCAFs 介导的新通路成治疗靶点
宫颈癌是全球女性第四大常见恶性肿瘤,晚期或复发性宫颈癌患者预后极差,免疫检查点阻断ICB反应不佳。尽管肿瘤微环境(TME)在促进免疫抑制中的作用已经得到证实,但宫颈癌中基质-免疫细胞间相互作用的精确机制仍不明确。

·研究背景·
宫颈癌(CC)早期患者可通过手术获得良好预后,但晚期、复发或转移性宫颈癌的治疗仍面临巨大挑战。以铂类为基础的化疗联合贝伐珠单抗的疗效有限,而针对PD-1/PD-L1的免疫检查点抑制剂虽已获批临床应用,其客观缓解率仍不理想,提示宫颈癌肿瘤微环境中存在强大的免疫抑制机制,限制了现有免疫疗法的效果。
肿瘤微环境(TME)是导致免疫治疗抵抗的核心原因,主要由肿瘤细胞、基质细胞(如癌症相关成纤维细胞,CAFs)和免疫细胞(如巨噬细胞、T细胞)等成分共同构成,其中癌症相关成纤维细胞(CAFs)和肿瘤相关巨噬细胞(TAMs)是构成免疫抑制微环境的两大关键基质和免疫细胞成分。CAFs具有高度异质性,其中炎症性CAFs(iCAFs)被认为通过分泌细胞因子招募免疫抑制细胞。然而,iCAFs如何与巨噬细胞等免疫细胞进行“对话”,共同构建免疫抑制微环境,在宫颈癌中尚不明确。
·研究结果·
单细胞解析宫颈癌的细胞异质性,发现 CD54⁺炎性癌相关成纤维细胞为肿瘤特异性亚群
为解析宫颈癌微环境的转录组图谱,作者进行了单细胞RNA测序实验,共获得77,221个高质量单细胞转录组(35,220个来自正常组织,42,001个来自肿瘤)。无监督聚类鉴定出8个主要细胞群(图1A):上皮细胞(EPCAM⁺ KRT8⁺)、B细胞(CD19⁺ MS4A1⁺)、T细胞(CD3D⁺ CD3E⁺)、中性粒细胞(CSF3R⁺)、单核吞噬细胞(C1QA⁺ CD14⁺)、肥大细胞(CPA3⁺)、成纤维细胞(DCN⁺ COL1A1⁺)和内皮细胞(PECAM1⁺ vWF⁺)。尽管所有细胞类型在肿瘤和正常组织中均可检测到,但它们的相对丰度存在显著差异,其中成纤维细胞在肿瘤中表现出明显的富集(图1B-C)。进一步对成纤维细胞进行亚群分析,鉴定出5个不同的亚群(图1F):正常成纤维细胞(NFs;DCN⁺ IGFBP6⁺)、祖细胞CAFs(proCAFs;IGF1⁺ OGN⁺)、基质CAFs(matCAFs;CTHRC1⁺ POSTN⁺)、肌成纤维细胞CAFs(myCAFs;RGS5⁺ ACTA2⁺)和炎性CAFs(iCAFs;CD54⁺ CCL2⁺ CXCL12⁺)。尽管所有亚群均表达核心成纤维细胞标志物(COL1A1、COL1A2),但每个亚群都具有独特的转录特征(图1G)。宫颈癌微环境以iCAF、myCAF和proCAF浸润为主,matCAFs相对罕见。
为了描绘CAF的功能异质性,作者对肿瘤和正常组织来源的成纤维细胞进行了比较转录组分析。值得注意的是,一个公认的肿瘤-免疫相互作用介导分子——CD54成为差异最显著的免疫调控基因之一(图1H-I)。在单细胞分辨率下,CD54表达也特异性富集于炎性CAF亚群(称为CD54⁺ iCAFs;图1J),提示该群细胞可能在肿瘤微环境中充当潜在的组织者。拟时序分析显示 proCAFs 可分化为 myCAFs 和 iCAFs,CD54 标记该分化过渡状态, 表明在宫颈癌进展过程中存在动态的成纤维细胞激活。为了阐明沿分化轨迹的功能变化,作者进行了GO分析,结果显示:“成纤维细胞生长因子信号的负调控”和“整合素介导的细胞粘附负调控”等生物学过程逐渐下调,而“泛素连接酶抑制剂活性”、“细胞死亡调控”和“间质迁移”等相关术语在CAFs中上调。总之,该单细胞图谱描绘了宫颈癌中CAF亚群的动态异质性和发育轨迹,并鉴定出CD54⁺ iCAFs在肿瘤进展的关键作用。
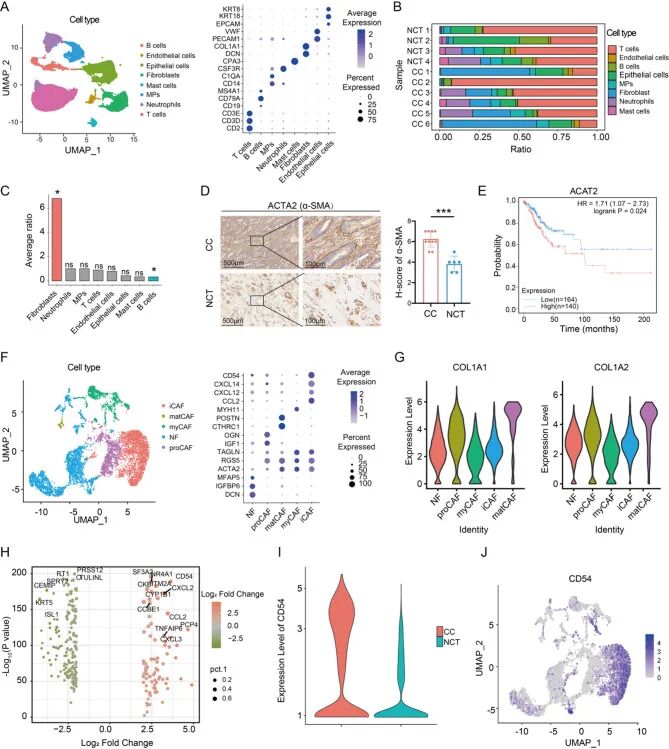
图1 宫颈癌及正常宫颈组织的单细胞测序分析
CD54⁺ iCAF丰度与宫颈癌进展及不良预后呈正相关
在确认CD54⁺ iCAFs是一个免疫抑制性群体后,作者首先通过多免疫组化(mIHC)在宫颈癌组织原位证实了CD54⁺ iCAFs的存在(图2A)。相比正常组织,肿瘤组织中CD54与α-SMA的共定位显著增强。为了在分子水平上定义并分离CD54⁺ iCAF群体以进行功能实验,研究者进行了生化和流式细胞术表征。从人宫颈癌标本及配对癌旁正常组织中分别分离出原代CAFs和NFs。Western blot证实两种细胞均表达经典的成纤维细胞标志物(如α-SMA和波形蛋白),且CAFs中α-SMA和波形蛋白的表达显著增高。此外,CAFs中CD54蛋白水平也显著高于NFs,证实其可作为肿瘤相关成纤维细胞的特异性标志物。
为研究 CD54⁺炎性癌相关成纤维细胞的生物学功能,作者使用靶向 CD54 的 siRNA 在分选的原代 CD54⁺ iCAFs 中进行敲低,同时在 NIH/3T3 成纤维细胞中构建 CD54 过表达模型,以评估 CD54 对肿瘤细胞迁移及体内免疫微环境的影响,结果显示:与对照成纤维细胞相比,CD54⁺炎性癌相关成纤维细胞可显著促进 SiHa 和 HeLa 细胞的迁移能力,且在介导肿瘤细胞迁移中发挥关键作用(图2C-D)。
为评估 CD54⁺炎性癌相关成纤维细胞的临床预后价值,作者利用组织芯片对宫颈癌患者进行分析,结果显示:与正常组织相比,CD54 在肿瘤基质中呈显著高表达(图2E),且与患者总生存期显著缩短相关(图2F)。上述结果表明,CD54⁺炎性癌相关成纤维细胞是与宫颈癌不良预后相关的具有临床意义的成纤维细胞亚群。
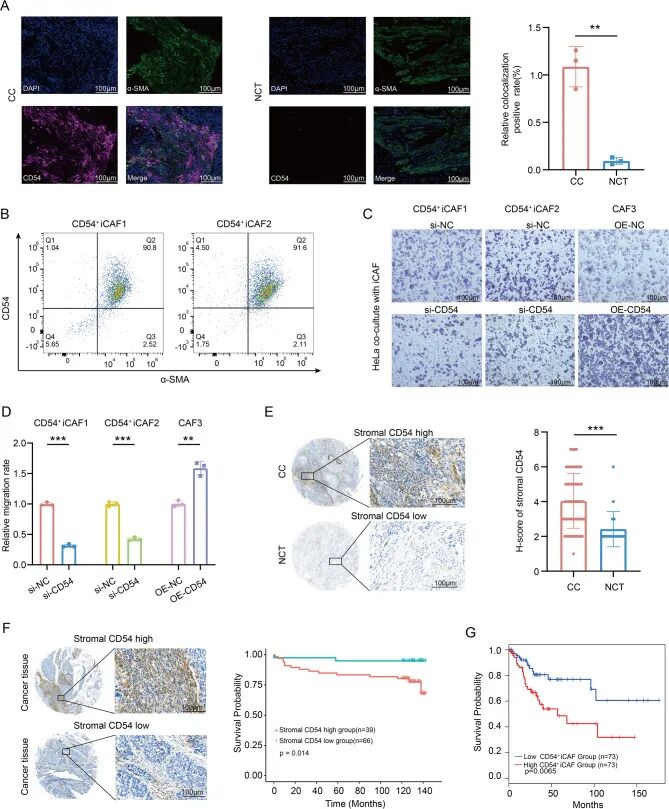
图2 CD54⁺ iCAFs促进宫颈癌迁移,预测预后不良
CD54⁺ iCAFs与巨噬细胞协同浸润构成宫颈癌的免疫抑制微环境
为阐明 CD54⁺炎性癌相关成纤维细胞与肿瘤微环境中免疫细胞的功能相互作用,作者利用 CellChat 软件对 8 个主要细胞群进行配体 - 受体分析,结果显示宫颈癌中成纤维细胞与单核吞噬细胞(MPs)之间存在强烈的细胞间通讯(图3A-B),提示 CD54⁺炎性癌相关成纤维细胞可能通过招募并调控单核吞噬细胞发挥免疫抑制作用。对 CD54⁺炎性癌相关成纤维细胞中差异表达基因的GO分析显示,其显著富集于 “髓系白细胞迁移”“粒细胞趋化” 等相关条目,进一步证实该细胞亚群参与免疫细胞的趋化过程。
接下来作者对MP的异质性进行解析,鉴定出 3 个转录水平不同的亚群(图3C-D):免疫调节性树突状细胞(BIRC3⁺HLA-DQB1⁺)、巨噬细胞(CD68⁺CD163⁺ITGAL⁺)和炎性单核细胞(FCN1⁺APOBEC3A⁺)。配体 - 受体网络分析显示,CD54⁺炎性癌相关成纤维细胞与 ITGAL⁺巨噬细胞之间存在极强的相互作用(图3E),其中 CD54-ITGAL 信号对为最主要的信号轴(图3F)。多重免疫组化实验验证了 ITGAL⁺巨噬细胞的免疫抑制表型,且证实其与 CD54⁺炎性癌相关成纤维细胞在肿瘤 - 基质界面呈空间共定位(图3G-H)。GEPIA2 数据库分析进一步证实:宫颈癌患者中 CD54⁺炎性癌相关成纤维细胞与 ITGAL⁺巨噬细胞的表达呈显著正相关,强化了该细胞间相互作用的临床相关性。
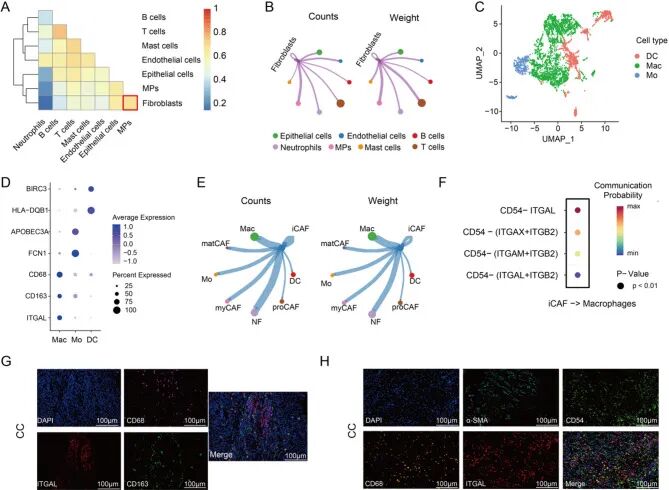
图3成纤维细胞与单核吞噬细胞的相互作用
空间转录组证实在肿瘤-基质界面存在CD54⁺ iCAF-ITGAL⁺巨噬细胞免疫抑制生态位
为了阐明 CD54⁺iCAF与 ITGAL⁺巨噬细胞相互作用的空间结构特征,作者对6例CC样本进行了空间转录组学分析,结果显示:CD54⁺炎性癌相关成纤维细胞与 ITGAL⁺巨噬细胞在肿瘤 - 基质边界呈显著共定位(图4A)。对两种细胞共定位位点进行功能注释,发现其显著富集于免疫调控相关过程,包括 “白细胞活化负调控”“髓系细胞活性调节” 和 “细胞间黏附动态调控” 等(图4D)。KEGG分析进一步显示,这些位点在 “细胞因子 - 细胞因子受体相互作用”“代谢重编程” 和 “趋化因子信号通路” 等通路中呈协同激活状态(图4F)。这些结果证实,CD54⁺ iCAF-ITGAL⁺巨噬细胞单元作为CC中一个结构化的免疫抑制生态位,通过细胞募集、代谢调节和微环境重塑来促进免疫逃逸。
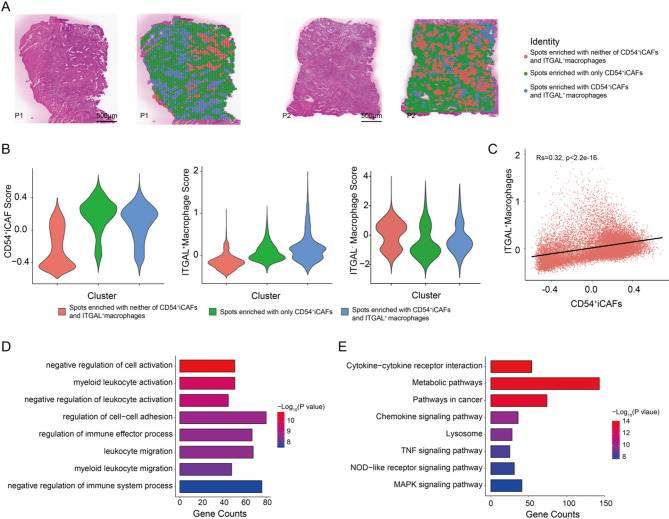
图4 空间转录组学揭示CD54+ iCAF和ITGAL+巨噬细胞的共定位
CD54⁺ iCAFs通过CCL2介导的单核细胞募集来调控ITGAL⁺巨噬细胞的极化
为了研究CD54⁺ iCAFs在驱动巨噬细胞向M2样表型极化中的作用,作者建立了CD54⁺ iCAFs与THP-1单核细胞的共培养系统。功能分析表明:与NFs相比,CD54⁺ iCAFs显著增强了单核细胞的迁移(图5A),并促进了它们向M2样TAMs的分化,表现为典型M2标志物(包括CD163、PDGFB和MRC1)表达增加(图5B)。与这种极化表型一致,与CD54⁺ iCAFs共培养的THP-1细胞表现出M2相关效应细胞因子(包括CCL17、IL-10、MMP9、TGFB和VEGFA)的mRNA水平显著升高(图5C)。
接下来作者探讨了CD54⁺ iCAFs如何招募单核细胞并促进其极化为M2样巨噬细胞。通过对si-CD54或si-NC的CD54⁺ iCAFs进行RNA测序,结果显示:CCL2是CD54敲减后下调最显著的前五个基因之一(图5D),WB也证实了这一结果(图5E)。此外,功能验证也证实CD54⁺ iCAFs分泌的CCL2蛋白显著高于NFs(图5F)。因此,为了确定CCL2本身是否足以诱导单核细胞迁移,作者用重组CCL2处理单核细胞,结果显示:该处理可完全模拟 CD54⁺iCAF条件培养基对单核细胞的趋化效应(图5G)。这些结果表明:CD54⁺ iCAFs通过CCL2招募单核细胞并将其极化为具有M2样特征的ITGAL⁺巨噬细胞进而介导肿瘤免疫抑制,提示需进一步探究其更广泛的免疫调控作用。
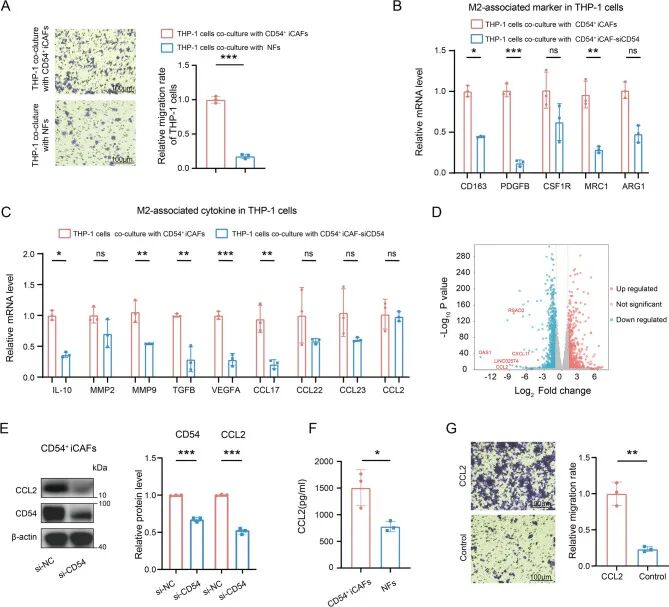
图5 CD54⁺ iCAFs通过CCL2分泌促进单核细胞迁移和M2样极化
CD54⁺ iCAFs通过促进TME中ITGAL⁺巨噬细胞来源的CXCL8来介导免疫抑制
通过对与CD54⁺ iCAFs共培养的THP-1来源巨噬细胞(有或无ITGAL敲减)进行转录组分析,作者鉴定出CXCL8是ITGAL⁺巨噬细胞中上调最显著的细胞因子(图6A)。GO分析表明,上调的DEGs与生物过程中的细胞因子介导的信号传导和免疫系统抑制、细胞组分中的富含胶原的ECM以及分子功能中的细胞因子/受体-配体功能相关。KEGG通路分析确定细胞因子-细胞因子受体相互作用和ECM-受体结合为显著通路。基因集富集分析(GSEA)进一步证实了免疫系统通路激活的富集,提示CD54⁺ iCAFs可能通过细胞因子信号传导和ECM重塑来编程ITGAL⁺巨噬细胞,驱动CXCL8依赖的免疫抑制。
由于CXCL8是与CD54⁺ iCAFs共培养的THP-1来源巨噬细胞中上调最显著的细胞因子编码基因,作者检测了临床标本中其与CD54⁺ iCAFs丰度的相关性。对CC组织的流式细胞术分析显示:CD54⁺ iCAFs高浸润的样本一致地表现出CXCL8表达增加(图6B),提示CD54⁺ iCAF-ITGAL⁺巨噬细胞-CXCL8轴在塑造免疫抑制性TME中的病理生理学意义。
为了确定TME内CXCL8的主要细胞来源,作者分析了scRNA-seq数据,显示CXCL8表达主要富集在ITGAL⁺巨噬细胞中,并且流式细胞术和mIHC在临床样本中验证了这一发现,并在空间上定位其表达。两种方法均证实ITGAL⁺巨噬细胞是CXCL8蛋白的主要来源(图6C-D),强化了ITGAL⁺巨噬细胞作为免疫抑制网络中关键分泌组分的角色。鉴于CXCL8有助于免疫抑制并导致CC患者预后不良,据此推测 CD54⁺ iCAFs通过促进ITGAL⁺巨噬细胞分泌CXCL8来诱导免疫抑制微环境。
在评估CD54⁺ iCAFs的体内作用之前,作者构建了过表达CD54的NIH/3T3成纤维细胞(OE-CD54)。使用该模型将TC-1小鼠细胞与OE-CD54或对照成纤维细胞共注射到小鼠体内,以评估它们对肿瘤生长和免疫微环境的影响。与对照组相比,共注射OE-CD54成纤维细胞的肿瘤表现出显著加速的生长(图6F-G)。对肿瘤浸润免疫细胞的流式细胞术分析显示:OE-CD54组中CD206⁺ M2样巨噬细胞显著增加(图6H-I),支持CD54⁺ iCAFs在促进巨噬细胞向免疫抑制表型极化中的作用。由于CXCL8在小鼠中不存在,作者测量了巨噬细胞炎症蛋白-2(MIP-2),即人CXCL8的功能性鼠同源物。ELISA证实OE-CD54组肿瘤中MIP-2水平显著升高(图6J)。总之,这些体内结果表明,CD54⁺ iCAFs不仅加速肿瘤进展,而且通过极化ITGAL⁺ M2样巨噬细胞和刺激CXCL8/MIP-2分泌来重塑免疫微环境,揭示了CC发展中基质-免疫相互作用的关键机制。
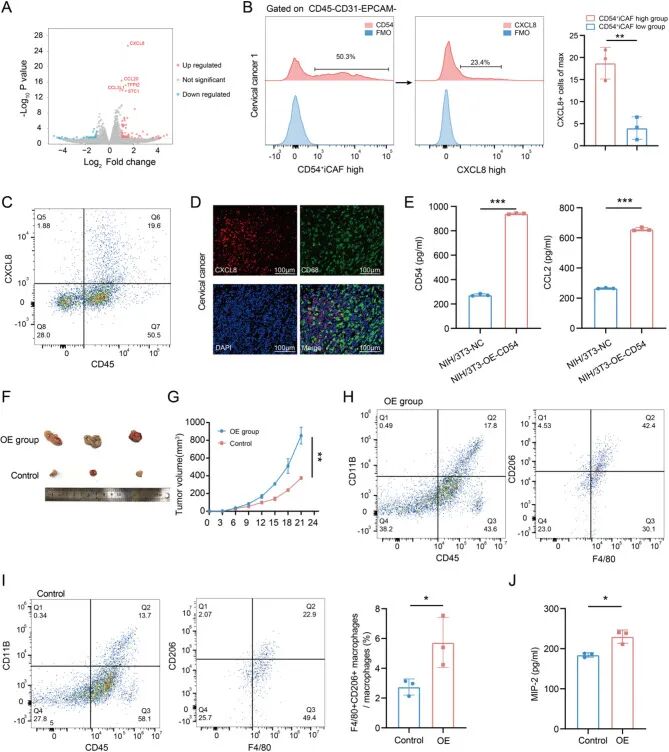
图6 CD54 ⁺ iCAF驱动的巨噬细胞重编程在体内促进CXCL8表达和肿瘤进展
CD54⁺iCAF通过双重机制诱导巨噬细胞来源的CXCL8/PD-L1轴激活,进而抑制 CD8⁺T 细胞功能
在确定CD54⁺ iCAFs增强了ITGAL⁺巨噬细胞分泌CXCL8基础上,作者进一步探究了该细胞因子如何促进CC TME中的免疫重塑。CIBERSORT分析显示:CXCL8水平与CD8⁺ T细胞浸润之间存在显著的负相关(P<0.001),提示CD54⁺ iCAFs驯化的巨噬细胞可能通过排除细胞毒性淋巴细胞来促进免疫抑制生态位(图7A)。对GEPIA2中CSEC队列分析进一步证实了这种负相关关系,显示CXCL8高表达的肿瘤含有显著更少的细胞毒性CD8⁺ T细胞。与转录组分析结果一致,免疫组化实验证实:在本研究的患者样本中 CXCL8 与 CD8 的蛋白表达呈负相关(图7B-C)。
鉴于先前有报道称CXCL8可诱导PD-L1表达以减弱细胞毒性T细胞功能,假设CXCL8也可能通过该调节轴在CC中驱动免疫逃逸。CSEC队列分析显示CXCL8高表达的巨噬细胞与PD-L1表达呈正相关,这一发现在临床标本中通过流式细胞术进一步验证(图7D)。为了确定TME中PD-L1的主要细胞来源,作者对CC组织进行了IHC和流式细胞术,IHC显示:CD68⁺巨噬细胞与PD-L1蛋白表达呈正相关(图7E),流式细胞术证实巨噬细胞是主要的PD-L1⁺免疫群体(图7F)。重要的是,与低CXCL8对照组相比,高CXCL8肿瘤表现出PD-L1⁺巨噬细胞浸润显著增加(图7G)。
为阐明 CD54⁺iCAF诱导巨噬细胞分泌 CXCL8 并上调 PD-L1 的分子机制,作者探究了巨噬细胞的重编程是否依赖细胞间的直接接触或可溶性因子,对比直接共培养(允许细胞间完全物理接触)和跨膜共培养(仅允许可溶性因子交换)两种体系,发现巨噬细胞中 CXCL8 和 PD-L1 的高效诱导需要细胞间的直接接触,且可溶性因子单独作用也可诱导二者呈部分但显著的上调(图7H)。基于该接触依赖的效应,进一步验证 CD54-ITGAL 的结合是否为该相互作用的特异性介导机制,结果显示:用中和抗体阻断炎性癌相关成纤维细胞表面的 CD54 或巨噬细胞表面的 ITGAL,均可显著抑制 CXCL8 和 PD-L1 的上调。
此外,在无炎性癌相关成纤维细胞共培养的情况下,单独敲低巨噬细胞中的 ITGAL 对其 PD-L1 表达无影响(图7J),表明 ITGAL 的功能发挥需要其配体的结合。鉴于可溶性因子也参与巨噬细胞的调控,且 CD54 敲低后 CCL2 的表达显著下调,在transwell体系中通过中和抗体阻断 CCL2 的作用,结果显示:CCL2 的阻断可部分但显著抑制 CXCL8 和 PD-L1 的诱导。综上,本研究结果表明CD54⁺iCAF通过两条不同的通路介导肿瘤免疫抑制:依赖细胞间接触的 CD54-ITGAL 信号通路和依赖可溶性因子 CCL2 的巨噬细胞重编程通路。上述过程可触发巨噬细胞自分泌 CXCL8,进而上调 PD-L1 的表达,最终导致 CD8⁺T 细胞的功能受抑,促进宫颈癌免疫耐受微环境的形成。
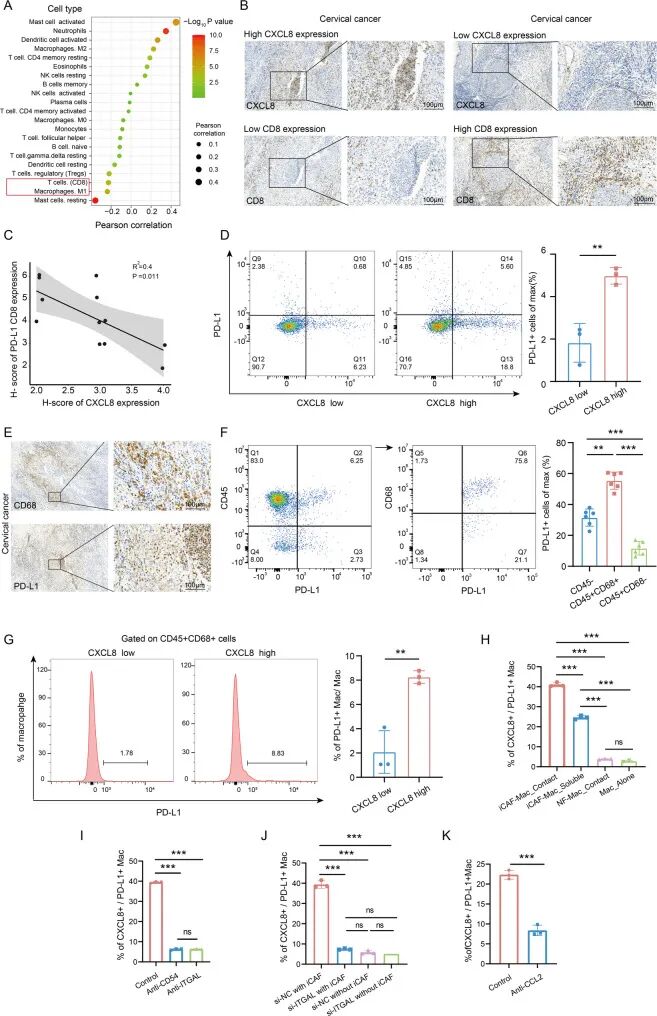
图7 CXCL8与CD8 + T细胞排斥相关,通过细胞接触和可溶性因子依赖机制促进巨噬细胞上PD-L1的表达
靶向 CXCL8/PD-L1 轴的治疗可恢复CC的抗肿瘤免疫功能
为从机制上验证 CXCL8 在 PD-L1 诱导中的作用,作者采用 CXCL8 信号通路抑制剂Reparixin处理宫颈癌原代细胞悬液,该抑制剂可阻断 CXCR1/CXCR2 结合后的胞内信号转导。结果显示:Reparixin处理可显著降低 PD-L1⁺细胞和 PD-L1⁺巨噬细胞的数量(图8A),证实 CXCL8 是调控巨噬细胞 PD-L1 表达的关键分子。重要的是,Reparixin处理还可改善抗肿瘤免疫功能,表现为肿瘤浸润 CD8⁺T 细胞中 GZMB⁺细胞的比例升高,效应细胞因子(IFN-γ、TNF-α)的分泌增加,且细胞溶解标志物(CD107a)的释放增强。
作者进一步在免疫健全的 C57BL/6 小鼠荷 TC-1 肿瘤模型中评估Reparixin的治疗潜力,该模型中肿瘤细胞与 CD54 过表达的 NIH/3T3 成纤维细胞共接种(初始肿瘤体积约 50mm³)。尽管小鼠中无 CXCL8 的同源基因,但人 CXCL8 可通过小鼠的 CXCR1/CXCR2 发挥信号传导作用。结果显示:Reparixin单药和 PD-L1 抑制剂单药均能显著抑制肿瘤生长,且两种单药治疗的效果无统计学差异(图8E);更值得关注的是,与任一单药治疗相比,联合治疗对肿瘤的控制效果显著更优。流式细胞术分析证实:联合治疗可进一步提高肿瘤浸润 CD8⁺T 细胞中细胞溶解蛋白(GZMB)的表达和效应细胞因子(IFN-γ、TNF-α)的分泌(图8F-G)。
综上,本研究构建的机制模型表明:CD54⁺iCAF通过分泌 CCL2 将 ITGAL⁺巨噬细胞极化为 M2 样表型,同时促进该巨噬细胞中 CXCL8 的表达,进而通过自分泌方式上调 PD-L1;Reparixin可阻断 CXCL8-PD-L1 轴,恢复 CD8⁺T 细胞的功能,并与 PD-L1 抑制剂产生协同作用。该结果提示,靶向基质 - 免疫细胞相互作用的联合治疗策略在宫颈癌中具有潜在的治疗价值(图9)。
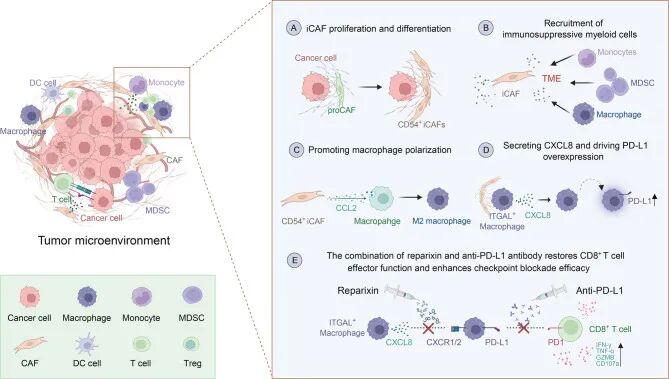
图9 模式图
·全文总结·
本研究通过单细胞与空间多组学技术,在宫颈癌中发现一类高表达CD54的炎性癌症相关成纤维细胞(CD54⁺ iCAFs)。该细胞亚群丰度与患者不良预后正相关,并能与ITGAL⁺巨噬细胞在空间上形成免疫抑制微环境。机制上,CD54⁺ iCAFs通过分泌CCL2及直接的CD54-ITGAL接触依赖信号,将巨噬细胞极化为M2样表型;后者进一步通过自分泌CXCL8上调自身PD-L1表达,从而有效抑制CD8⁺ T细胞的浸润与杀伤功能,构成“成纤维细胞-巨噬细胞-T细胞”三级联免疫逃逸轴。治疗层面,使用CXCR1/2抑制剂Reparixin可破坏该信号轴,减少PD-L1⁺巨噬细胞积累,恢复CD8⁺ T细胞功能,并与抗PD-L1抗体产生协同抗肿瘤效应。综上,本研究不仅从机制上阐明了宫颈癌中“CAF-巨噬细胞-PD-L1”这一新型免疫逃逸通路,更为重要的是,提出了针对基质-免疫交互的联合治疗策略,即CXCR1/2抑制剂联合免疫检查点阻断剂,为克服宫颈癌免疫治疗抵抗提供了坚实的理论依据和临床前证据。
原文链接:https://pubmed.ncbi.nlm.nih.gov/41121145/
和元服务
和元一直致力为肿瘤研究提供整体解决方案,从基因筛选、基因功能研究到机制研究,提供质粒构建、病毒包装、基因过表达、基因干扰、基因敲除稳转株构建、细胞功能学实验、双荧光素酶检测服务到动物模型构建一站式技术服务!

更多活动详情可长按或扫描上方二维码,填写表单,我们将尽快安排专人与您联系!
精彩合集

病毒载体在神经领域中的应用
病毒载体在代谢领域中的应用
肿瘤载体在肿瘤研究中的应用
AAV靶向看这个就GO了
慢病毒系列
多组学、单细胞及空间转录组
外泌体知识宝典
生信云平台
和元生物
和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。

