Gut Microbes 杨洪军/刘玥合作揭示源于舌苔的具核梭杆菌介导口-肠菌轴加重心肌缺血再灌注损伤的新机制

心肌缺血再灌注损伤(MIRI)是冠心病再灌注治疗中亟待解决的关键临床难题。尽管及时血运重建可显著改善急性心肌缺血患者预后,但患者再灌注后心肌损伤程度存在显著个体差异,这一异质性与宿主代谢状态及微生物组密切相关。近年来,口腔菌群紊乱与心血管健康的关联备受关注,但其调控MIRI的具体分子机制仍缺乏系统性实证依据。
2026年4月25日,中国中医科学院杨洪军研究员团队与国家中医心血管病临床医学研究中心刘玥主任医师团队合作,在肠道菌群领域国际知名期刊Gut Microbes发表题为“An oral-gut microbial metabolite links Fusobacterium nucleatum to aggravated myocardial ischemia-reperfusion injury”的研究论文。该研究以口腔关键条件致病菌具核梭杆菌(Fusobacterium nucleatum, F. nucleatum)为核心,首次提出并完整验证了“口腔致病菌—肠道菌群代谢重塑—循环代谢物—心肌损伤”的口-肠菌轴全新机制,串联起口腔微生态、肠道代谢与心脏信号通路,为口腔菌群紊乱参与心血管疾病提供了跨部位、跨系统的实证支撑。

研究团队前期立足中医“心开窍于舌”等理论认识,持续关注中医舌诊背后的微生物学实质,围绕口腔菌群紊乱及其参与的代谢性心血管疾病机制开展了系列研究。团队此前已在糖尿病冠心病人群中发现并验证了源于舌苔的口腔菌群与肠道菌群之间的关联和互作特征,提示口腔菌群紊乱可能通过口-肠菌轴参与宿主代谢异常与心肌损伤(Cardiovascular Diabetelogy, 2024)。在此基础上,本研究进一步探索舌诊的微生物学机制,围绕F. nucleatum展开研究,首次提出并验证了其介导的口-肠菌轴新机制:口腔F. nucleatum并非主要依赖持续肠道定植或简单的屏障破坏致病,而是通过重塑肠道菌群代谢功能,促进关键代谢物咪唑丙酸(imidazole propionate, ImP)升高,进而加重心肌缺血再灌注损伤(myocardial ischemia–reperfusion injury, MIRI)。该研究串联了口腔微生态、肠道代谢与心肌损伤信号通路,建立了一条跨部位菌群互作的机制链条。
研究团队首先在动物实验中发现,经F. nucleatum 灌胃后,小鼠MIRI明显加重,表现为心功能进一步下降、心肌细胞凋亡增加以及循环心肌损伤和炎症指标升高。进一步PCR分析显示,F. nucleatum 灌胃后小鼠肠道中乳杆菌等菌群丰度增加,而等量大肠杆菌灌胃未出现相应的菌群改变和促损伤效应。值得注意的是,这种致病效应并不依赖于F. nucleatum 在肠道内的持续定植,也未伴随明显的口腔或肠道黏膜屏障破坏,提示其更可能通过跨部位重塑肠道菌群组成及代谢功能而促进MIRI (图1)。
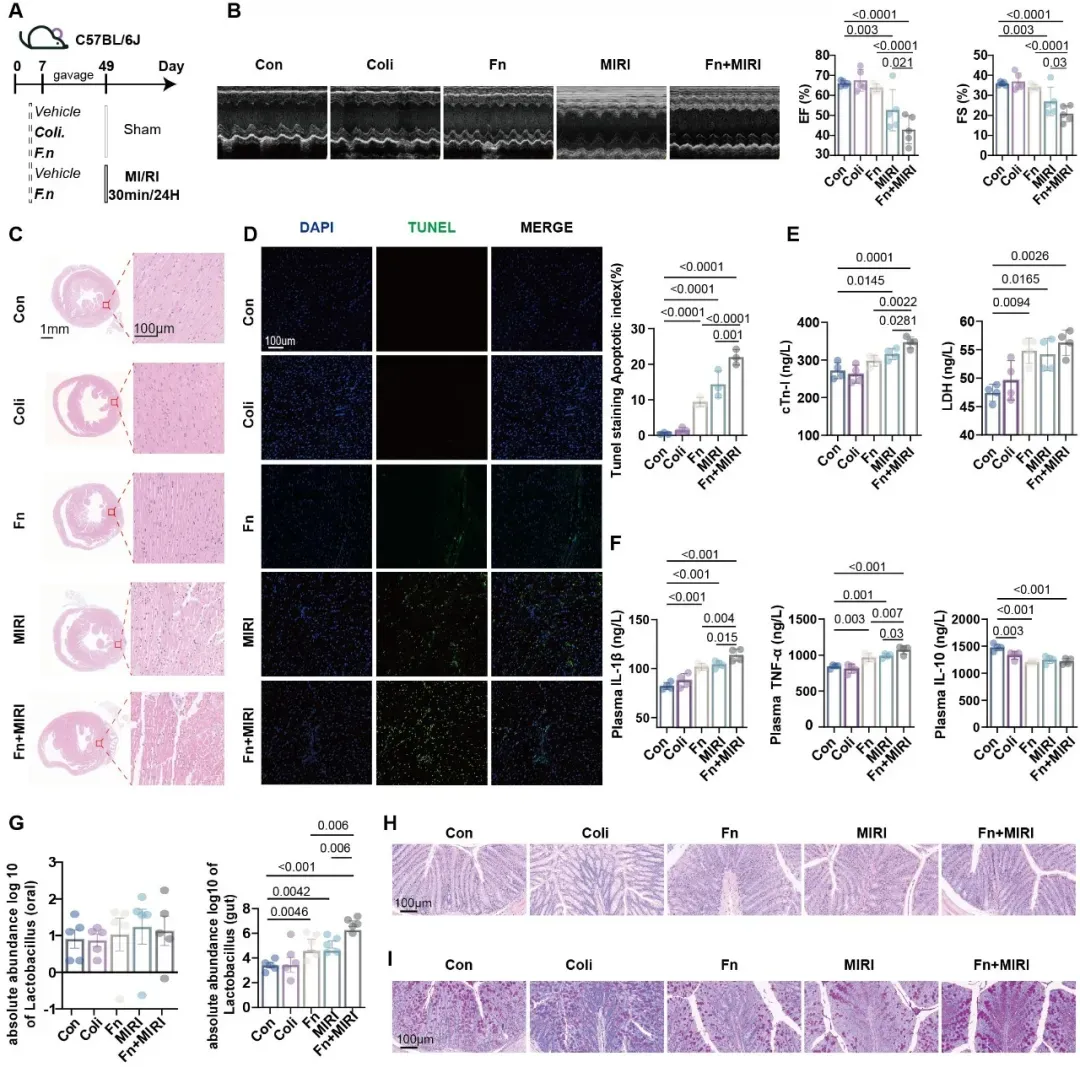
图1. 具核梭杆菌灌胃加重MIRI并影响肠道菌群(乳杆菌为代表)丰度
研究进一步分析了F. nucleatum灌胃后小鼠的肠道及循环代谢变化,结果显示,F. nucleatum干预后小鼠结肠内组氨酸代谢显著变化,其中组氨酸的代谢物尿刊酸(urocanate)显著升高;血浆中的尿刊酸代谢终产物咪唑丙酸(ImP)也显著升高。临床队列分析进一步证实,冠心病患者血浆ImP 水平升高。ImP的生成主要来源于肠道菌群中具有尿刊酸还原酶(urocanate reductase, UAR)的部分菌种,而非直接来源于F. nucleatum。这提示,口腔F. nucleatum通过重塑肠道菌群的组氨酸代谢功能,促进ImP 生成(图2)。
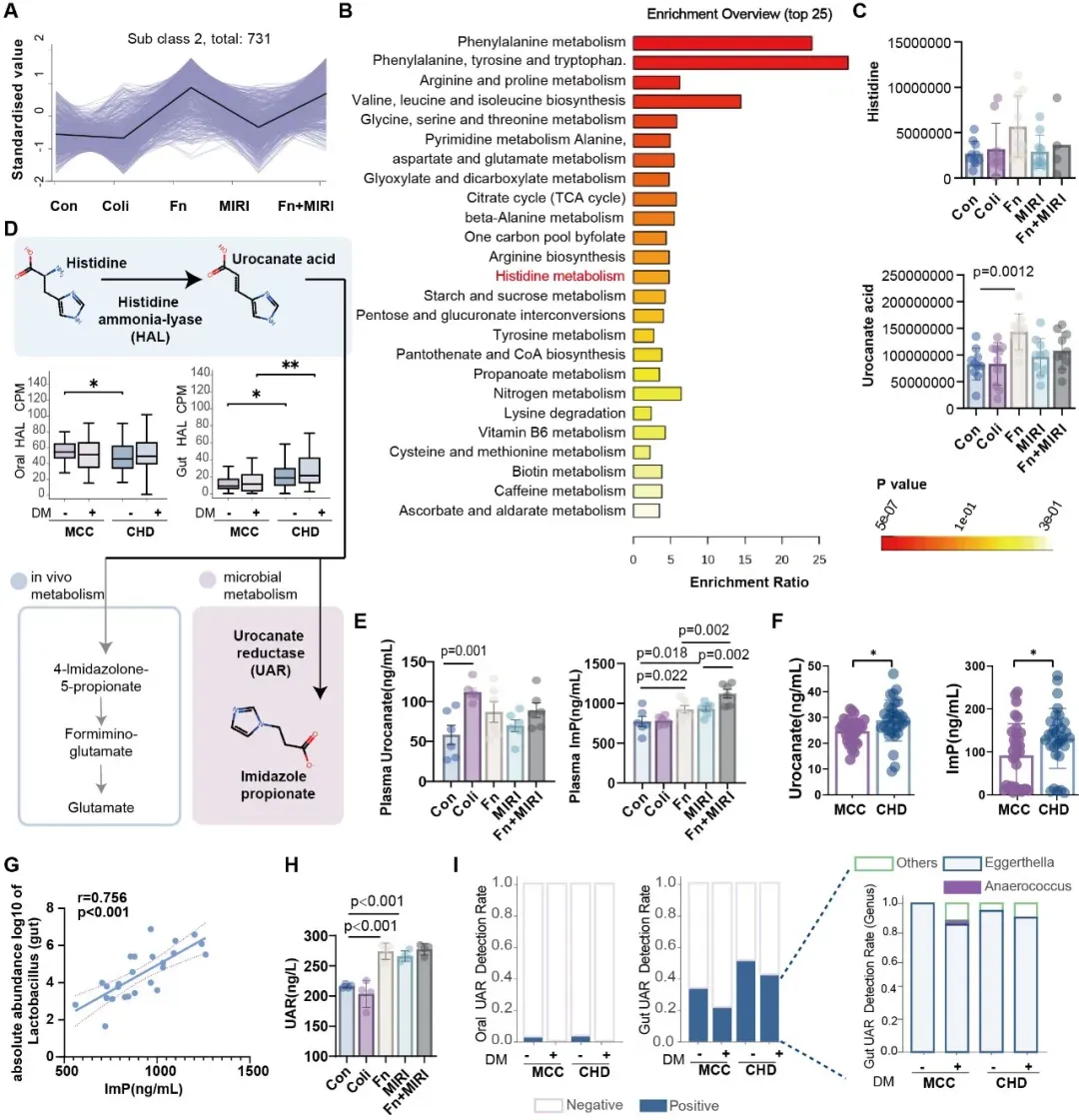
图2. 具核梭杆菌重塑肠道组氨酸代谢并促进ImP生成
为了验证这一口-肠菌轴相关的ImP代谢来源,研究构建了伪无菌模型。使用广谱抗生素(ABX)耗竭肠道菌群后,小鼠血浆ImP水平显著下降,同时伴随小鼠MIRI程度减轻。超微结构观察进一步发现,经ABX干预的小鼠心肌线粒体肿胀减轻、可见更多的自噬相关囊泡样结构,提示心肌自噬相关超微结构特征改善。同时,抗生素处理还可降低心肌组织层面的p62免疫荧光信号(图3)。
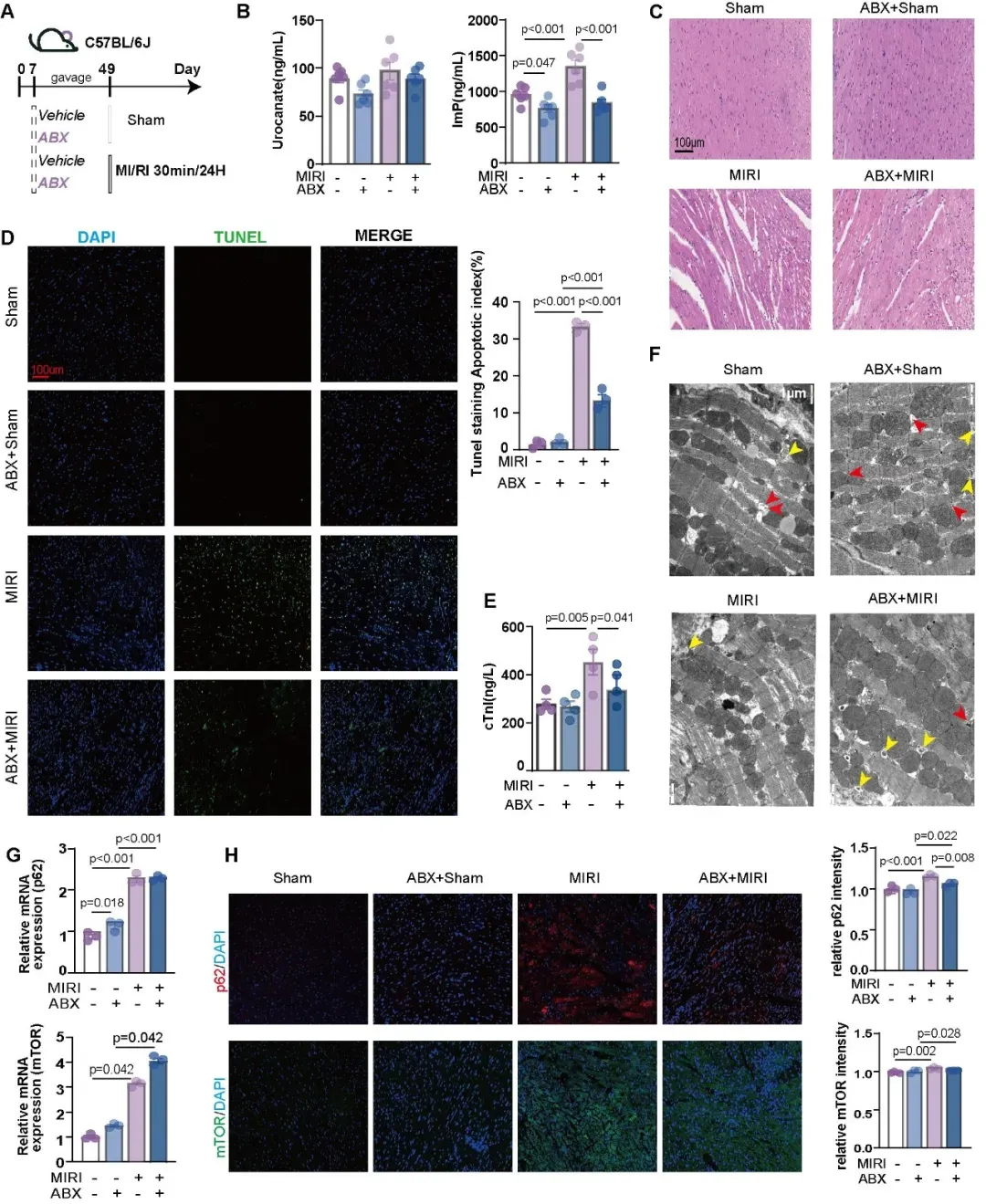
图3. 伪无菌模型下血浆ImP水平降低并伴随MIRI减轻
在此基础上,研究团队进一步验证:ImP本身是否损伤心肌细胞。在H9c2缺氧/复氧(H/R)模型中,ImP呈剂量依赖性降低细胞活力。ImP使Beclin1、LC3B-II和ATG5等自噬相关蛋白下降,并伴随电镜下自噬相关囊泡结构改变。更重要的是,ImP显著上调p62和mTOR的mRNA及蛋白表达,并增加下游S6K1丰度;与此同时,IRS1蛋白表达下降(图4)。
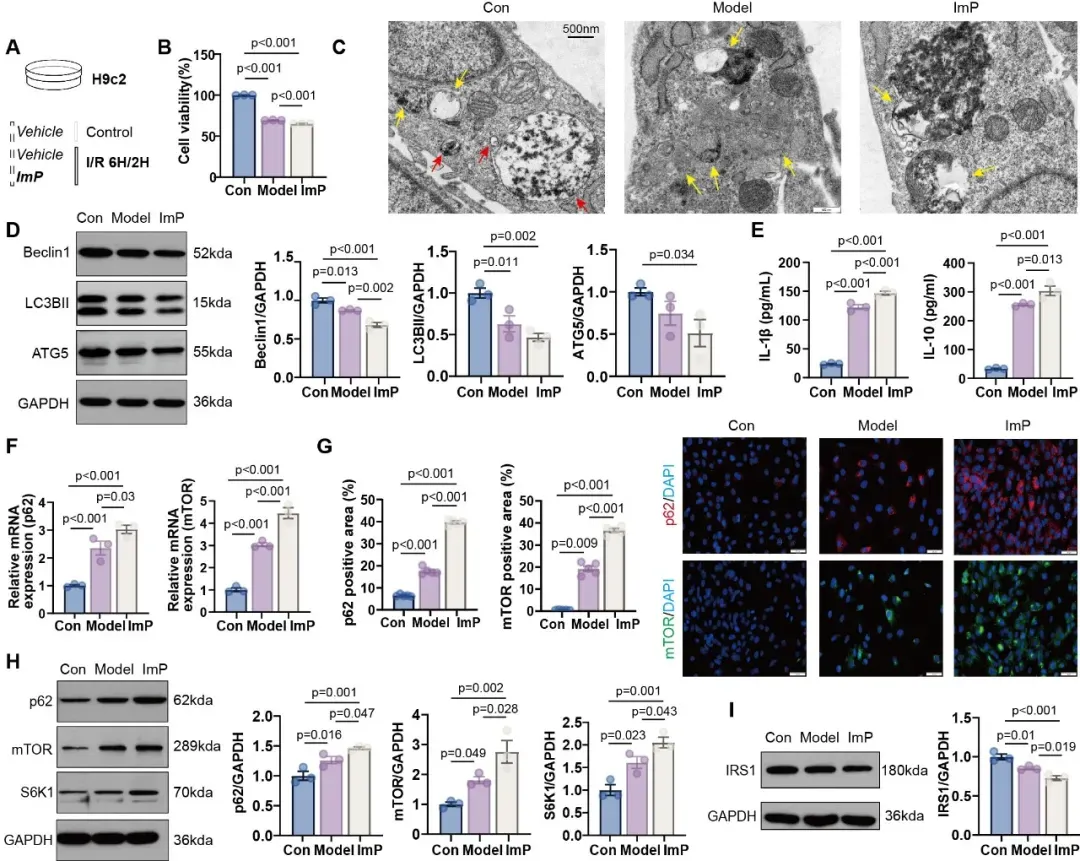
图4. ImP在体外加重缺氧/复氧损伤并激活p62/mTOR/S6K1
研究团队进一步探究ImP加重心肌损伤的作用是否依赖p62相关通路。在体外H/R+ImP条件下,p62敲低可部分改善细胞超微结构异常,并削弱ImP诱导的p62/mTOR相关信号激活。同时,IRS1抑制并未随p62敲低而恢复,提示ImP对心肌损伤的调控可能并不完全依赖p62/mTOR/S6K1通路(图5)。
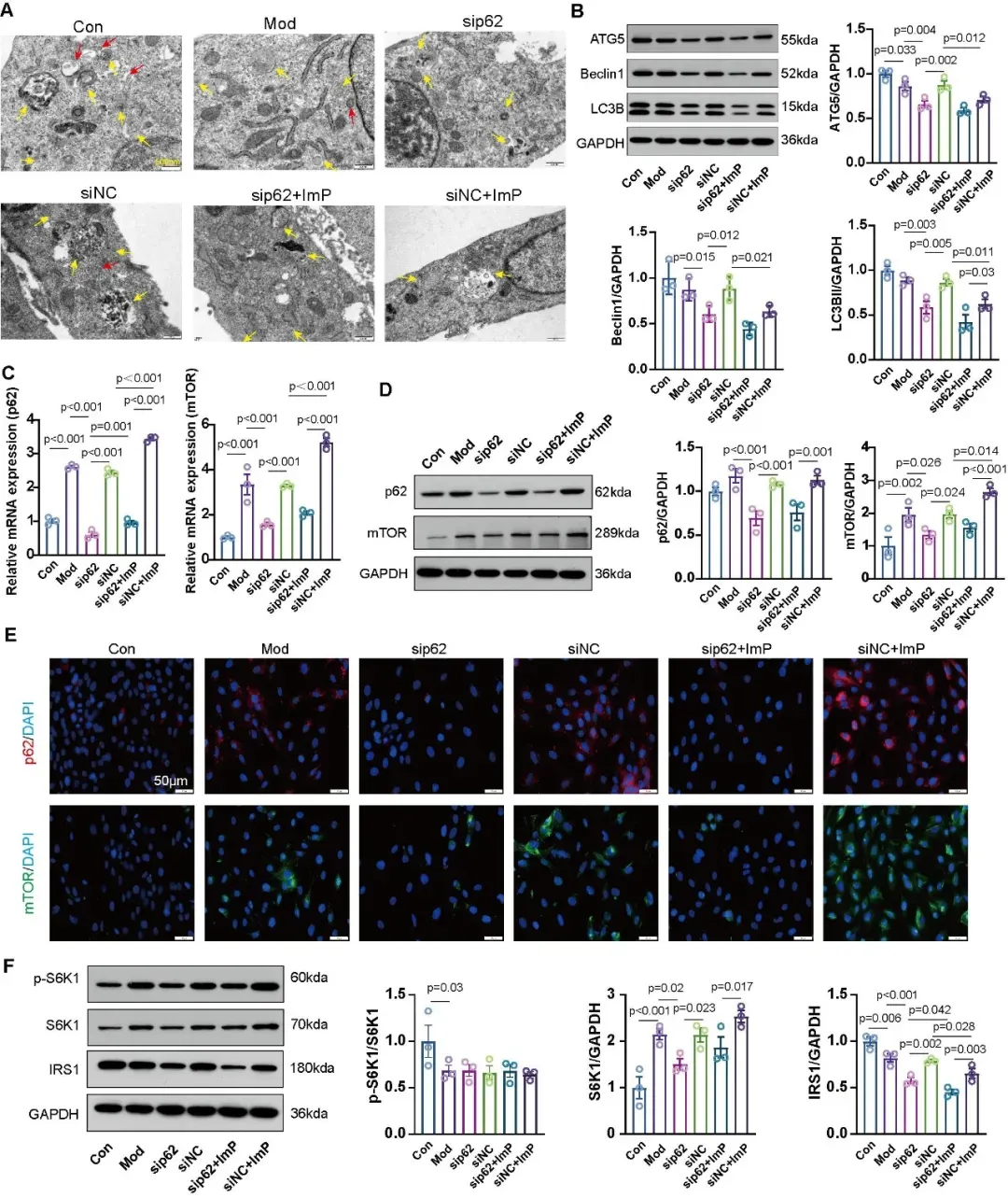
图5. p62敲低削弱ImP在体外对p62/mTOR/S6K1信号的激活作用
为了进一步确认上述机制,研究团队又进行了AAV-shp62的体内实验。结果显示,ImP可在MIRI基础上进一步加重心肌损伤,而p62敲低可明显缓解这一效应并抑制心肌p62/mTOR/S6K1信号通路的激活;p62敲低后IRS1仍处于抑制状态(图6)。
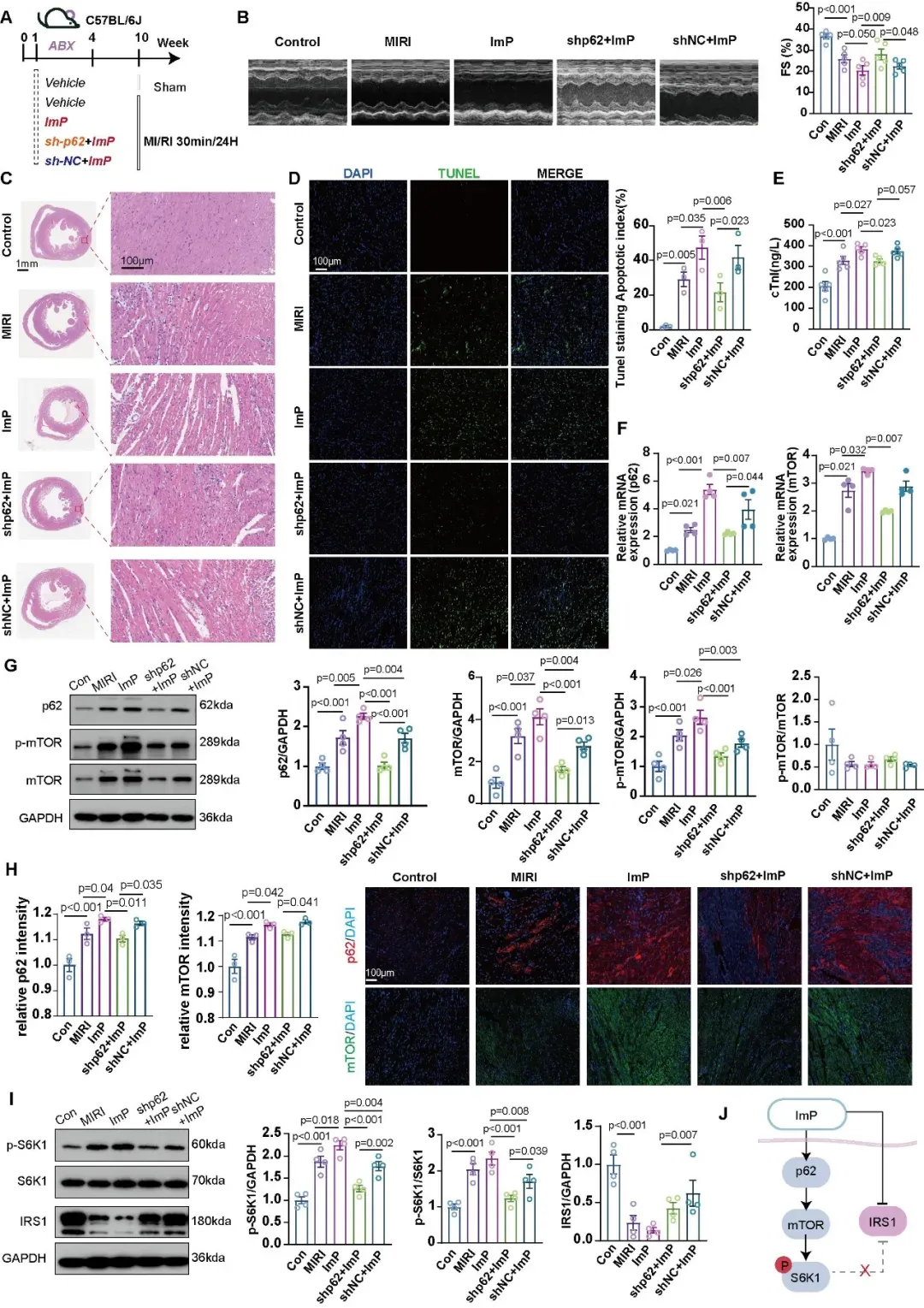
图6. 敲低p62可减弱ImP对小鼠心肌mTOR/S6K1信号的激活作用
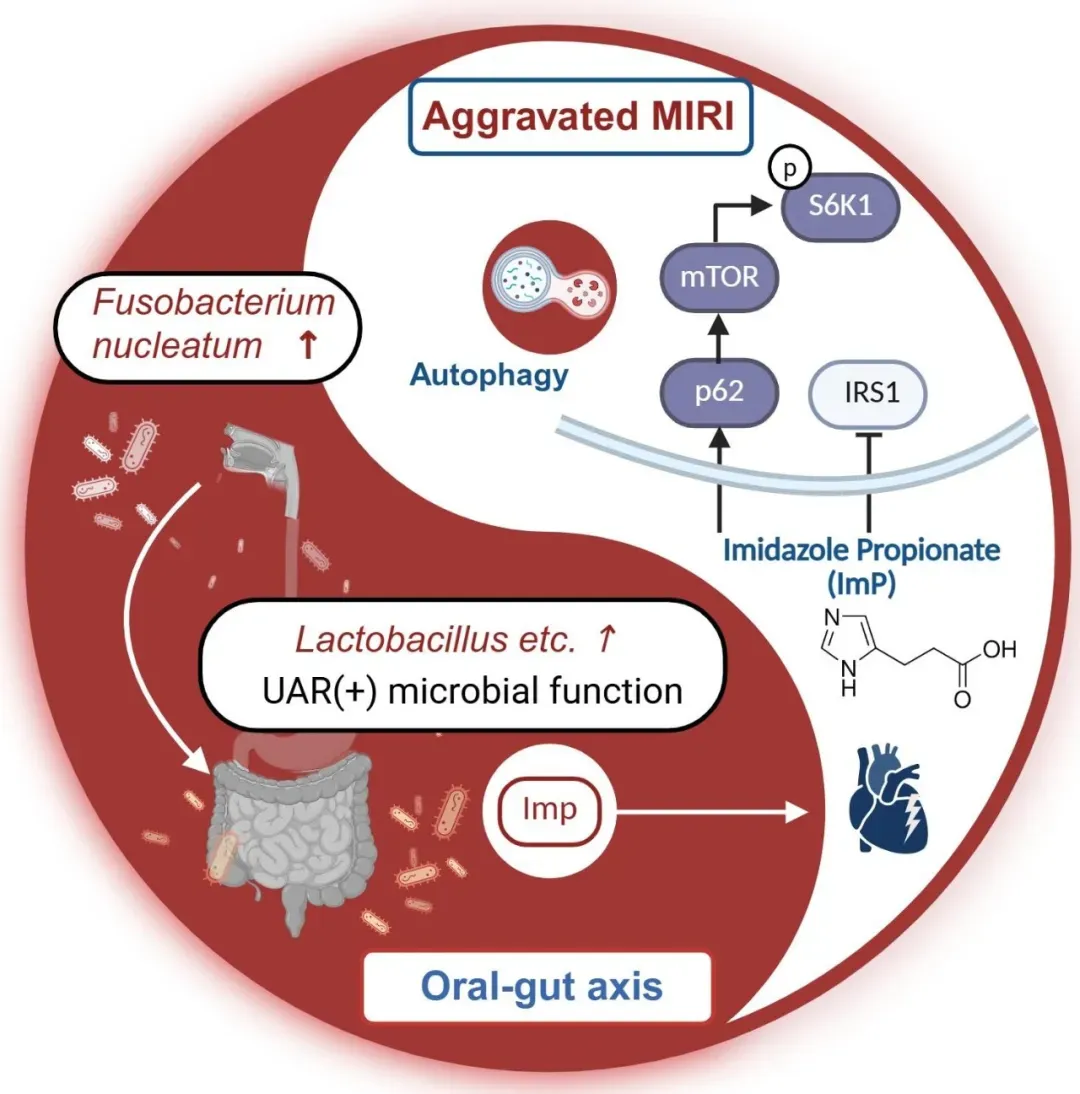
综上,本研究完整解析了“口腔具核梭杆菌—口-肠菌轴—肠道ImP—p62/mTOR/S6K1—心肌缺血再灌注损伤”的全新机制路线,证实口腔致病菌无需肠道定植,即可通过生态重塑介导心脏损伤;首次将肠道源性ImP确立为连接口-肠-心轴的核心代谢因子;揭示p62/mTOR/S6K1是ImP加重MIRI的关键信号。本研究为MIRI的防治提供“调控口腔菌群、抑制肠道ImP生成、阻断p62信号”的全新临床策略,既为解析中医“舌-肠-心”相关理论提供了现代微生物学与组学证据,也为心血管疾病的微生态干预开辟了新方向。
中国中医科学院医学实验中心在站博士后李逸雯助理研究员和西苑医院心血管病中心徐茜博士为本文的共同第一作者,中国中医科学院杨洪军研究员和中国中医科学院西苑医院刘玥主任医师为本文的共同通讯作者。该研究获得国家自然科学基金和北京市自然科学基金资助。
原文链接:
https://doi.org/10.1080/19490976.2026.2662082

版权声明:本文来源于Gut Microbes、论道心血管。中药大品种联盟(BBTCML)编校发布。编辑:远志。转载请标注作者及出处。本公众号文章、图片、视频版权归原作者所有,仅供学习参考,如有侵犯版权请联系中药大品种联盟秘书处,我们将及时回复。
中药大品种联盟秘书处联系方式:
邮箱:bbtcml@163.com
电话:84099077
《打破“不可逆”认知!中药逆转胃癌前状态疗效获国际认可》
《奇正藏药营业收入连续9年稳健增长 拟每10股派发现金红利4.1元》
《我国傣药产业研究(上)》
由于公众号平台更改了分发机制,不再按照时间显示,而是按权重随机推送,如您没有对我们公众号设为星标,也很少点在看,权重会降的非常低,有可能看不到我们的推文内容了。
如果大家觉得我们的内容还不错,还想每天看到更多文章,请大家动动手:
1.将“大品种联盟”公众号设为星标⭐
2.看完文章,在文末右下角给我们点下“在看”
3.点击左下角 “分享”,更欢迎您的留言评论。
▼▼▼点击阅读原文,查看历史消息

