中国博后一作Cell论文:发现全新lncRNA,调控造血干细胞,影响白血病风险


撰文丨王聪
编辑丨王多鱼
排版丨水成文
2026 年 5 月 1 日,哈佛大学医学院 Vijay G. Sankaran 团队(博士后吕鹏为论文第一作者)在国际顶尖学术期刊 Cell 发表了题为:Genetic variation reveals a homeotic long noncoding RNA that modulates human hematopoietic stem cells 的研究论文。
研究团队 HOXA 基因座与血液表型相关的变异时,意外发现在 HOXA7 和 HOXA9 之间反义方向存在一种特征不明显的长链非编码 RNA(lncRNA),其在造血干细胞(HSC)自我更新中发挥着关键作用,并将其命名为——HOTSCRAMBL。HOTSCRAMBL 的变异或缺失会降低 HOXA 依赖性急性髓系白血病的风险。

HOX 基因编码高度保守的转录因子,对胚胎发育至关重要,尤其在建立身体轴向模式和界定节段身份方面。其中,HOXA 基因座最初是作为身体分节的调控因子被发现的,而近年来的研究进一步确认了它对正常和恶性造血过程的关键作用。例如,HOXA 基因调控人类和小鼠造血干细胞的特化、自我更新与维持。此外,多个 HOXA 基因(尤其是HOXA9)在急性髓系白血病(AML)中常因体细胞驱动事件的激活而过表达,并提示预后不良。尽管这些发现强调了在造血过程中严格调控 HOXA 基因座的重要性,但其完整的底层调控机制仍未完全明晰。
之前的研究已发现多种调控造血干细胞中 HOXA 基因座表达的因子。例如,SOX17 可通过调控发育期造血内皮中的 HOXA 基因表达来启动定向造血。此外,混合谱系白血病融合蛋白可直接结合并促进白血病中 HOXA 基因的异常表达;造血干细胞中 HOXA 基因座转录延伸的增强会驱动髓系恶性肿瘤的遗传易感性。三维染色质相互作用能够维持增强子-启动子间的远程交互,而 HOXA7 与 HOXA9 之间 CTCF 边界结构的破坏会改变染色质拓扑结构,导致急性髓系白血病中后端 HOXA 基因的异常激活,这凸显了基因组构象在调控 HOXA 基因座中的关键作用。
长链非编码 RNA(long non-coding RNA,lncRNA)也已被证实在 HOXA 基因调控的多个方面发挥关键作用。研究显示,lncRNA Haunt 及其所在基因组区域在胚胎干细胞分化过程中对 HOXA 基因的激活产生相反的影响,凸显了该基因座顺式调控的复杂性。重要的是,HOXA 基因簇内部的反义 lncRNA 对 HOXA 基因表达具有直接的调控作用。例如,lncRNA HOTTIP 能促进染色质激活并介导 HOXA 基因间的染色质环化,其过表达可增强造血干细胞自我更新能力,从而参与急性髓系白血病的发生发展。位于 HOXA1 与 HOXA2 之间的 HOTAIRM1 则通过部分剪接调控机制,在髓系分化过程中调控 HOXA1 和 HOXA4 的表达,同时还能塑造染色质状态和三维结构以协调 HOXA 基因的激活。尽管这些发现证明了 lncRNA 及其他调控因子在该基因座转录调控中的关键作用,但人类遗传变异对 HOXA 基因表达的影响仍鲜有研究。
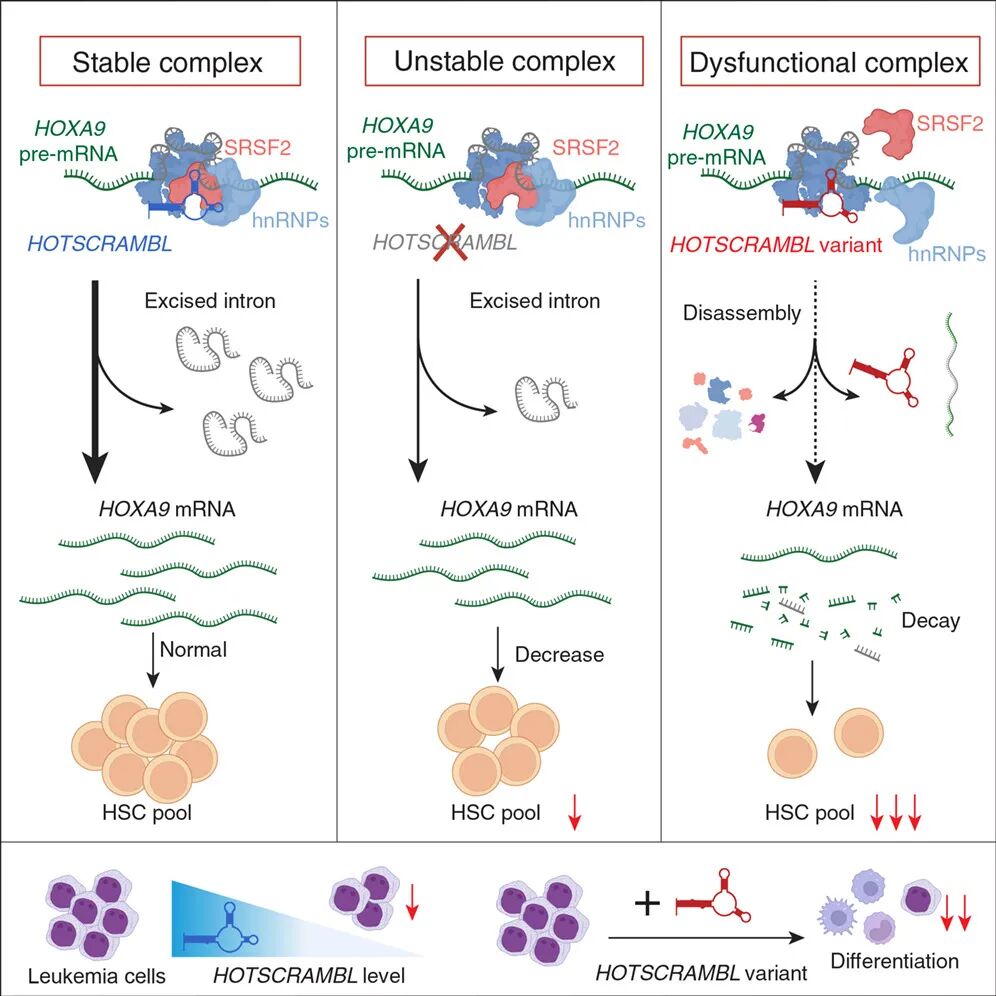
该研究的核心发现:
遗传精细定位确定了长链非编码 RNA HOTSCRAMBL 中的 rs17437411 位点;
HOTSCRAMBL 变异可预防克隆性造血和血液癌症;
HOTSCRAMBL 变异降低造血干细胞的自我更新能力;
HOTSCRAMBL 通过 SRSF2 促进造血干细胞和白血病细胞中 HOXA9 的剪接。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00439-3




点在看,传递你的品味




