外囊泡递送 in vivo CAR-中性粒细胞针对脑胶质瘤,全球首创疗法即将进入临床

2026 年 5 月 6 日
医麦客新闻 eMedClub News
近期,Nature Biomedical Engineering 上发表了由普渡大学 Bao Xiaoping 团队完成的题为 「CAR-neutrophils produced in vivo to treat glioma」 的研究论文。该研究开发了一种中性粒细胞特异性修饰 RNA 翻译平台(NeuSMRT),将工程化细胞外囊泡或脂质纳米颗粒(LNP)用于修饰 RNA 递送,从而在体内生成 CAR-中性粒细胞。

胶质母细胞瘤(GBM)是最具侵袭性、最常见的脑部肿瘤之一,中位总生存期约 15-18 个月。新兴过继性细胞治疗目前正开展多项 GBM 临床试验,但疗效有限。这一局限部分归因于血脑屏障(BBB)和局部免疫抑制性肿瘤微环境(TME)。
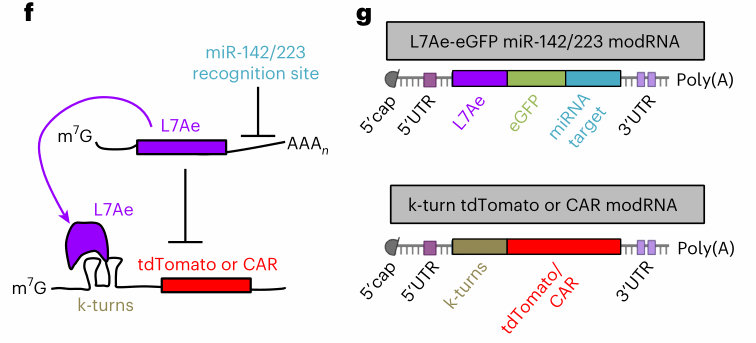
研究人员通过 GNSTM 基序糖基化肽-LAMP2b 融合蛋白,在工程化外囊泡表面修饰能够特异性结合的 CD177 靶向肽。为进一步实现中性粒细胞特异性 modRNA 表达,他们设计了 microRNA 响应型 L7Ae:k-turn RNA-蛋白开关,从而释放下游 CAR 蛋白的翻译。 实验数据显示,工程化 EVs 对人类原代中性粒细胞的递送效率达到约 60%,高于未经过修饰的外囊泡和传统 LNPs。
筛选不同 modRNA CAR 设计后,确定包含 CD28 跨膜结构域、胞内结构域与 CD3ζ 信号结构域的构建体适合介导中性粒细胞抗肿瘤信号。在同基因小鼠胶质瘤模型中,体内生成的 CAR-中性粒细胞显著抑制肿瘤生长、延长生存期。

单细胞 RNA 测序(scRNA-seq)与流式细胞术分析显示,胶质瘤肿瘤微环境中 T 细胞招募与活化增强,髓系细胞介导的免疫抑制降低。此外,CAR-中性粒细胞在同基因胶质瘤模型中增强化疗与 CAR-T 细胞治疗的疗效。NeuSMRT 在人源化 GBM 小鼠模型中也展现抗肿瘤活性,在犬类实验中显示良好安全性。
该研究论文提到,包括晚期前列腺癌与卵巢癌在内的其他实体瘤患者,很少获得持久且具有临床意义的免疫治疗响应,主要归因于 「冷」 肿瘤微环境,而 CAR-中性粒细胞可重新编程此类冷肿瘤微环境,增强更广谱实体瘤的治疗疗效。
基于 CAR 的治疗应用已超出肿瘤领域。CAR-T 细胞已被证实在治疗自身免疫性疾病、纤维化、慢性感染与其他非恶性疾病中有效。鉴于中性粒细胞在循环中丰度高,迁移能力优于 T 细胞,中性粒细胞可能成为靶向纤维化及其他癌症以外炎症或退行性疾病的治疗手段。
头部企业即将开展人体试验
中性粒细胞疗法目前仍处于早期探索阶段,头部企业当属美国的 Lift Biosciences,该公司认为中性粒细胞是实体肿瘤免疫治疗未来的核心,特化的抗肿瘤中性粒细胞在肿瘤控制与免疫治疗响应中发挥决定性作用:

经激活的中性粒细胞会启动干扰素刺激的抗肿瘤程序,在肿瘤微环境中招募并激活 T 细胞与 NK 细胞。
抗肿瘤中性粒细胞可直接清除肿瘤抗原逃逸变异株——这是 CAR-T 等靶向治疗失败的关键原因之一。
Lift Biosciences 的免疫调节型α中性粒细胞(IMANs)是首创的现成中性粒细胞谱系疗法,旨在直接杀死肿瘤细胞并重新激活癌症患者的抗肿瘤免疫。
2025 年 11 月,Lift Biosciences 在第 40 届癌症免疫治疗学会上展示了其首创 IMANs 的临床前研究数据:在肿瘤模型中,IMANs 增强效应细胞的招募,杀伤肿瘤细胞,并能够与 CAR-T 细胞协同,增强了难治性宫颈癌和胰腺癌模型中的肿瘤清除效果。据悉,Lift Biosciences 在今年 1 月宣布计划开展该候选产品的首个人体 I 期临床试验。
总结
中性粒细胞疗法企业极少,本质是由其短寿命、体外操作难、功能双向性、工艺壁垒高、临床监管无先例等多重硬核壁垒共同决定的。但当下细胞治疗赛道正朝着多样化的方向发展,越来越多的研究正为后续临床转化进行铺垫,Lift Biosciences 即将进一步验证,值得期待。
责任编辑丨浔
校对丨浔
参考资料:
1.Chang, Y., Shao, K., Li, H. et al. CAR-neutrophils produced in vivo to treat glioma. Nat. Biomed. Eng (2026).
2.企业官网

点点“分享”、“点赞”和“在看”
给我充点儿电吧~
