33 款双抗 ADC 齐发,5 款有望率先「冲线」

2026 年 5 月 5 日
医麦客新闻 eMedClub News
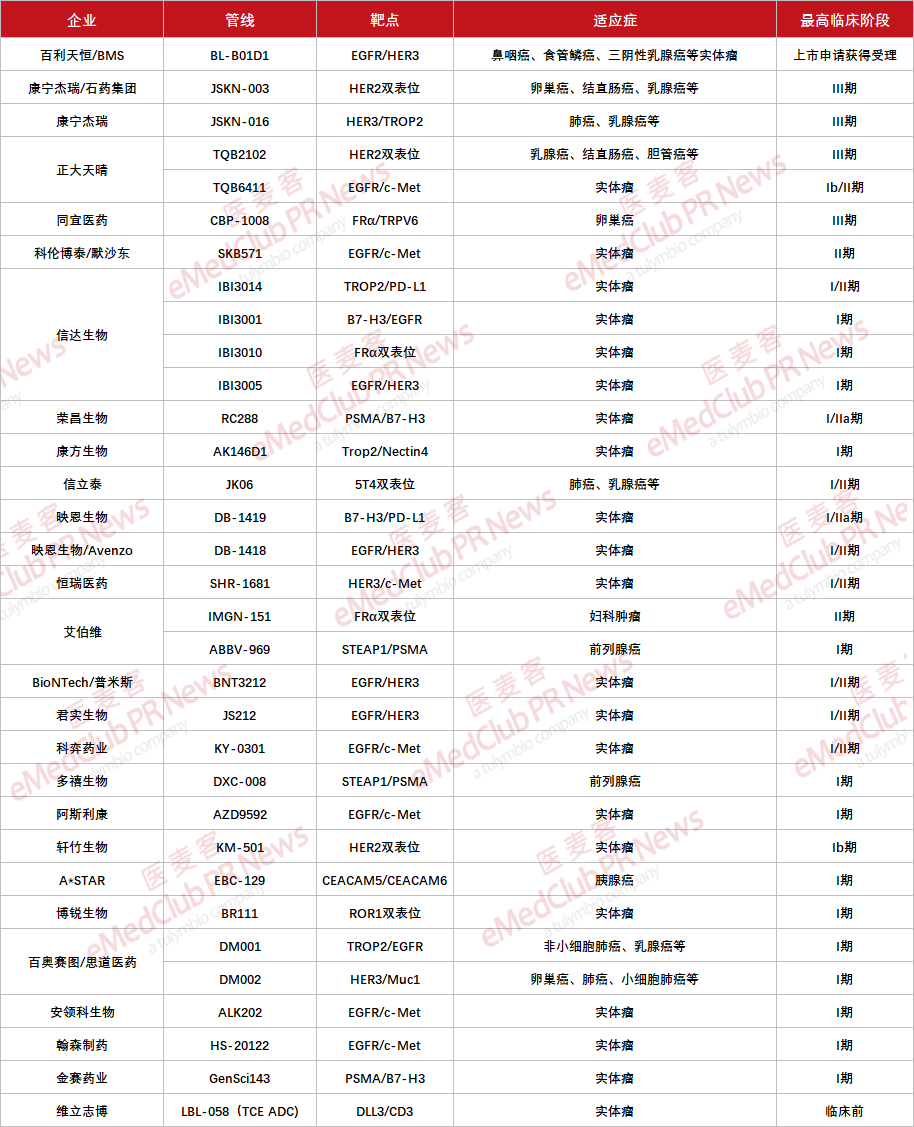
从管线布局来看,中国企业已在双抗 ADC 领域已形成产业集群优势。
靶点选择上,HER2、EGFR、c-Met、TROP2 等传统 ADC 热门靶点仍是主流组合选择,反映出企业对「经典靶点验证+双抗协同增效」策略的偏好。同时,也出现了 FRα/TRPV6、STEAP1/PSMA 等差异化组合,体现行业在细分领域寻求突破的探索意图。值得关注的是,除肿瘤特异性靶点外,PD-L1、CD3 等免疫调节类靶点的组合布局,标志着双特异性 ADC 技术正向免疫调控领域延伸。
适应症布局则呈现明显的临床需求导向特征,管线高度集中于实体瘤领域,尤其肺癌、胃癌、乳腺癌等高发癌种。
临床阶段分布上,尽管整体仍属早期开发阶段,但头部企业已逐渐拉开身位。百利天恒、康宁杰瑞、正大天晴、同宜医药等企业率先突破,均已有产品挺进 III 期临床,国产双特异性 ADC 正迎来临床价值验证的关键期。
双特异性 ADC 代表管线
百利天恒/BMS:BL-B01D1
BL-B01D1(iza-bren)是一款 EGFR×HER3 双特异性 ADC,其双特异性抗体部分采用了差异化结合亲和力设计,通过四肽可裂解连接子偶联了新型拓扑异构酶 I 抑制剂 ED04(喜树碱衍生物),药物抗体比率(DAR)达到了 8,既能够有效减少单靶点耐药,又能够产生强大的「旁观者效应」,杀伤肿瘤细胞的同时降低脱靶毒性。
2025 年 11 月,BL-B01D1 的上市申请获得 CDE 受理,这也是全球首个靶向 EGFRxHER3 双特异性 ADC 的新药上市申请成功受理。该受理是基于 BL-B01D1 在鼻咽癌的 III 期临床试验(研究方案编号:BL-B01D1-303)期中分析达到主要终点。与化疗相比,Iza-bren 显著提高了客观缓解率(ORR)和无进展生存期(PFS)。

2026 年 1 月,BL-B01D1 用于治疗既往经 PD-1/PD-L1 单抗联合含铂化疗治疗失败的复发性或转移性食管鳞癌的新药上市申请获得 CDE 受理,这是基于 BL-B01D1 在食管鳞癌的 III 期临床试验(研究方案编号: BL-B01D1-305)的积极结果:经独立数据监查委员会(iDMC)判断,在预设的期中分析中达到 PFS 和总生存期(OS)双主要终点,均取得阳性结果。
早在 2023 年 12 月,百利天恒与 BMS 达成关于 BL-B01D1 的合作,潜在交易总额高达 84 亿美元,2025 年 11 月,百利天恒触发里程碑事件,获得了 BMS 支付的 2.5 亿美元里程碑付款。
康宁杰瑞:
JSKN003(石药集团合作)、JSKN-016
JSKN003 是康宁杰瑞通过将安尼妥单抗 Fc 上糖基定点偶联获得 DAR 4 的均一稳定的 ADC,能够结合肿瘤细胞 HER2 的两个表位,通过增强细胞内吞释放拓扑异构酶Ⅰ抑制剂,发挥肿瘤杀伤作用。相较于同类药物,其具有血清稳定性更优、更低的血液学毒性、更强的肿瘤抑制和旁观者杀伤效应,显著扩大了治疗窗。
2024 年,石药集团子公司以潜在高达 30 亿元获得 JSKN003 在中国内地肿瘤适应症的独家开发、销售及商业化许可。2025 年 10 月,JSKN003 获 CDE 批准,开展用于治疗 HER2 阳性晚期结直肠癌的 III 期临床研究;2026 年 2 月,JSKN003 已完成该临床的首例患者给药。

根据 2025 年欧洲肿瘤内科学会(ESMO)大会上发布的数据,JSKN003 在 32 例 HER2 阳性晚期结直肠癌患者中,ORR 为 68.8%,mPFS 为 11.04 个月,相较于现有疗法展现出明显的疗效优势。
JSKN-016 是康宁杰瑞利用单域抗体和双抗平台开发的靶向 TROP2 和 HER3 双抗,通过糖基定点偶联获得 DAR4 的均一稳定的 ADC,可以精准结合肿瘤细胞表面受体,阻断致癌信号通路并释放拓扑异构酶Ⅰ抑制剂杀伤肿瘤,糖基化偶联技术使其具有高稳定性与低脱靶毒性。
2026 年 3 月,JSKN-016 用于治疗三阴性乳腺癌的 III 期临床研究(JSKN016-301)已完成首例患者给药。
正大天晴:TQB2102、TQB6411
TQB2102 抗体端采用非对称型结构设计,同步结合 HER2 的 ECD II/IV 结构域,显著提升肿瘤选择性及内吞效率,增强抗肿瘤活性,通过酶裂解型连接子搭配拓扑异构酶 I 抑制剂毒素,DAR 优化至 5.8-6.0。
2026 年 3 月,正大天晴宣布 TQB2102 用于 HER2 阳性晚期乳腺癌的一项 III 期临床试验已完成全部受试者入组。
在 2025 年的 ESMO 大会上,TQB2102 用于 HER2 阳性晚期乳腺癌 Ib 期研究结果显示:既往多线治疗失败的 HER2 阳性乳腺癌患者的 ORR 为 58.8%,其中目标剂量 6 mg/kg 组 ORR 高达 67.4%,整体安全性良好。
TQB6411 是一款 EGFR/c-Met 双抗 ADC,与肿瘤细胞表面 EGFR、c-Met 结合后能够阻断其信号通路激活,经细胞内吞并转运到溶酶体,连接子经酶切后释放出毒素,导致 DNA 损伤和细胞死亡,并且能通过旁杀效应杀死相邻肿瘤细胞。
2025 年 7 月,TQB6411 顺利完成 I 期临床研究的首例受试者给药;2026 年 3 月,TQB6411 针对经治的复发或转移性食管癌 Ib/II 期临床试验正在招募。
同宜医药:CBP-1008
CBP-1008 是由同宜医药自主开发的 Bi-XDC 技术平台研制的第一代双配体小型药物偶联体,其双配体分别靶向肿瘤细胞膜上表达的 FRα和 TRPV6 受体。另外,CBP-1008 分子量约为传统 ADC 药物的 1/50,生产成本和用药费用远低于 ADC 药物。
据官方披露,CBP-1008 在既往接受过 1-3 线治疗的铂耐药 OC(PROC)患者中,RP3D 剂量下表现出显著疗效:在高级别浆液性腺癌(HGSOC)和透明细胞卵巢癌患者中,不论 FRα和 TRPV6 表达水平,ORR、DCR 和 OS 显著优于铂耐药 OC 治疗的历史数据。2025 年 7 月,CDE 同意 CBP-1008 开展铂耐药卵巢癌(PROC 注册)的 III 期临床试验。
责任编辑丨浔
校对丨浔
参考资料:
1.企业官网及公开资料
2.CDE

点点“分享”、“点赞”和“在看”
给我充点儿电吧~
