正文如下:
问:药品注册申请受理后,需要申请人在原申报资料基础上补充新的技术资料的,申请人如何进行补充资料?
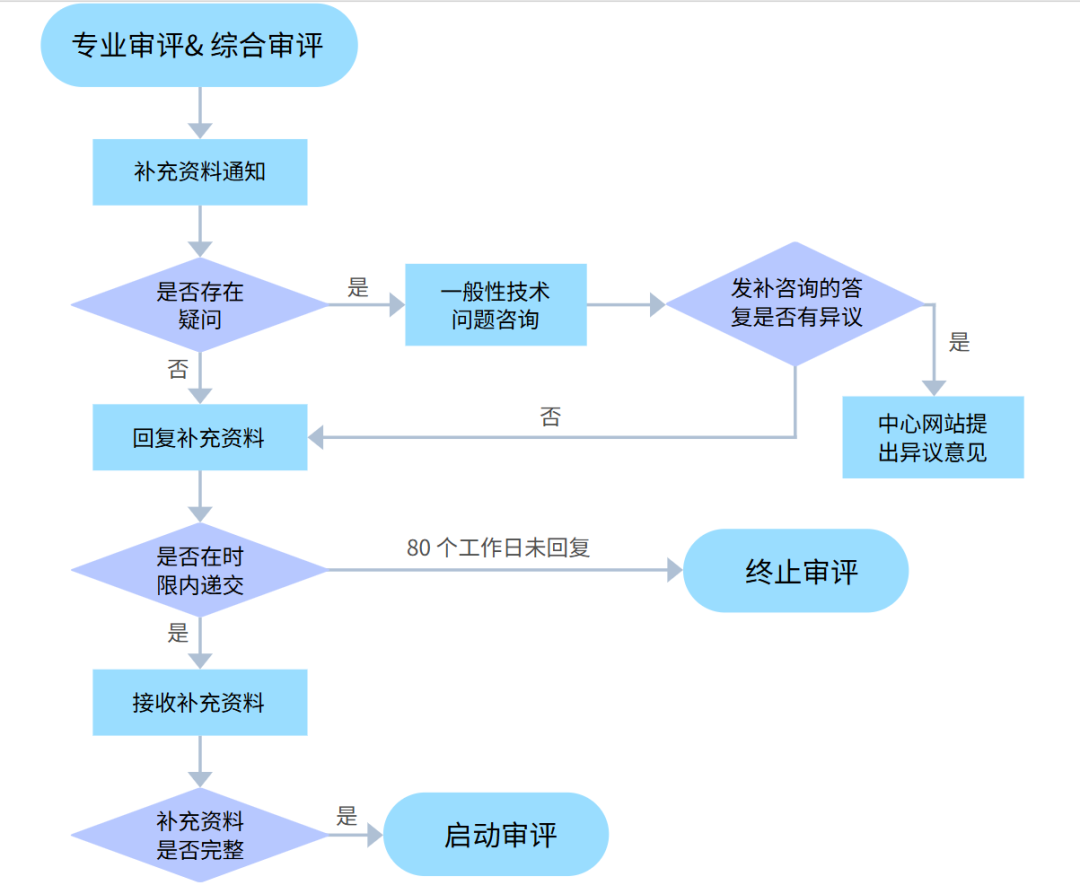
答:《药品注册管理办法》第八十七条 药品注册申请受理后,需要申请人在原申报资料基础上补充新的技术资料的,药品审评中心原则上提出一次补充资料要求,列明全部问题后,以书面方式通知申请人在80个工作日内补充提交资料。
申请人对发补要求有疑问,可在接到书面补充资料通知10个工作日内通过药品审评中心网站提出一般性技术问题咨询申请,由项目管理人员协调适应症团队在15个工作日内以书面或会议方式完成答复,需要召开会议的,原则上以电话会议形式进行。申请人对发补咨询的答复仍有异议的,可在收到答复意见之日起10个工作日内通过药品审评中心网站提出异议意见,异议意见应列明理由和依据。申请人应在80个工作日内一次性按要求提交全部补充资料,补充资料时间不计入药品审评时限。药品审评中心收到申请人全部补充资料后启动审评,审评时限延长三分之一;适用优先审评审批程序的,审评时限延长四分之一。1.《药品注册管理办法》(国家市场监督管理总局令第27号)2.国家药监局药审中心关于发布《药品审评中心补充资料工作程序(试行)》的通告(2020年第42号)3.国家药监局药审中心关于发布《国家药品监督管理局药品审评过程中审评计时中止与恢复管理规范(试行)》的通知(药审业〔2022〕614号)5.国家药监局药审中心关于将补充资料通知由纸质邮寄调整为电子推送有关事宜的通知6.国家药监局药审中心关于办公地址搬迁有关事宜的通知8.关于试行以网络传输方式提交药品注册电子申报资料的通知9.关于取消提交临床试验数据库光盘、更新电子申报资料制作软件的通知1.药品注册审评补充资料管理工作,按照《药品注册管理办法》及《国家药监局药审中心关于发布〈药品审评中心补充资料工作程序(试行)〉的通告》(2020年第42号)要求执行。2.请严格按照补充通知的内容要求提交补充资料,资料的顺序为:补充资料通知、如涉及检验部门复核须提交送检凭证加盖检验部门公章、提交资料说明及《药品审评中心补充资料工作程序(试行)》附件声明(加盖公章)、资料目录、技术资料(申请人应逐条回复每一项需要补充的内容,按补充资料通知中各项意见的顺序排列)。对于一并提交的其他超出补充资料通知内容的资料,基于注册管理的一般要求不予接收,并因人力所限,该部分资料不予退回,由药品审评中心统一做销毁处理。3.申请人未能在规定时限内提交补充资料的情形,药品审评中心将按照《药品注册管理办法》第九十二条第二款第(四)项不予批准情形办理终止审评程序。4.邮寄补充资料前,请在药品审评中心网站“申请人之窗”相关预约模块,如实填写并提交申报资料相关信息,收件信息如下:收件人:国家药监局药品审评中心业务管理处。收件地址:北京经济技术开发区广德大街22号院,邮编:100163 收件时间:工作日上午8:30—11:30。