80亿美金的重磅药,竟是过期分子组合


近日,Axsome Therapeutics发布财报,旗下用于治疗重度抑郁症(MDD)的重磅药物Auvelity第一季度销售额达1.53亿美元,同比增长59%,累计开出超过22.3万张处方,同比增长35%。一周前,这款旧分子新组合刚刚获FDA批准用于治疗阿尔茨海默病躁动症(ADA)。为此,Axsome将Auvelity峰值销售额预期上调至80亿美元,短短数日内公司股价已跳涨23%,过去三周累计涨幅达到45%。

80亿美金的底气从何而来

Auvelity于2022年获批,是60多年来首款具有新作用机制的抑郁症口服疗法,今年又进一步成为获批治疗ADA的首款非抗精神病药物。其作用基础来自国民止咳药右美沙芬和老牌抗抑郁药安非他酮两种老药分子:右美沙芬作为非竞争性NMDA受体拮抗剂与sigma-1受体激动剂,调控谷氨酸能神经传递,带来快速情绪改善;安非他酮既作为CYP2D6酶抑制剂,显著延长右美沙芬的半衰期,又作为去甲肾上腺素-多巴胺再摄取抑制剂,补充单胺能调节效应。

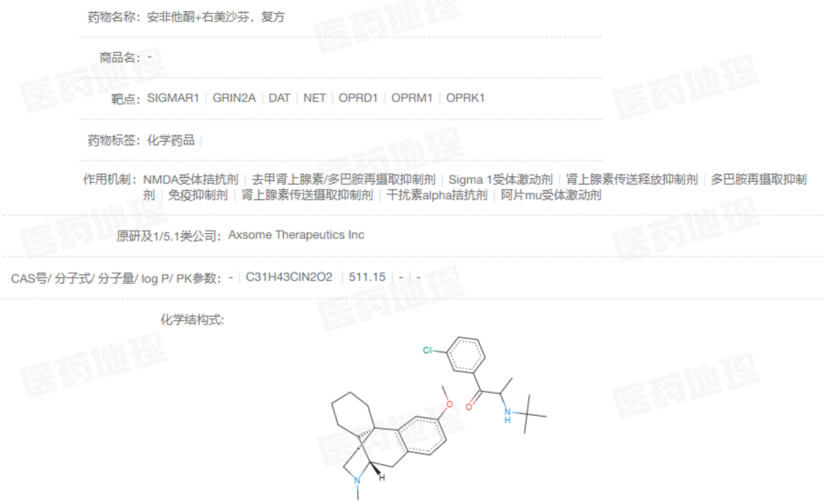
Auvelity基本信息
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
这两个早已过了专利保护期的“廉价分子”组合在一起,Axsome却扬言要卖出80亿美元。这究竟是资本叙事下的泡沫,还是对药物价值的重新定义?
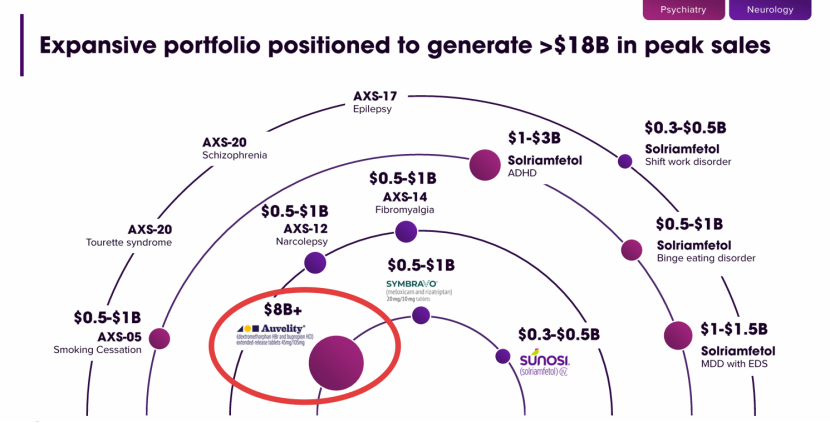
来源:Axsome官网
在全美700万AD患者中,76%受躁动困扰,潜在人群超530万,而市场上仅有灵北和大冢的Rexulti一款获批药物。2025年Rexulti销售额为62.1亿丹麦克朗(约合9.73亿美元),增长23%。不幸的是,Rexulti带有黑框警告,提示痴呆相关精神病患者死亡风险更高,这无疑将推高Auvelity的市场预期。
此前,Axsome与梯瓦达成的和解协议约定,美国市场的仿制药最早要到2038年才能进场。Axsome表示Auvelity的现有的两项适应症将各贡献一半营收,且正在将销售团队扩充至630名代表,覆盖68000名医疗专业人士。
与此同时,公司计划于今年第二季度启动Auvelity用于戒烟的2/3期临床试验,并强调靶向NMDA和sigma-1受体对其他神经精神疾病具有高度潜在适用性,加上处于临床后期的ADHD、暴食症和倒班工作障碍等管线,80亿美元的故事似乎有了更大的想象空间。
国内企业抢争首仿
中国市场的Auvelity仿制药虽然起步略,但监管通道已于2024年1月正式打开——NMPA发布第75批仿制药参比制剂目录,将氢溴酸右美沙芬盐酸安非他酮缓释片纳入参比制剂,为国产仿制药研发确立了明确的质量对标标准。
然而,2024年7月1日起,国家药监局已将右美沙芬(包括其盐类及单方制剂)列入第二类精神药品目录。一方面提升了药物管控,另一方面也对仿制药企的原料药供应链管理、生产资质和处方流通提出了更高的合规要求。
就在上周,江苏恩华药业按化药注册分类3类申报的右美沙芬安非他酮缓释片上市申请获CDE受理,成为该品种首家提交上市申请的国内企业。若后续顺利获批,恩华有望摘得国内首仿资格,率先填补原研及仿制药均未在华上市的空白。

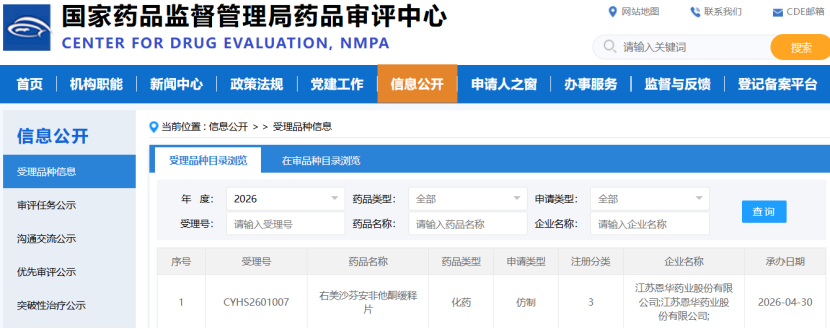
来源:CDE官网
恩华的速度建立在此前扎实的临床积累之上。其针对18-65岁符合DSM-5诊断标准的抑郁症患者III期临床试验(登记号:CTR20253260)目前已完成。
石药集团欧意药业是另一家进度靠前的玩家。其BE试验(登记号:CTR20242867)早在2024年8月已启动。III期试验(登记号:CTR20250967)也于2025年3月开展,目前已完成,但石药在上市申报时间线上已落于恩华之后。
四川科伦药业的BE试验(登记号:CTR20253243)于2025年8月公示,目前处于招募中状态。
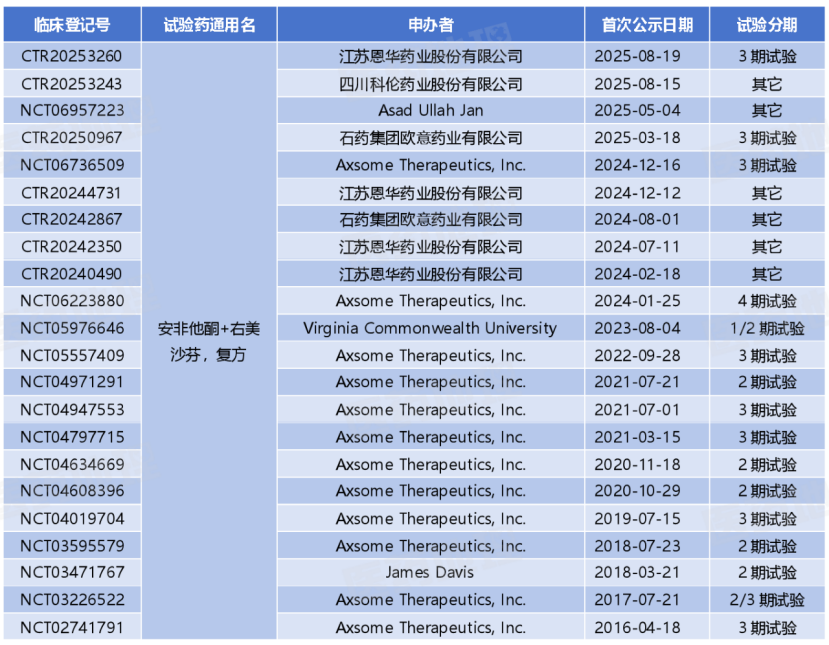
安非他酮+右美沙芬全球临床试验
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
与上述三家直接仿制Auvelity的策略不同,信立泰选择不走仿制药而是走“me-better”的道路。其开发的SAL0114为氘代右美沙芬安非他酮复方制剂,通过将右美沙芬分子中的氢原子替换为氘原子,有望改善药物的代谢稳定性、延长半衰期,从而优化给药方案。目前SAL0114正处于2期临床阶段,同时正在开展与Auvelity的头对头I期临床试验。

安非他酮+氘右美沙芬全球临床试验
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
Auvelity“旧分子新组合”的精彩故事,能不能让80亿美元从PPT走进财报,让我们拭目以待。



