含羰基化合物RP-HPLC峰形异常原因剖析(1)—亲核加成
发布时间:2026-05-07来源:药事纵横
摘要:含羰基化合物在反相高效液相色谱(RP-HPLC)分析中常出现峰分叉、峰展宽、前伸或拖尾等峰形异常现象,严重影响定性与定量结果的准确性。本文从有机化学反应机理出发,系统剖析了该类化合物在色谱过程中发生峰形畸变的根本原因之一,即酸性条件下醛酮与流动相中水、醇及铵盐等亲核试剂发生可逆亲核加成反应,生成偕二醇、半缩醛/酮、亚胺等衍生物,导致化合物以多种形态共存于色谱柱中。基于上述机理,本文以杂环芳香醛为模型化合物,设计了系统的实验方案,分别考察碱性亲核缓冲盐体系、碱性非亲核缓冲盐体系、亲核试剂辅助高柱温及非亲核试剂辅助高柱温四种策略对峰形的改善效果。实验结果表明,使用碱性非亲核缓冲盐常规柱温体系或酸性非亲核缓冲盐辅以高柱温体系均可显著改善色谱峰形。一、理论基础
1.1 醛酮与水加成
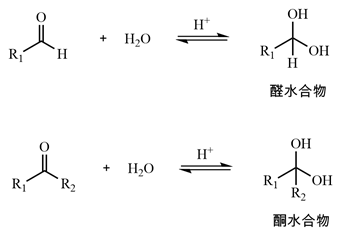
基础有机化学指出,水是亲核试剂,在酸性条件下,可以和醛酮发生亲核加成反应,形成相应的醛或酮加成水合物(偕二醇),这样的化合物在热力学上不稳定[1]。反应机理如图1所示。图1醛酮与水加成示意图Cooper等人[2]采用¹H-NMR分析乙醛酸水溶液时,发现在pH 0.5–6.0范围内水合物(偕二醇)占主导(pH 0.5时>99%,pH 6.0时仍达95%);Gray Be等人[3]采用¹³C-NMR分析α-蒎烯和β-石竹烯的醛类氧化产物时,在氘水(D₂O)中观察到醛基碳信号(~200 ppm)显著减弱,同时在90 ppm附近出现新的偕二醇碳信号。这些为醛的水亲核加成提供了直接核磁证据。Bure等人[4]采用ESI-MS检测乙醛酰胺类肽时,在低pH水溶液中直接观察到对应水合物([M+H₂O+H]⁺)的分子离子峰,为醛的水亲核加成提供了直接质谱证据。1.2 醛酮与醇加成
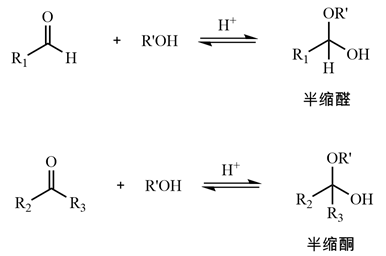
基础有机化学指出,醇是亲核试剂,在酸性条件下,可以和醛酮发生亲核加成反应,生成半缩醛或半缩酮,半缩醛和半缩酮在酸性或碱性溶液中都是不稳定的[5]。反应机理如图2所示:图2醛酮与醇加成示意图Nastase等人[6]采用密度泛函理论(DFT)计算模拟H-ZSM-5沸石孔道内13C-NMR化学位移时,在半缩醛和甲氧基甲醇模型中获得了与醛酮-醇加成产物一致的特征化学位移(分别为110~111ppm和100~101ppm);Munster等人[7]采用¹H-¹³C-HSQC和HMBC核磁共振技术分析2,3-二醛纤维素在水溶液中的结构时,明确检测到分子内半缩醛(五元环)和分子间半缩醛的特征相关信号(¹Hδ 3.42~4.78,¹³Cδ 57.3~96.8 ppm),为醛酮在酸催化环境下与醇亲核加成生成半缩醛提供了理论NMR依据。1.3 醛酮与铵盐加成
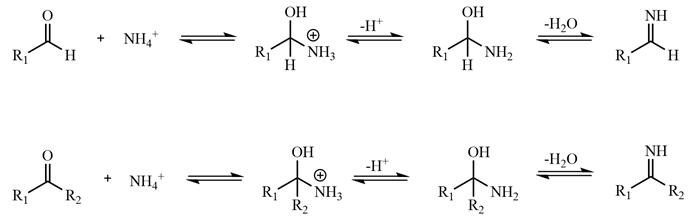
基础有机化学指出,铵盐是亲核试剂,其孤对电子进攻羰基碳,形成α-氨基醇衍生物,随后,羟基氧将质子转移给氮原子,生成氨鎓醇盐(或相应的铵离子形式),在酸性条件下,羟基与相邻的氢(来自氮上)以水分子形式离去,生成亚胺[8]。反应机理如图3所示:图3醛酮与铵盐加成示意图Liu等人[9]采用LC-Q-TOF MS分析含活性羰基化合物时,在以0.1%氨水为流动相的条件下,明确检测到[M+imine+H]⁺(亚胺加合离子)峰,同时原始醛的[M+H]⁺信号显著减弱,直接证实了铵盐(NH4+)作为亲核试剂与醛酮发生亲核加成-脱水反应生成亚胺。二、RP-HPLC峰形异常可能原因剖析
上述三类亲核加成反应均可在RP-HPLC的色谱过程中发生,导致同一化合物在色谱柱中以多种形态共存,包括原形化合物、偕二醇、半缩醛/半缩酮及亚胺等。这些形态在固定相上的保留行为存在差异,从而在色谱图上表现为峰展宽、分叉、前伸或拖尾等多种峰形异常。表1对上述理论进行了系统汇总,并针对性地分析了峰形异常的可能原因及初步解决方案。表1借鉴点汇总、RP-HPLC峰形异常原因分析及可行性实施方案拟定<span lang="EN-US" style="font-size:12.0pt; font-family:"Times New Roman",serif; mso-fareast-font-family:仿宋; mso-no-proof: <p>yes; "><span leaf=;" "="">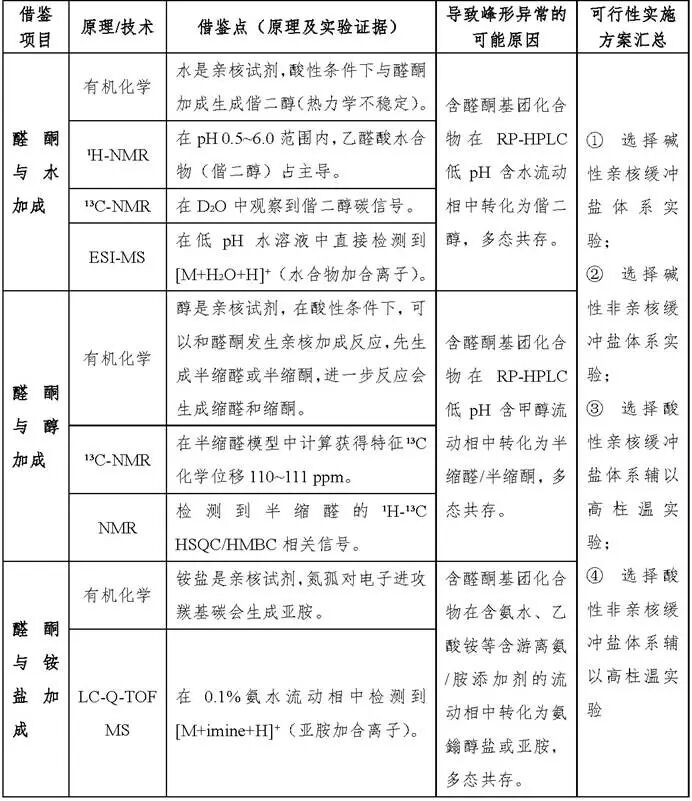
三、实验验证
3.1 模型化合物
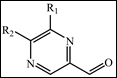
本研究选取杂环芳香醛SM1作为模型化合物进行系统实验。SM1吡嗪环上两个高电负性氮原子的强吸电子诱导效应,使整个环成为缺电子体系,直接拉走与其相连的醛基碳上的电子云,同时芳环无法通过共轭给电子来补偿,使羰基的亲电性显著增强,亲核加成反应活性较高,峰形异常问题突出,适合作为机理验证的典型对象。3.2 酸性亲核缓冲盐常规柱温体系(亲核加成)
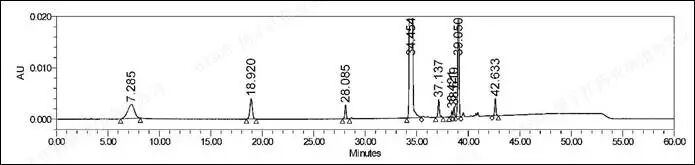
关键色谱条件为:常规C18(BDS Hypersil C18,4.6mm×250mm,5μm)+20mM乙酸铵缓冲液(pH 6.0)-甲醇+柱温30℃。系统适用性典型图谱如下所示。图4 SM1酸性亲核缓冲盐常规柱温体系对应图谱SM1(RT=7.285)主峰严重展宽,峰宽2.48min,对称因子2.34。3.3 碱性亲核缓冲盐常规柱温体系(抑制亲核加成)
关键色谱条件为:耐碱C18(XBridge C18,4.6×150mm,3.5μm)+20mM乙酸铵缓冲液(pH 10.5)-甲醇+柱温30℃。系统适用性典型图谱如下所示。图5 SM1碱性亲核缓冲盐常规柱温体系对应图谱SM1(RT=7.867)主峰展宽依旧严重,峰宽1.94min,对称因子2.13。3.4 碱性非亲核缓冲盐常规柱温体系(避免使用亲核试剂+抑制亲核加成)
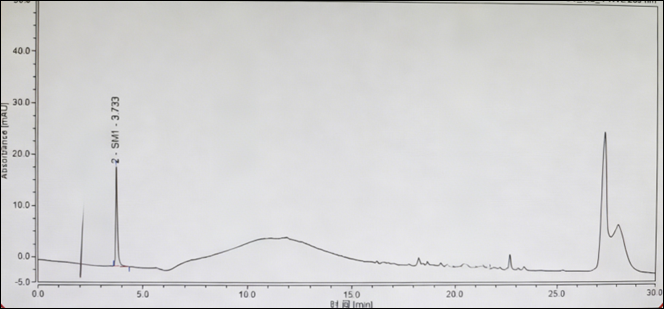
关键色谱条件为:耐碱C18(XBridge C18,4.6×150mm,3.5μm)+20mM碳酸钠缓冲液缓冲液(pH 10.5)-乙腈+柱温30℃。典型图谱如下所示。图6 SM1碱性非亲核缓冲盐常规柱温体系对应图谱SM1(RT=3.733)峰尖锐对称,峰宽0.35min,对称因子1.05。3.5 酸性亲核缓冲盐辅以高柱温体系(促进多态向原型转化)
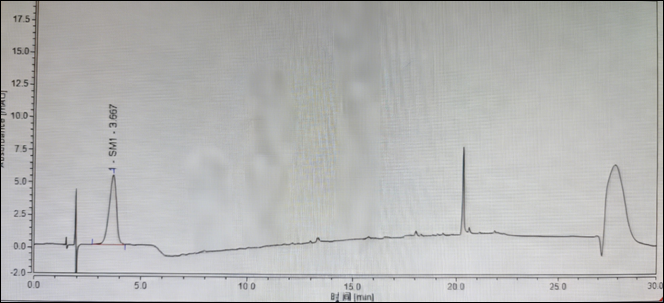
关键色谱条件为:耐高温C18(Zorbax SB-C18,4.6×150mm,3.5μm)+20mM乙酸铵缓冲液(pH 6.0)-甲醇+柱温60℃。典型图谱如下所示。图7 SM1酸性亲核缓冲盐辅以高柱温体系对应图谱SM1(RT=3.667)主峰展宽改善,峰宽1.32min,对称因子0.72。3.5 酸性非亲核缓冲盐辅以高柱温体系(抑制多态形成+促进多态向原型转化)
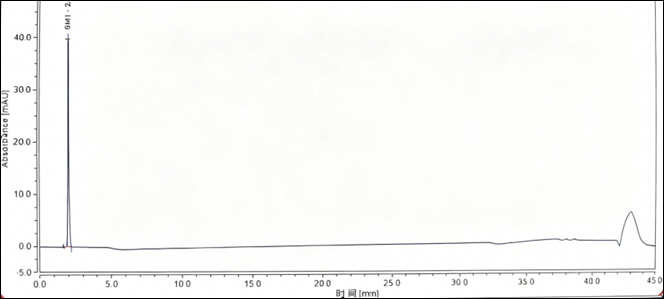
关键色谱条件为:耐高温C18(Zorbax SB-C18,4.6×150mm,3.5μm)+20mM高氯酸钠缓冲液(pH 4.0)-乙腈+柱温60℃。典型图谱如下所示。图8 SM1酸性非亲核缓冲盐辅以高柱温体系对应图谱SM1(RT=2.015)峰尖锐对称,峰宽0.31min,对称因子1.03。四、结论
本文基于醛酮类化合物在RP-HPLC条件下易发生亲核加成反应的机理,设计了四种代表性的色谱体系,并以模型化合物SM1为对象进行了系统验证。通过对峰宽、对称因子的比较,得出如下结论:- 碱性非亲核缓冲盐常规柱温体系可同时满足“高pH抑制酸催化”与“无亲核试剂”两个关键条件,最终达到改善含醛酮基团化合物峰形的效果。
- 酸性非亲核缓冲盐辅以高柱温体系:在避免亲核试剂的同时利用高温促进形态归一化或加速互变,最终亦能达到改善含醛酮基团化合物峰形的效果。
基于上述预实验结果,针对含醛酮基团化合物的RP-HPLC方法开发,提出如下策略选择建议:使用非亲核性缓冲盐(如碳酸钠)提高流动相pH并配合乙腈为有机相,是解决含醛酮基团化合物峰形异常的首选策略。该策略从源头抑制了酸催化和亲核试剂两类致畸因素,适用于大多数含活泼羰基的化合物。当样品在碱性条件下不稳定(如含碱敏感基团、易发生消旋或降解),或受限于色谱柱耐碱性能无法更换时,在酸性条件(pH 2.0~6.0)下升高柱温(如60℃)可作为有效的备选方案。该策略通过热力学平衡加速多态向原形转化,在不引入亲核试剂的前提下亦能显著改善峰形。需指出,本文仅以单一的杂环芳香醛作为模型化合物进行了验证,使用范围可能存在一定的局限性,后续仍需在更多结构类型的含醛酮化合物(如脂肪醛、α,β-不饱和酮、甾体类酮等)中进一步验证。[1] 邢其毅, 裴伟伟, 徐瑞秋, 等. 基础有机化学(第4版)上册[M]. 北京: 北京大学出版社, 2016: 460, 465-466.[2] Cooper A J L, Redfield A G. Proton magnetic resonance studies of α-keto acids[J]. Journal of Biological Chemistry, 1975, 250(2): 527-532.[3] Gray Be A, Upshur M A, Liu P, et al. Cloud activation potentials for atmospheric α-pinene and β-caryophyllene ozonolysis products[J]. ACS Central Science, 2017, 3(5): 452-462.[4] Buré C, Marceau P, Meudal H, et al. Synthesis and analytical investigation of C-terminally modified peptide aldehydes and ketone: application to oxime ligation[J]. Journal of Peptide Science, 2011, 17(12). DOI: 10.1002/psc.1429.[5] 邢其毅, 裴伟伟, 徐瑞秋, 等. 基础有机化学(第4版)上册[M]. 北京: 北京大学出版社, 2016: 460, p466.[6] Nastase S A F, Ye Y, Li T, et al. Simulated 13C chemical shifts used to investigate zeolite catalysis[J]. Journal of Catalysis, 2023, 428: 115183.[7] Münster L, Hanulíková B, Machovský M, et al. Mechanism of sulfonation-induced chain scission of selectively oxidized polysaccharides[J]. Carbohydrate Polymers, 2020, 230: 115503.[8] 邢其毅, 裴伟伟, 徐瑞秋, 等. 基础有机化学(第4版)上册[M]. 北京: 北京大学出版社, 2016: 460, p460.[9] Liu G, Luan B, Xin L, et al. Peak distortion in reversed-phase liquid chromatography separation of active carbonyl-containing compounds: mechanism and solution for this overlooked phenomenon[J]. Journal of Chromatography A, 2019, 1598: 112-120.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。