第一AI药物
2026年的春天,对于全球生物医药行业而言,是一个充满分水岭意义的季节。在瑞士蒙特勒的医疗投资峰会、在波士顿剑桥的实验室、在杭州医药港的写字楼里,一个共同的话题被反复提及并激烈争论:究竟谁会成为第一支由人工智能设计并问世的药物?这不再是一个关于未来的科幻设想,而是一场正在发生的、由数据、算力和分子竞相奔跑的现实竞赛。作为长期观察这一领域的药物研发科学家,我认为有必要穿透资本市场的喧嚣与公关稿件的迷雾,立足于最真实的临床数据与监管动态,深度剖析这场关乎制药未来范式的“冰与火之歌”。
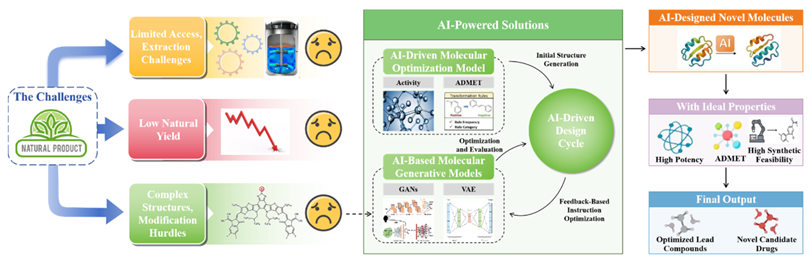
概念之争:如何定义“第一个AI药物”
在展开深度调研之前,我们必须首先建立一套严谨的评判坐标系。究竟什么样的药物才有资格被载入史册,被称为“第一个AI药物”?行业内对此存在显著的认知梯度。最宽泛的定义是,在研发过程中的任何一个环节,哪怕仅仅是文献调研阶段使用了AI工具,都可被贴上AI药物的标签。而最严苛的定义则要求,该药物的关键发现——无论是全新靶点的提出,还是全新分子结构的生成——必须由人工智能算法主导,而非人类专家的直觉经验。
在2025年下半年至2026年初,随着英矽智能(Insilico Medicine)的ISM8969获得美国FDA的IND(临床试验申请)批准,以及德睿智药(Dorophy)的MDR-001启动III期临床试验,关于“第一”的定义开始分化出两条清晰的赛道。一条赛道比拼的是“从0到1”的原创思想,即AI能否发现人类未曾设想的路径;另一条赛道争夺的则是“从1到N”的商业化终点,即谁能第一个抵达药店货架。从药物研发的科学本质出发,我们更倾向于关注那些全程或关键节点由AI深度驱动的项目,但也不得不承认,对于患者而言,真正具有里程碑意义的时刻,是有一瓶药真实地握在手中。因此,我们的调研将覆盖从临床后期到注册批件的多个维度,试图还原这场多维竞赛的真实图景。
中国速度:MDR-001的III期冲锋
在上市倒计时的读秒声中,来自中国杭州的一支四十多人的团队,正以惊人的速度改写着全球减重药物的版图。德睿智药研发的口服减重新药MDR-001,作为中国首款进入III期临床试验的AI设计药物,无疑是最靠近上市终点线的选手之一。
MDR-001属于当下最为炙手可热的GLP-1受体激动剂赛道,但其差异化的价值在于“口服”与“小分子”。与目前市场上主流的司美格鲁肽等多肽类药物不同,MDR-001是一种化学小分子,这意味着它在生产成本、储存便利性以及患者依从性(口服而非注射)方面具备理论上的巨大优势。然而,小分子GLP-1的研发壁垒极高,如何在口服的生物利用度和疗效之间找到平衡,曾是困扰业界多年的难题。

源头创新:英矽智能的靶点突破与临床验证

NLRP3炎症小体是当前炎症及免疫领域的明星靶点,其过度激活与多种疾病相关。然而,开发一个既能有效抑制NLRP3,又能穿透血脑屏障直达中枢神经系统的药物,难度极高。ISM8969的突破性在于,它通过英矽智能的生成式化学引擎Chemistry42,成功设计出了具有理想血脑屏障穿透特性的分子结构。在临床前研究中,它展现出了优越的药效、选择性和安全性,这正是AI在复杂化学空间中高效导航能力的体现。
英矽智能的实践,验证了生成式AI在药物研发中的完整闭环。从最初的靶点发现(利用PandaOmics平台),到分子生成与优化(利用Chemistry42),再到临床试验设计,AI贯穿始终。更值得关注的是其商业模式与平台价值的双重验证。除了自研管线,英矽智能通过向制药巨头授权其平台和管线,实现了技术价值的变现。2026年初,其与齐鲁制药达成的战略合作,聚焦于心血管代谢疾病的小分子抑制剂开发,合同总价值接近1.2亿美元。这表明,大型药企不仅认可AI发现的分子,更愿意为AI平台本身的持续产出能力付费。
此外,英矽智能最领先的资产Rentosertib(用于治疗肺纤维化)已在2025年6月登上《自然·医学》,其IIa期临床结果不仅验证了AI发现的全新靶点(TNIK)在人体中的可行性,更标志着AI驱动的药物发现已经从概念验证走向了临床疗效的实证阶段。虽然Rentosertib的上市进程可能稍晚于MDR-001,但它在科学探索上的“含金量”无疑更高,代表了AI拓展人类认知边界的可能性。
技术与资本的共舞:Exscientia与Recursion的平台化叙事
除了上述两家直接冲刺上市的药物,还有一类AI制药公司构成了行业的“基础设施”,它们未必亲自将药物推到上市,但其平台能力正在通过一个个里程碑得到验证。英国的Exscientia和美国的Recursion,正是这一维度的典型代表。
Exscientia在2021年8月宣布,百时美施贵宝(BMS)行使了对一款免疫调节药物的选择权,为此支付了2000万美元的期权费。这款未披露具体信息的候选药物针对的是一个传统方法极难成药的免疫激酶靶点,而Exscientia仅用了11个月就完成了从药物设计到候选分子筛选的全过程。这不仅是Exscientia与BMS两年合作的第一个产出成果,更是对其AI平台高效解决复杂化学问题能力的强力背书。在此之前,Exscientia还通过EXALT-1研究展示了其在精准医学维度的布局。这项发表在《Cancer Discovery》上的研究显示,利用其单细胞功能精准医学平台,可以为晚期血液癌症患者推荐更优的治疗方案,使54%的患者获得了超过1.3倍的无进展生存期获益。这意味着AI不仅在设计分子,更在优化治疗决策。
而Recursion则走了一条更为“重资产”的工业化道路。通过其庞大的湿实验室自动化系统和递归操作系统(Recursion OS),该公司正在构建高通量的生物数据工厂。在2026年初的摩根大通医疗健康大会上,Recursion披露了其财务状况和平台进展:手握7.55亿美元现金,足以支撑运营至2027年底;其管线中已有约5个 wholly owned 临床项目和15个发现阶段资产,并与罗氏、赛诺菲、基因泰克等巨头建立了合作。Recursion的核心逻辑在于,通过大规模、标准化的实验数据喂养AI模型,让模型更好地理解生物学,从而反向设计更优的分子。
Exscientia和Recursion的模式揭示了一个更深层的行业趋势:AI制药的竞争,正从单一算法的比拼,进化为“算法-数据-自动化”三位一体的平台能力较量。谁能更快、更准地生成高质量的反馈数据,让AI模型持续进化,谁就能在长跑中建立难以逾越的护城河。
冰山融化时:传统药企的AI求生与行业重塑
当AI制药公司在聚光灯下攻城略地时,传统的大型制药企业正在经历一场深刻的生存焦虑。正如业内评论所言,2025年秋至2026年初,AI制药风暴以超预期的速度席卷全球,传统研发的“冰山”正在以前所未有的速度融化。
这座冰山由三层坚冰构成:第一层是高成本、低效率的“试错炼狱”,平均耗时超10年、耗资超10亿美元的模式难以为继;第二层是部门林立的僵化组织,计算化学长期被边缘化;第三层是同质化竞争的“创新枯竭”,扎堆PD-1等热门靶点导致大量资源浪费。
面对AI带来的“高温”,传统药企的应对策略正在从“要不要用AI”的观望,转向“如何用好AI”的实操。我们看到,诺和诺德联手Deep Apple,礼来投资Juvena,阿斯利康引入石药集团的AI平台,赛诺菲与Formation Bio深度合作。这些百亿美元级别的资本涌动和战略合作,标志着AI已被视为驱动下一代疗法的核心战略资产,而非锦上添花的工具。
在这场自救与重塑中,一条清晰的转型路径正在浮现。首先是数据资产化,将数十年积累的“暗数据”——失败的临床试验、未被发表的化合物活性——转化为AI可理解的“知识金矿”。其次是组织革新,建立跨学科的“人机共生”团队,例如礼来与英伟达共建的AI实验室,让生物学家的经验与工程师的算力深度融合。最后是战略升维,从聚焦单个明星药物的“自己捕鱼”,转向构建开放创新平台的“运营渔港”,通过外部合作与内部转化并举,形成创新生态。
结语:混沌中的曙光
站在2026年的中点回望,关于“第一个AI药物”的归属,依然充满悬念。可能是德睿智药的MDR-001,以减重药物巨大的市场潜力率先撞线;可能是英矽智能的ISM8969,以神经退行性疾病的突破性疗法名垂青史;也可能是一匹尚未被广泛关注的黑马,在肿瘤或罕见病领域异军突起。
但比“第一”归属更重要的是,我们已然见证了历史。这些进入临床后期或获得关键监管批准的AI药物,无论哪一个最终率先上市,都将共同宣告一个旧时代的终结和一个新时代的开启。它们证明了人工智能不再是制药行业的“玩具”,而是能够真正创造出具备优异疗效与安全性、并进入人体进行大规模验证的“工具”。对于饱受低效率和高成本困扰的生物医药产业而言,这正是冰川消融后,照进裂缝的第一缕曙光。对于科学家而言,未来的挑战不再是争论AI能否制药,而是如何驾驭这股力量,去攻克那些曾经被视为不可能的人类疾病。
主要参考资料
1.Rethinking Nature’s Pharmacy: AI Era and Natural Product Drug Discovery
2. 德睿智药官网信息
3. 英矽智能官网信息
4智慧芽:人工智能赋能:口服小分子GLP-1首度进入III期临床试验
5. 環球生技月刊:Exscientia鎖定難以成藥標靶免疫調節AI新藥獲BMS授權2千萬美元入袋
6. 药事纵横冰山融化时:传统药企的AI诺亚方舟何在?


