两款亿级仿制药同日获批,国产替代的春天还有多远?
发布时间:2026-05-06来源:药事纵横
近日,华海药业两款仿制药同日获批上市,引发行业关注。然而,更值得深思的是:两个年销合计超4亿元的品种,原研厂家仍分别占据六成乃至八成以上的市场份额。国产仿制药企扎堆申报、低价厮杀,却迟迟难以撼动原研地。一、热闹的“抢仿”背后,原研依旧“稳坐钓鱼台”
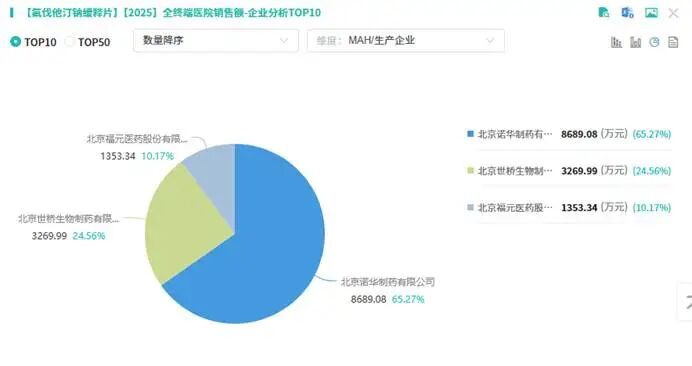
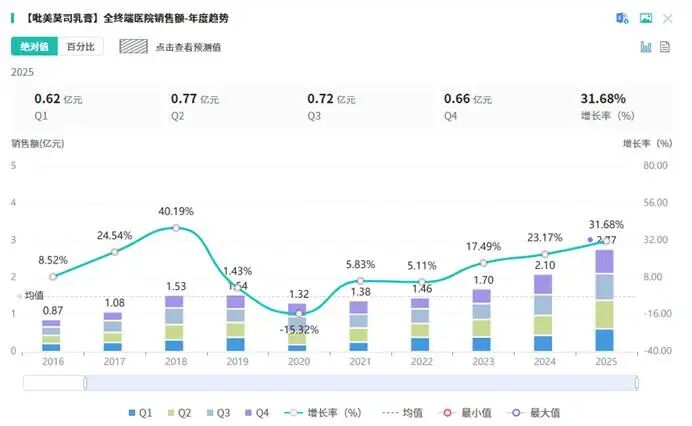
仿制药的核心价值的是通过高质量仿制,降低用药成本、提升药物可及性,推动原研药的市场替代,这也是国家推动仿制药发展的核心初衷。但从当前市场格局来看,即便多款仿制药获批过评、扎堆入局,原研药的市场主导地位依然难以撼动,“抢仿”的热闹与原研的坚挺形成鲜明对比,这一点在华海药业此次获批的两款品种上体现得淋漓尽致。先看氟伐他汀钠缓释片,该品种最早由诺华公司研发,2000年在美国上市,2009年进入中国市场,主要用于治疗饮食未能完全控制的原发性高胆固醇血症和混合型血脂异常,是心血管领域的常用药物。摩熵医药数据显示,2025年该品种全终端医院市场销售额达1.3亿元,而原研厂家北京诺华制药占据了超65.27%的市场份额,稳居院内榜首,几乎占据了三分之二的市场。图源:摩熵医药数据库从获批格局来看,氟伐他汀钠缓释片的“抢仿”竞争早已白热化。早在2021年,北京世桥生物制药就拿下了该品种的国内首仿+首家过评,率先切入市场;随着华海药业此次获批,目前国内已有6家药企的该品种获批并通过一致性评价,形成了多家企业同台竞争的格局。但即便如此,国产仿制药的市场份额合计不足35%,也就是说,超过六成的市场依然被原研诺华牢牢掌握。另一款品种吡美莫司乳膏的市场格局更为悬殊。该品种同样由诺华研发,2001年在美国上市,2003年进入中国,适用于无免疫受损的3个月及以上轻度至中度特应性皮炎患者,目前已纳入国家医保乙类目录,市场需求持续增长。摩熵医药数据显示,该品种近三年销售额增速亮眼,2024年超2亿元,同比增长23.17%;2025年进一步攀升至超2.7亿元,同比增长31.68%,展现出强劲的市场增长潜力。图源:摩熵医药数据库但与氟伐他汀钠缓释片类似,吡美莫司乳膏的市场主导权依然在原研诺华手中,其独占超80%的市场份额,意味着国产仿制药合计占比不足20%。从获批情况来看,江苏知原药业于2022年11月拿下该品种的国内首仿+首家过评,截至目前,包括华海药业在内,已有6家药企获批并视同通过一致性评价,但这些国产仿制药始终难以突破原研的市场壁垒,未能实现预期中的市场洗牌。这种“仿制药扎堆、原研独大”的格局,并非个例,而是当前国产仿制药行业的普遍现状。无论是心血管领域的血脂调节剂,还是皮肤科领域的外用制剂,即便仿制药通过一致性评价,在质量和疗效上与原研药实现等效,也依然难以撼动原研药的市场地位。热闹的“抢仿”背后,是国产仿制药面临的市场困境——获批不等于占领市场,过评不等于实现替代,原研药依旧“稳坐钓鱼台”。二、超10家排队、研发投入不足千万,仿制药“内卷”何去何从?
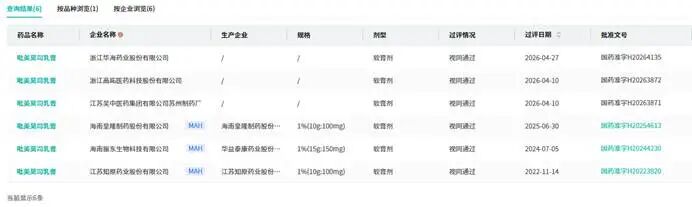
华海药业两款仿制药的获批,不仅折射出原研药的市场强势,更暴露了国产仿制药行业“内卷”加剧的现状。从申报格局来看,两款品种的排队审批企业数量众多,低门槛导致的扎堆申报现象突出,而有限的研发投入、狭窄的利润空间,进一步让仿制药行业陷入“内卷”困境,未来发展方向引人深思。目前氟伐他汀钠缓释片除了已获批的6家企业外,还有超10家药企提交了4类仿制药上市申请,正处于审评审批中;吡美莫司乳膏的竞争更为激烈,除已获批的6家企业外,湖南九典制药、上海现代制药、福元药业等12家药企也已提交申报,正在排队等待审批。这意味着,未来两年内,这两个品种的市场竞争将进一步加剧,更多企业的入局,将让本就拥挤的市场雪上加霜。图源:过评药品汇总数据库扎堆申报的背后,是仿制药研发的低门槛。从研发投入来看,华海药业在这两个项目上的投入分别为约1044万元(氟伐他汀钠缓释片)和689万元(吡美莫司乳膏),这一投入水平在国内仿制药行业中属于中等水平。相较于创新药动辄数亿元、数十亿元的研发投入,仿制药的研发成本显著更低,技术门槛相对不高,这也导致众多药企纷纷涌入仿制药领域,选择“抢仿”成熟品种,以低成本、快周期的方式获取市场份额。但低门槛带来的不仅是扎堆申报,还有难以避免的价格战。在国家集采常态化的背景下,仿制药的利润空间被急剧压缩。近年来,无论是国家组织的集中采购,还是地方联盟集采,均以“低价中选”为核心原则,仿制药的价格降幅普遍达到50%以上,部分品种降幅甚至超过90%。联环药业曾在投资者互动中表示,公司利润下滑主要受国家集采、地域联盟集采等政策影响,普通仿制药利润空间被大幅压缩,这也是国内仿制药企业的普遍困境。对于众多仿制药企业而言,若仅依靠“抢仿+低价”的策略,短期内或许能获得一定的市场份额,但长期来看,难以支撑企业的持续发展和创新投入。一方面,价格战导致企业利润微薄,无法投入更多资金用于研发升级、质量提升;另一方面,即便仿制药价格低廉,也依然面临多重市场壁垒,难以实现对原研药的替代。这些壁垒主要体现在三个方面:一是医院准入壁垒,原研药凭借长期的临床应用积累,已进入多数医院的采购目录,而仿制药要进入医院,需经过复杂的准入流程,耗时耗力;二是医生处方习惯壁垒,医生长期使用原研药,对其疗效和安全性更为熟悉和信任,即便仿制药通过一致性评价,也难以快速改变医生的处方习惯;三是患者品牌认知壁垒,部分患者仍存在“原研药比仿制药好”的刻板印象,即便仿制药价格更低,也更倾向于选择原研药。这些壁垒的存在,使得原研产品即便专利到期,依然能维持较高的市场份额,也让仿制药的“内卷”陷入恶性循环。三、从“仿制”到“替代”,国产药企还需要补什么课?
国产仿制药的核心目标,是实现对原研药的市场替代,让更多患者用得上、用得起高质量的药品。但从当前的行业现状来看,从“仿制”到“替代”,还有很长的路要走。华海药业今年以来已有7个品种获批并过评,显示出较强的仿制药申报能力,但这些品种多为成熟仿制药,缺乏差异化布局,也折射出国内仿制药企业的普遍短板。要实现真正的国产替代,国产药企还需要补齐多方面的“课程”。首先,要打破“重仿制、轻证据”的误区,补齐学术证据积累的短板。国产替代缓慢的核心原因之一,并非仿制药质量不足,而是原研药在长期的临床应用中,积累了大量的学术证据和临床数据,形成了深厚的学术壁垒。经过多年改革,我国仿制药质量和疗效一致性评价深入推进,药品监管体系日趋完善,审评标准全面与国际接轨,通过一致性评价的仿制药,在质量和疗效上已与原研药无显著差异,大量真实世界研究也证实了这一点。但国产仿制药企业往往忽视学术推广和临床数据积累,缺乏对仿制药临床价值的深度挖掘,导致医生和患者对其疗效稳定性的认可不足,难以实现临床替代。其次,要摆脱“扎堆抢仿”的内卷困境,补齐差异化布局的短板。当前,国内仿制药企业的研发布局高度同质化,大多聚焦于临床常用、技术门槛低、市场规模大的成熟品种,导致“千军万马过独木桥”的局面。华海药业此次获批的两款品种,以及排队申报的企业,均体现了这一问题。这种同质化布局,不仅导致价格战加剧、利润空间压缩,还难以形成企业的核心竞争力。未来,仿制药企业需要跳出“抢仿”思维,结合自身优势,聚焦细分领域,开展差异化布局,例如聚焦复杂制剂、儿童用药、罕见病用药等领域,避开同质化竞争,打造特色产品。再次,要突破“低价竞争”的局限,补齐品牌建设的短板。长期以来,国产仿制药的核心竞争力集中在价格上,但价格优势并非长久之计。原研药的高市场份额,不仅源于其学术积累,还源于其强大的品牌影响力——原研药企业通过长期的品牌建设,形成了较高的品牌信任度,而国产仿制药企业往往忽视品牌建设,导致患者和医生对其品牌认知度低。事实上,国产仿制药与原研药的差异,并非质量差距,而是结构与定位不同:原研药价格中包含高额创新成本、市场推广成本和品牌溢价,而仿制药专注于高质量仿制与普惠供给,两者的核心价值不同。国产药企需要加强品牌建设,通过提升产品质量、开展学术推广、积累真实世界数据,提升品牌信任度,摆脱“低价低质”的标签。最后,要明确发展方向,补齐创新转型的短板。对于仿制药企业而言,单纯比拼“首仿”数量和“过评”品种,难以真正撼动原研药的市场格局,也难以实现长期可持续发展。未来,仿制药企业的出路主要有两条:一是规模化、成本极致化,依托多品种布局,实现规模效应,通过精细化管理降低生产成本,在集采中占据优势,如华海药业、齐鲁制药、正大天晴等头部仿制药企业,已逐步形成多品种规模优势;二是向改良型新药、高端制剂转型,在仿制的基础上进行技术创新,优化制剂工艺、提升药物疗效、改善患者依从性,实现从“仿制”到“创新”的跨越,打破原研药的技术壁垒,形成自身的核心竞争力。结语
两款亿级品种同日获批,固然是企业的好消息,但远未到国产替代的拐点。数十家药企挤在同一条仿制药赛道上,低价、低利润、低市场占有率的“三低”困局亟待破解。唯有从“能仿”走向“仿优”,甚至向创新转型,国产药企才能真正从原研手中分得一杯羹。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。