从糖尿病到渐冻症,TIDES在崛起
发布时间:2026-05-06来源:药事纵横
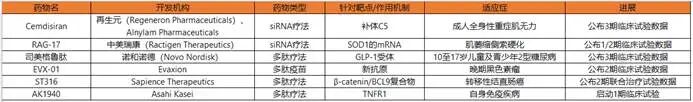
近年来,多肽与寡核苷酸(TIDES)药物正以惊人的速度进入临床核心舞台。从儿童糖尿病到重症肌无力,从结直肠癌到渐冻症,这一领域的最新临床数据不仅刷新了疗效预期,更在重新定义“难治”二字的边界。一、口服GLP-1的下一站:儿科2型糖尿病的破局者
近年来,儿童及青少年2型糖尿病的发病率呈逐年上升趋势,成为全球儿科内分泌领域的重大挑战。相较于成人2型糖尿病,青少年患者的治疗更具特殊性,既要有效控制血糖,又要兼顾生长发育需求,而传统治疗方案长期面临诸多困境,直到口服司美格鲁肽的出现,才为这一群体带来了破局之机。2026年,诺和诺德公布了口服司美格鲁肽3a期临床试验PIONEER TEENS的积极顶线结果,这是首项在10至17岁儿童及青少年2型糖尿病患者中评估口服GLP-1受体激动剂疗法的临床试验,为口服司美格鲁肽的儿科适应症拓展奠定了坚实基础。该研究采用随机、安慰剂对照设计,聚焦口服司美格鲁肽在青少年患者中的疗效与安全性,结果显示,与安慰剂相比,口服司美格鲁肽在降低糖化血红蛋白(HbA1c)方面达到优效终点,在治疗26周时,较安慰剂实现统计学显著且更优的血糖改善,HbA1c降幅优势达到0.83个百分点,展现出优异的血糖控制能力。安全性方面,口服司美格鲁肽展现出良好的耐受性,其安全性特征与此前司美格鲁肽在成人患者中的临床研究结果一致,未出现新增或意外的不良事件,主要不良反应为轻度胃肠道反应,且多为一过性,不影响治疗继续进行,这一特点对于需要长期治疗的青少年患者而言至关重要。基于这一积极结果,诺和诺德表示,预计将在2026年下半年向美国及欧盟监管机构递交Ozempic及Rybelsus(口服司美格鲁肽)的适应症扩展申请,有望成为首个获批用于10-17岁儿童及青少年2型糖尿病的口服GLP-1受体激动剂。要理解口服司美格鲁肽的临床价值,需先正视儿童及青少年2型糖尿病治疗的历史困境。长期以来,该群体的治疗药物选择极为有限,临床主要依赖胰岛素注射和少量口服降糖药,存在三大核心痛点:一是药物适配性不足,多数口服降糖药未在青少年群体中开展充分的临床试验,缺乏明确的安全性和有效性数据,临床应用存在盲目性;二是患者依从性差,胰岛素注射需长期规律操作,对于青少年而言,不仅痛苦且影响正常学习生活,部分患者因抵触注射而擅自停药、减药,导致血糖控制不佳;三是缺乏便捷的口服剂型,此前GLP-1类药物均为注射剂型,虽疗效明确,但给药不便的问题进一步降低了患者依从性,难以实现长期规范治疗。口服司美格鲁肽的出现,不仅破解了上述困境,更带来了代谢性疾病管理理念的革新。从技术层面来看,口服司美格鲁肽的成功并非简单的剂型改良,而是制剂技术的重大突破——通过优化药物递送系统,解决了多肽药物口服生物利用度低、易被胃肠道酶降解的难题,实现了GLP-1受体激动剂从注射到口服的跨越。这种剂型突破,不仅提升了患者依从性,更推动代谢性疾病管理向更早期、更便捷、更精准的方向演进。深层来看,口服司美格鲁肽在儿科领域的突破,意味着代谢性疾病的干预正逐步向青少年群体延伸,打破了“青少年糖尿病以生活方式干预为主”的传统认知,为早期控制血糖、延缓并发症发生提供了全新手段。若未来顺利获批,口服司美格鲁肽将填补儿科2型糖尿病口服GLP-1治疗的市场空白,成为该领域的标准治疗方案之一,同时也将推动更多企业布局儿科代谢性疾病的口服多肽药物研发,进一步丰富治疗选择,改善青少年患者的长期预后。二、沉默补体,重启希望
siRNA(小干扰RNA)疗法作为TIDES领域的另一大核心分支,凭借其“精准沉默致病基因、长效调控”的独特优势,正逐步打破自身免疫性疾病、神经退行性疾病等难治性疾病的治疗僵局。2026年以来,cemdisiran(重症肌无力)、RAG-17(ALS)两款siRNA疗法的积极临床数据,进一步印证了siRNA技术在复杂疾病领域的巨大潜力,也标志着RNA干扰技术正从罕见病向更广泛的治疗领域延伸。在自身免疫性疾病领域,再生元与Alnylam Pharmaceuticals联合开发的cemdisiran,成为首个向FDA递交监管申请的重症肌无力siRNA疗法,为全身性重症肌无力(gMG)患者带来了全新希望。cemdisiran是一种皮下注射、靶向C5补体的siRNA疗法,其作用机制是通过特异性沉默C5补体基因的mRNA表达,抑制C5补体的活化,从而阻断补体介导的免疫损伤,缓解重症肌无力患者的肌肉无力症状——这一机制精准针对gMG的核心发病环节,相较于传统免疫抑制剂,具有靶向性更强、副作用更小的优势。其3期临床试验NIMBLE的积极结果,为其上市提供了坚实支撑。该研究显示,cemdisiran达到了主要终点和关键次要终点,与安慰剂相比,每12周接受一次cemdisiran治疗的患者,在两项关键评估量表上均表现出显著且具有临床意义的改善。主要终点方面,cemdisiran组在重症肌无力日常生活活动(MG-ADL)评分上较基线平均改善4.5分,较安慰剂组实现2.3分的改善(p<0.001),其中76.6%的cemdisiran组患者改善≥3分,而安慰剂组的这一比例仅为44.1%;关键次要终点方面,在定量重症肌无力(QMG)评分上,cemdisiran组较基线改善4.2分,较安慰剂组实现2.8分的改善(p=0.002)。值得注意的是,这些改善在治疗2周内即已显现,并持续改善至第24周,且安全性良好,大多数不良事件为轻至中度,展现出长效、安全的治疗优势。在神经退行性疾病领域,中美瑞康的siRNA疗法RAG-17在ALS治疗中取得了突破性进展,为这一“渐冻症”带来了新的治疗可能。ALS是一种进展迅速、预后极差的神经退行性疾病,其中SOD1基因突变是家族性ALS的已知病因之一,突变后的SOD1蛋白会产生毒性,导致运动神经元损伤,最终导致患者瘫痪、死亡。RAG-17的核心作用机制,是通过特异性靶向并沉默SOD1基因的mRNA,减少有毒SOD1突变蛋白的产生,从而减缓或阻止SOD1-ALS的疾病进展。相较于传统疗法,RAG-17的核心优势在于其独特的递送技术——依托中美瑞康专有的智能化学辅助递送(SCAD)技术,将siRNA双链结合至辅助寡核苷酸(ACO),通过单次鞘内注射即可实现药物在中枢神经系统的广泛分布和持久的靶点结合,解决了传统siRNA药物难以穿透血脑屏障、在中枢神经系统递送效率低的难题,让药物“走得更远、钻得更深”,药效维持时间更长久。其1期临床试验结果显示,单次给药后,患者脑脊液中的SOD1突变蛋白实现了快速且持久的降低,在150 mg剂量组中,第90天时达到最大降幅58.1%,并在第210天仍维持具有临床意义的显著降低。作为神经退行性疾病的关键生物标志物,血浆神经丝轻链(NfL)的水平变化直接反映神经损伤程度,RAG-17治疗后,患者的NfL水平呈现明显下降趋势,在180 mg剂量组中,第150天时患者的NfL水平较基线降低了81.2%,提示药物能够有效抑制神经损伤。此外,临床评估也显示出令人鼓舞的稳定趋势,在180 mg剂量组中,部分患者的ALS功能评分量表修订版(ALSFRS-R)评估在长达150天的观察期内降幅极小或无下降,表明疾病进展可能得到延缓。安全性方面,RAG-17在所有剂量组中均表现出良好的安全性和耐受性,未发生严重不良事件或3级治疗伴发不良事件,为其后续临床推进奠定了基础。深入分析来看,cemdisiran与RAG-17的积极进展,彰显了siRNA疗法的共同优势:一是靶向精准,能够特异性沉默致病基因,实现“精准打击”,避免对正常细胞的损伤,解决了传统药物“杀敌一千、自损八百”的痛点;二是长效便捷,两款药物均实现了长效给药,cemdisiran每12周给药一次,RAG-17单次给药即可维持长期疗效,大幅降低了患者的给药频率,提升了依从性;三是可调控基因表达,能够从疾病根源上阻断致病过程,而非单纯缓解症状,为难治性疾病提供了“根治性”治疗的可能。更重要的是,这些疗法的突破具有里程碑意义:cemdisiran若顺利获批,将成为首个用于gMG的siRNA药物,填补该领域的治疗空白;RAG-17则为SOD1-ALS患者提供了首个针对性的基因沉默疗法,打破了ALS治疗“无特效药”的困境。从更广阔的行业视角来看,这也标志着RNA干扰技术正从罕见病领域走向更广泛的免疫和神经适应症,未来有望在类风湿关节炎、多发性硬化症、阿尔茨海默病等更多难治性疾病中实现突破,重塑相关疾病的治疗格局。三、多肽靶向Wnt通路:ST316在转移性结直肠癌中的黑马表现
转移性结直肠癌(mCRC)是全球高发的恶性肿瘤之一,其治疗长期面临“疗效有限、耐药性突出”的困境,尤其是对于二线及以上治疗的患者,传统化疗、靶向治疗的疗效已进入瓶颈期。而Sapience Therapeutics公司的在研多肽疗法ST316,凭借其独特的作用机制和优异的临床数据,成为mCRC治疗领域的一匹黑马,也为多肽药物在复杂肿瘤信号网络中的应用开辟了新路径。ST316的核心创新之处,在于其精准靶向Wnt/β-连环蛋白信号通路的作用机制。Wnt信号通路是调控细胞增殖、分化、凋亡的关键通路,在结直肠癌等多种肿瘤的发生、发展中发挥着核心作用——该通路异常激活会导致肿瘤细胞无限增殖、侵袭和转移,是结直肠癌发生的重要驱动因素。但长期以来,Wnt通路一直被视为“难成药”靶点,核心原因在于其信号网络复杂,靶点蛋白多为胞内蛋白,传统小分子药物难以穿透细胞膜实现精准结合,且易产生脱靶效应,导致药物疗效不佳、毒性较大。而ST316作为一款潜在“first-in-class”β连环蛋白(β-catenin)多肽拮抗剂,成功破解了这一难题。其作用机制是通过特异性结合β连环蛋白,破坏β连环蛋白与BCL9的相互作用,从而抑制Wnt/β-连环蛋白信号通路的异常激活,阻断肿瘤细胞的增殖和转移。与传统小分子药物相比,ST316具有更高的靶向性和特异性,能够精准作用于肿瘤细胞内的致病靶点,同时对正常细胞影响有限,展现出优异的治疗窗口。2026年4月公布的2期剂量扩展研究数据,充分彰显了ST316的临床潜力。截至2026年4月13日,该研究共纳入15名接受ST316联用标准疗法(FOLFIRI+bevacizumab)作为二线治疗的mCRC患者,根据RECIST 1.1标准评估,其确认的客观缓解率(ORR)达47%,其中7名患者达到部分缓解(PR),疾病控制率(DCR)高达93%。这一数据显著优于同类疗法的历史研究数据——传统二线治疗方案的ORR仅为5%-23%,ST316的加入,让mCRC患者的缓解率实现了翻倍提升,展现出强大的肿瘤杀伤能力。ST316的疗效具有广谱性,在不同分子特征的患者中均能展现出良好的治疗效果。研究显示,无论是RAS突变、RAS野生型患者,还是伴有肝转移的患者,均能从ST316联合治疗中获得缓解,这一特点解决了传统靶向药物“仅适用于特定分子亚型患者”的局限,扩大了适用人群,为更多mCRC患者提供了治疗希望。例如,RAS突变型结直肠癌患者约占所有结直肠癌患者的50%以上,这类患者对传统靶向治疗不敏感,治疗选择极为有限,而ST316在这类患者中的有效缓解,无疑为其带来了新的生机。安全性方面,ST316同样展现出显著优势。在1期剂量递增研究中,ST316单药治疗表现出良好的耐受性,未观察到剂量限制性毒性(DLT)或相关的严重不良事件(SAE),其不良反应主要为轻度胃肠道反应和乏力,且可通过对症处理缓解,不影响治疗继续进行。这一安全性特征,与多肽药物的固有优势密切相关——多肽药物多为天然蛋白片段,与人体自身蛋白结构相似,免疫原性低,脱靶效应小,相较于传统化疗药物和小分子靶向药物,具有更高的安全性和耐受性。TIDES药物正从实验室的“潜力股”成长为临床的“实力派”。无论是口服多肽的便捷性,还是siRNA的持久沉默能力,它们都在回应同一个核心命题:如何以更智能的方式干预疾病本源。未来五年,随着更多监管获批与适应症拓展,这一领域或将真正改写全球难治性疾病的标准治疗图谱。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。