2025中国临床试验盘点:新药占比近六成,BE试验增速亮眼!
2026年伊始,中国创新药迎来高光时刻。随着国家药监局“全链条支持创新药中国首发”政策的落地,2025年以76个创新药、76个创新医疗器械获批的“双新高”成绩画上句号。审评审批从60日迈向30日,政策红利与研发效率双重叠加,中国医药正以“新质生产力”之姿,重构全球竞争版图。
报告以CDE数据为基石,全方位、多维度剖析了2025年中国临床试验领域:从行业整体登记概况、药品类型与治疗领域分布,到靶点及品种研发格局,再到申办方与临床研究机构的竞争态势,系统拆解并展望了中国创新药的未来前景。
本文摘选自报告核心章节,聚焦2025年中国临床试验登记整体概况,从总量趋势、月度波动、结构演变到地域分布,深度解读全年临床试验领域发展全貌。
一、总量持续扩容:五年复合增长率达12.27%
放眼全球,中国临床试验的吸引力与活跃度正不可逆转地向上攀升。2021年至2025年,中国临床试验登记数量呈现出稳健的增长态势。据统计,登记总量从2021年的3279项稳步增至2025年的5210项,复合年均增长率(CAGR)达到12.27%,整体扩容态势显著。
2021-2025年中国临床试验登记数量
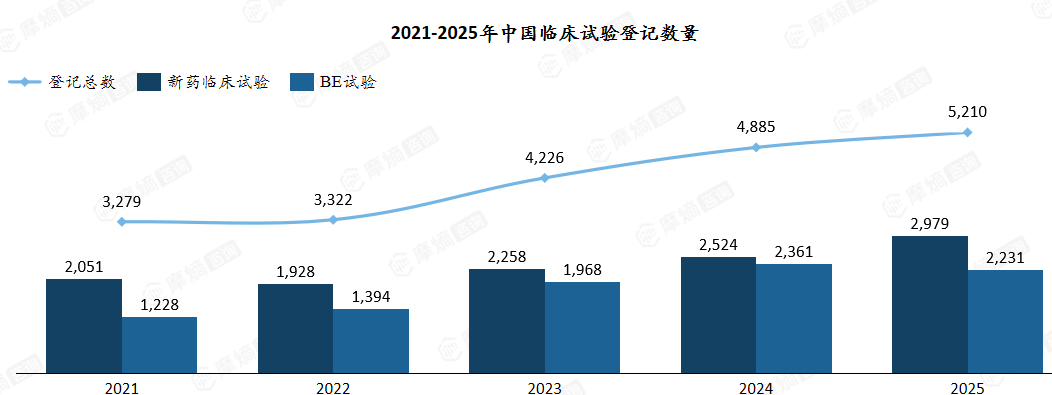
新药临床试验 作为研发创新的核心构成,数量由2021年的2051项增至2025年的2979项,复合年均增长率为9.78%。这一增速虽略低于整体水平,但其绝对规模的增长折射出我国新药研发领域的持续投入与稳步推进。
BE试验 (生物等效性试验)的增长则更为突出,从2021年的1228项增至2025年的2231项,复合年均增长率高达16.10%。这不仅折射出国内仿制药一致性评价的深化落地,更隐约透露出大批创新药企在管线布局上的务实策略——通过“仿创结合”夯实基本盘,为长期的创新投入储备弹药。
二、月度波动与季度演变:峰值与节奏各有章法
2025年中国临床试验月度登记量波动上升,新药临床试验占比逐季提升。
2025 年中国临床试验月度登记量整体呈波动上升趋势,全年总量5210项。其中,4月登记量达全年峰值535项,下半年整体活跃度高于上半年,12月登记量回升至492项,显示年末研发申报热度不减。
2025年中国临床试验登记数量 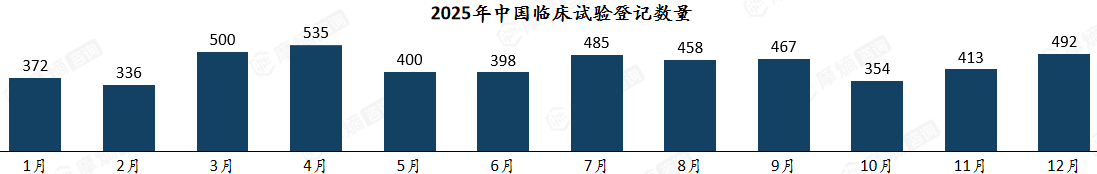
(注:登记数量以首次公示日期计,试验状态统计截止日期2025年12月31日)
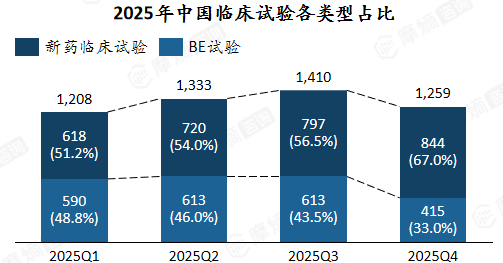
季度分布方面 ,2025年各季度试验总量先升后降,三季度为全年最高;值得注意的是,新药临床试验占比逐季提升,从一季度的51.2%上升至四季度的67%,而BE试验占比相应回落。
从项目状态看 ,2025年中国临床试验呈“高活跃、高完成、低终止”的良性特征。进行中与已完成项目合计占比超98%,主动终止/暂停项目仅占1.8%。这一状况为我国医药研发提供了良好的基础,表明临床试验活动整体运行良好。 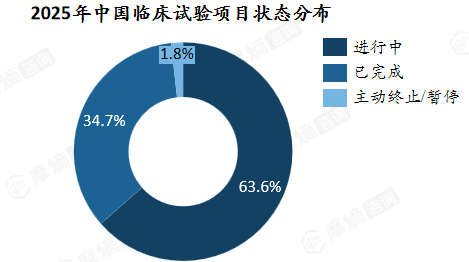
三、国内试验主导:早期研发活跃,国际参与深化
2025年中国临床试验以国内试验为主,国内试验早期研发活跃度高。
(一)国内试验占主导,早期研发热情高涨
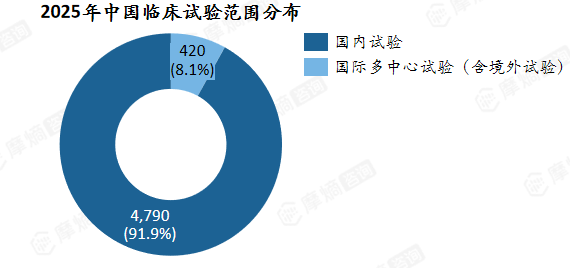
2025年中国临床试验以国内试验为主,占比高达91.9%,而国际多中心试验(含境外试验)仅占约8.1%。
在新药国内试验中,以I期、II期临床试验为主力,两者合计占比高达75.1%,表明中国在药物临床研发的早期阶段展现出极高的活跃度。 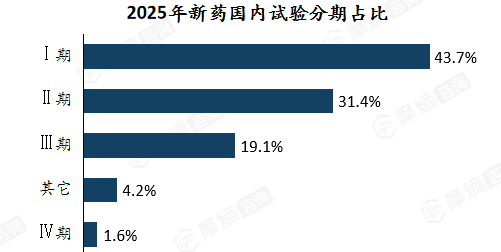
大量处于概念验证阶段的项目在国内落地推进,构成了创新药研发管线的基础环节,也标志着我国已具备承接早期创新项目大规模临床实施的产业能力。这种“早期在国内夯实基础、后期在全球验证价值”的分工模式,正在成为中国创新药研发的典型路径。
(二)国际多中心试验:聚焦后期临床,深度参与全球关键注册
与国内试验不同,新药国际多中心试验集中于后期临床,III 期占比44.7%,反映出中国正深度参与全球关键注册试验,加速融入全球新药研发体系。
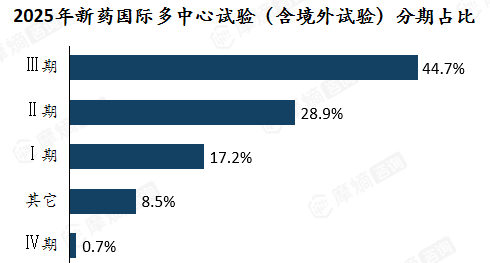
无论是作为试验的主要参与区域,还是在部分项目中扮演牵头或共同牵头的角色,中国深度嵌入全球关键注册试验的格局已然形成。正如2025年9月国家药监局所强调的,30日审评通道特别鼓励全球早期同步研发和国际多中心临床试验,服务临床急需和国家医药产业发展。可以预见,随着政策的持续赋能与本土研发能力的不断跃升,中国在全球临床试验版图中的战略地位还将进一步前移。
结语:
纵观2025年中国临床试验的整体表现,无论是规模的稳步扩张、结构的持续优化,还是效能的显著提升与全球融入的纵深推进,一幅由中国创新驱动的医药新蓝图正在徐徐展开。而要想捕捉这些宏观趋势、放大其中的微观信号,都离不开底层数据的精准支撑。
