源头创新的老大哥还是无法撼动
发布时间:2026-05-08来源:药事纵横
如果说中国创新药的十年跨越是一场以“Fast-follow”和“Me-better”为主力的追赶运动,那么美国则一直是全球FIC药物研发的引领者。理解美国的FIC创新模式——它的数据、它的生态、它的机制——对于中国而言,不仅是对标和学习,更是一次对源头创新本质的深刻审视。中国创新药的爆发是真实的,但真正的自主研发全球FIC仍然稀缺。2025年中国批准了76个创新药,但自主研发的FIC仅4个,占比约5.7%。而在同一时期,美国FDA CDER批准的46个新药中,FIC药物达20个,占比约43%。这个差距不仅仅是数字上的,更折射出两国在创新药生态上的根本性差异。今日不妨去探寻下这个核心问题:美国究竟做对了什么,使其能够持续产出从“0到1”的源头创新?1.美国FIC药物的最新数据全景
1.1 2025年FDA批准情况:FIC稳居高位
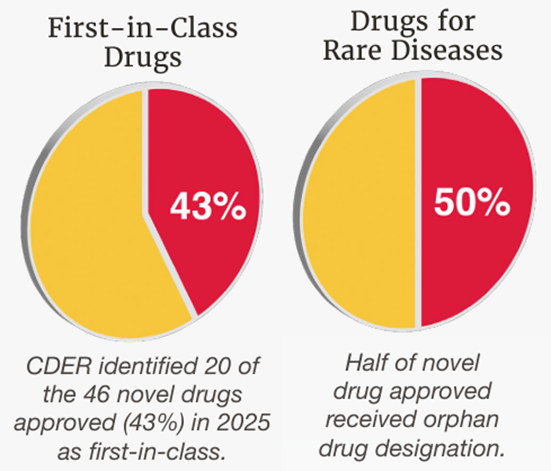
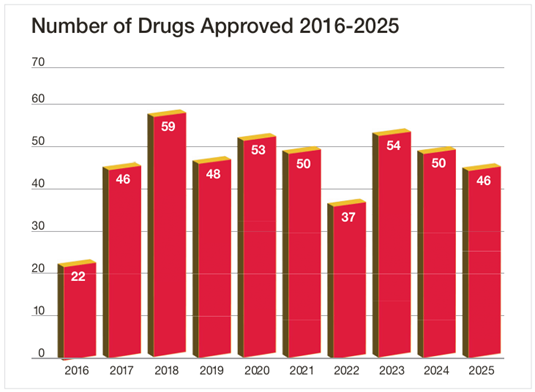
2025年是全球医药创新的一个重要年份。FDA下属药物评价与研究中心全年共批准46个新药,尽管数量较2024年的50个有所回落,但创新含量显著提升。在获批新药中,FIC药物共计20个,占比43%。超过半数获批新药通过在美国获得FDA批准实现了全球首次上市,充分体现了FDA在全球新药审评中的主导地位。在技术类型上,获批新药涵盖小分子化药、单克隆抗体、ADC、siRNA、ASO、融合蛋白和双特异性T细胞接合器等多种模态,药物类型极为丰富。值得注意的是,50%的获批新药获得孤儿药认定,显示出FIC药物与罕见病治疗之间的高度关联性——许多FIC药物最初正是从孤儿药路径获得突破。1.2历年趋势:FIC占比稳步提升
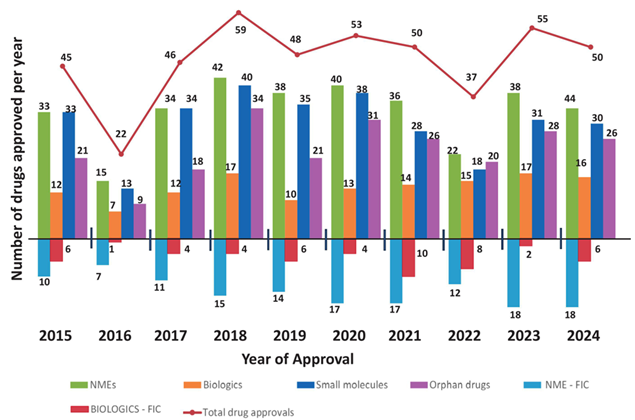
2015年至2024年间,美国FDA批准的FIC(首创新药)药物占比呈现波动上升趋势。具体来看:2015年FIC占比为36%,2016年FIC占比为36%,2017年FIC占比为33%,2018年约为32%,2019年回落至42%,2020年进一步增至40%,2021年达到十年来的峰值54%。此后,2023年FIC药物共20个,占比36%;2024年增至24个,占比40%。从2015年至2024年的十年间,FDA累计批准465个新药,其中FIC药物总体占比为37%。这一趋势传递出一个清晰的信号:美国新药研发正在从“数量驱动”转向“质量驱动”,FIC药物不再是偶然现象,而是成为美国创新药体系中的“常规产出”。1.3在研管线:赛道覆盖与FIC领先度
在更早期的在研管线层面,美国的优势同样突出。截至2024年,美国在研管线覆盖1689个赛道,覆盖度达53%,在其中的1212个赛道(占比38%)研发进度排名全球第一。全球范围内同赛道进度排名第一的药物可被认为是FIC创新药,美国在这一指标上遥遥领先。在肿瘤药物领域,美国在首创新药研发上保持全球领先,中国与美国共同驱动了全球62.7%的肿瘤药物开发,但在FIC创新方面,美国仍占据主导地位。1.4 2026年早期动态:FIC管线持续活跃
进入2026年,美国FIC管线的活跃度仍在延续。武田制药的orexin受体激动剂Oveporexton(TAK-861)作为潜在FIC疗法用于发作性睡病1型,其NDA申请已获FDA受理并授予优先审评资格。同样来自武田的rusfertide,作为一种first-in-class的铁调素模拟肽疗法,用于治疗真性红细胞增多症,其NDA也获受理并获优先审评。Praxis Medicines的relutrigine作为优先抑制持续性钠电流的首创小分子,开发用于发育性和癫痫性脑病,NDA已获FDA受理并进入优先审评。这些动态表明,美国FIC药物从早期管线到后期审批的链条运转持续保持强劲。二、美国FIC药物的成功基因
美国之所以能够成为全球FIC药物的高地,并非偶然。慷慨的支付机制、成熟的资本市场、强大的人才体系,以及高效的技术转化生态,这些因素构成了一套完整的“源头创新操作系统”。2.1基础研究与源头发现:NIH的“长周期播种”
FIC药物的根本是新靶点和新机制的发现,而这依赖于长期、稳定、高水平的基础研究投入。美国的独到之处在于建立了以NIH为核心的国家级基础研究体系。2013年,NIH启动了“照亮可成药基因组Illuminating the Druggable Genome (IDG)”项目,专门研究GPCR、离子通道和蛋白激酶这三类药物靶点家族中尚未被充分研究的蛋白质。这类前瞻性、长期性的基础研究项目,为FIC药物提供了源源不断的“弹药”。NCATS等转化科学中心则在高通量筛选和分子发现方面搭建公共平台,服务于整个学术界和产业界。许多的新生物技术公司源自NIH资助的学术研究。这意味着,NIH的每一笔基础研究经费,都可能在未来孕育出一家改变治疗格局的生物技术公司。这是一场跨越数十年的“长周期播种”,而美国正是凭借这套机制,始终站在新靶点发现的最前沿。2.2产学研转化链:从实验室到创业公司的“无缝衔接”
基础研究转化为FIC药物,需要一套高效的转化医学体系。美国的顶尖学术机构已经形成了成熟的“实验室-创业公司”转化模式。高校教职员工创办初创公司,将基础研究成果加速转化为临床疗法。这些初创公司成为FIC药物研发的“前哨阵地”——它们灵活、专注、敢于承担高风险,是验证新靶点和新机制的理想载体。与此同时,美国大型药企越来越注重内外结合的复合型创新模式,持续加强与大学和科研机构的合作,或通过并购小型生物技术公司引入外部创新。这种“小公司做早期探索、大公司做后期开发和商业化”的分工协作,形成了从科学发现到药品上市的高效流水线。波士顿、旧金山等生命科学创新集群的兴起,进一步放大了这种生态的集聚效应。2.3资本生态:长期耐心的“风险资本”
FIC研发是一场高风险、长周期的“赌博”,需要极具耐心的资本支持。美国的生物医药VC基金规模约为欧洲的两倍,处于增长阶段的公司可获得的资本量更是欧洲的八倍。这种体量上的优势,使得美国初创生物技术公司能够获得充足的“弹药”去探索前沿靶点。然而,即使在美国,风险资本也并非永无止境。2026年第一季度,美国生物技术VC支持融资轮次同比下降25.2%,创下2021年以来的最低水平。J.P. Morgan医疗健康大会也指出,生命科学和医疗健康行业的资本仍然紧张,退出路径存在不确定性。更令人担忧的是,自2025年1月以来,近800个NIH研究资助项目被终止,涉及超过20亿美元的取消资金,而约40%的新生物技术公司源自NIH资助的学术研究,这一变动正在对FIC创新的源头产生冲击。这些信号提醒我们:即便是在FIC创新最为成熟的美国,其资本生态和政策环境也并非铁板一块,而是处于动态调整和压力测试之中。2.4支付体系:为创新定价的“溢价机制”
FIC药物的高投入需要高回报来支撑。美国的支付体系为FIC创新提供了慷慨的市场回报。朱义指出,美国对FIC和BIC创新药有慷慨的支付机制,为创新提供了重要保障。孤儿药法案和突破性疗法认定等制度安排,不仅加速了FIC药物的审批,还通过市场独占期和定价优势确保了研发投入的回报。这种“高投入-高风险-高回报”的闭环,构成了美国FIC创新得以持续的商业逻辑。三、中美FIC创新模式对比
理解美国的优势,最终是为了审视中国所处的坐标。中美两国在创新药领域已呈现出“总量相当、结构迥异”的格局。3.1数量对比:总量追上,结构不同
2025年,中国在创新药批准数量上首次超越美国——中国批准了76个创新药,美国批准了46个。中国在研管线数量与临床试验数量也双双超过美国,中国年临床试验量约为7100至7700项,而美国约为6200至6300项。这是中国医药产业能力提升的有力证明。然而,在FIC药物的占比上,差距依然明显。2025年美国FDA批准的FIC药物占比约43%-48%,而中国自主研发的全球FIC药物在获批创新药中的占比仅为约5.7%。美国在首创机制与罕见病体系上的优势仍然明显。中国在健康科学和临床研究领域仍偏弱,而美国在规模、机构与人才上仍占主导。3.2模式差异:中国“快速跟进”vs美国“源头引领”
这种结构差异的本质,是两种创新模式的差异。中国的创新模式以“快速跟进”为主导——紧盯已验证靶点,通过工程优化实现差异化竞争。这一模式的优势在于周期短、风险可控、成功率高,能够快速形成产业规模。美国的创新模式则以“源头引领”为特征——不断探索新靶点、新机制,愿意承担科学上的不确定性。这一模式的优势在于能够开辟全新的治疗领域,建立知识产权壁垒,获得更高的商业回报。但它的代价是更长的研发周期、更高的失败率和更大的资金投入。两种模式没有优劣之分,而是处于不同发展阶段国家的理性选择。但当中国希望从“跟跑”迈向“并跑”乃至“领跑”时,就必须正视这一结构差距,并思考如何补上源头创新的短板。四、美国模式的可借鉴之处
其一,基础研究是源头创新的“活水”。NIH的长期稳定投入、国家级靶点发现计划、公共转化平台的建设,为FIC药物提供了源源不断的科学基础。中国需要加大对新靶点发现、基础生物学研究的长期投入,并建立从实验室到临床的顺畅转化通道。其二,产学研转化需要“专业化”的生态支撑。UCSF等机构孵化的40多家创业公司,形成了从科学发现到商业转化的完整闭环。中国需要进一步完善技术转移体系,鼓励科研人员创业,并降低初创企业的创新门槛。其三,资本需要建立对“长周期创新”的耐心。FIC研发是一场十年的马拉松,中国的医药基金周期普遍偏短,倾向投资后期项目。借鉴美国经验,中国需要发展更多专注于早期、前沿技术投资的“耐心资本”,构建覆盖研发全周期的科技金融服务体系。结语
美国的FIC药物体系不是一夜建成的。它是NIH数十年如一日的投入、是波士顿和旧金山湾区的创新生态、是敢于为高风险创新买单的资本体系、是为创新合理定价的支付机制——所有这些要素共同构建起的一套“操作系统”。这套系统并非没有裂缝——NIH资金面临削减压力、VC融资周期下行、生物科技并购不确定性增加,美国自身的FIC创新生态也正在经历考验。对于中国而言,真正的“见贤思齐”不在于简单的数字对标,而在于理解美国这套系统的底层逻辑,并思考如何构建适合自身发展阶段和制度环境的“中国式FIC创新体系”。我们走在正确的道路上,但要让源头创新的星星之火真正燎原,还需要在基础研究、转化平台和耐心资本这三个维度上持续深耕。当那一天到来时,中国医药行业才算真正从“大国”走向“强国”。参考文献
2. Novel drugs approved by the EMA, the FDA and the MHRA in 2025: A year in review3. A map of molecular drug targets and therapeutics for the US FDA-approved drugs: The impact of expedited regulatory pathways and first-in-class drug approvals on drug innovation
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。