铁死亡再登顶刊Cell:抑制铁死亡,改善器官移植效果

撰文丨王聪
编辑丨王多鱼
排版丨水成文
缺血再灌注损伤(IRI)是与心肌梗死、心血管手术、中风和器官移植相关的重大临床并发症。缺血期间氧气和营养物质的最初剥夺会破坏细胞内稳态,而随后的再灌注则通过氧化应激、免疫激活和受调控的细胞死亡加剧组织损伤。
在缺血再灌注损伤(IRI)相关的各种细胞死亡途径中,铁死亡(一种铁依赖性、脂质过氧化驱动的程序性细胞死亡方式)已成为实质损伤和长期器官功能障碍的关键促成因素。尽管越来越多的研究揭示了铁死亡在缺血再灌注损伤(IRI)中的作用,但目前尚无获批的疗法能有效靶向临床环境中的铁死亡。
器官移植是终末期器官衰竭患者的生命挽救疗法,但仍有 10%-20% 的等待移植者在获得供体器官前死亡。为扩大供体来源,移植中心越来越多地依赖高风险器官,而体外机器灌注已成为评估和改善移植器官质量的一种有前景的策略。这一灌注窗口为在植入前通过药物干预来限制铁死亡介导的损伤提供了独特的机会。
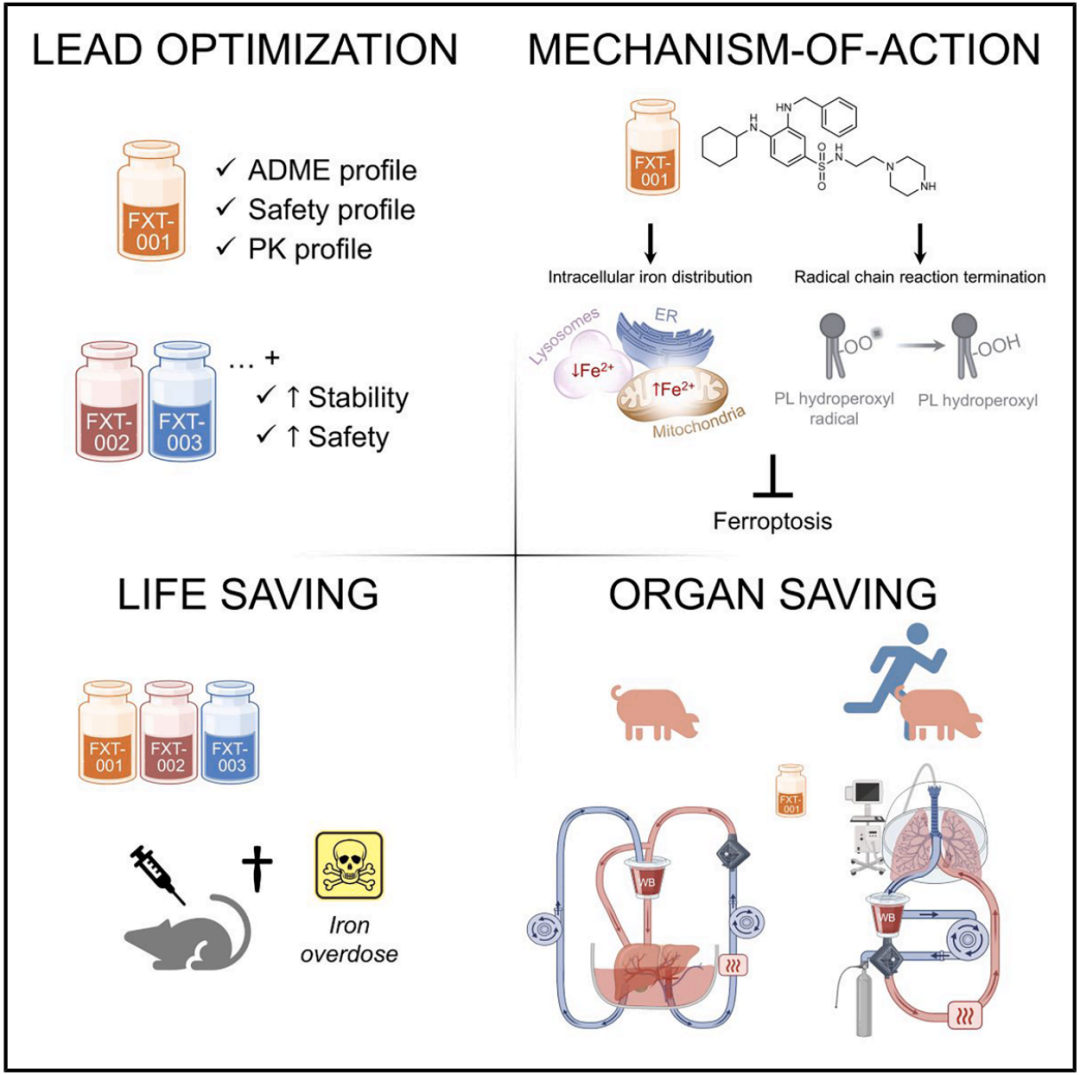
该研究发现,人体肝脏移植早期会出现短暂的脂质过氧化增加,并将其确认为治疗靶点。FXT-001 是一种具有自由基清除和铁螯合的双重作用的铁死亡抑制剂,其在包括猪的肝脏和肺移植体的离体灌注在内的临床前模型中提供了强大的保护作用。在使用已故人体供体的离体机器灌注实验中,FXT-001 治疗可保持移植物活力,而未经治疗的肺则会恶化。研究团队还开发了具有更优药代动力学和安全性特征的 FXT-002 和 FXT-003。这些发现支持将铁死亡抑制剂作为器官移植及其他缺血再灌注损伤相关病症的治疗策略。
在器官移植领域,有一个长期困扰医生的难题:缺血再灌注损伤(IRI)。当捐献者的器官被取出后,血液供应中断,细胞处于“缺氧”状态;而当器官被植入受体体内,血液重新灌注时,反而会引发更严重的组织损伤,这种矛盾现象导致了许多原本可用的器官无法使用。
什么是铁死亡?为什么它对移植器官如此致命?
铁死亡是一种铁依赖性的、由脂质过氧化驱动的程序性细胞死亡方式。细胞膜就像一层保护墙,而铁死亡就像是这堵墙被“锈蚀”的过程——过量的活性铁和氧分子在细胞膜上引发连锁反应,产生大量脂质自由基,最终导致细胞膜完整性被破坏,细胞死亡。
在器官移植过程中,缺血阶段破坏了细胞的能量和氧化还原平衡,再灌注时大量氧气涌入,就像在已经生锈的铁器上浇油,瞬间引发剧烈的脂质过氧化反应。在这项最新研究中,研究团队在人类肝移植患者中发现,脂质过氧化的标志物丙二醛在再灌注后 30 分钟就达到峰值,这与移植后肝功能损伤密切相关。
双重机制:FXT-001 如何工作?
第一代铁死亡抑制剂(例如 Fer-1)体内稳定性差以及溶解度有限,阻碍了其临床转化。FXT-001(原名 UAMC-3203)是 Fer-1 的同类最佳(best in class)类似物,具有良好的类药性,并在多种铁死亡驱动的疾病模型中展现出治疗潜力。
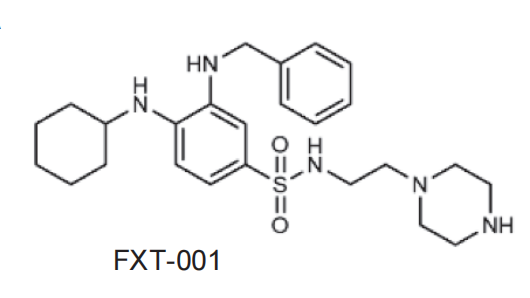
FXT-001 不是普通的抗氧化剂,它拥有独特的双重作用机制——
第一重:自由基“灭火器”,FXT-001 的分子结构包含亲脂性核心,能像锚一样嵌入细胞膜的磷脂双分子层中。一旦脂质自由基开始链式反应,FXT-001 就能在“火势蔓延”前及时扑灭,终止自由基的传播。
第二重:铁离子“调度员”,FXT-001 的邻苯二胺基团能与铁离子结合,改变细胞内铁的分布。它能够将铁从容易产生有害反应的溶酶体转移到线粒体,减少毒性铁离子的积累,从源头上遏制铁死亡的发生。
这种双重作用机制,让 FXT-001 在纳摩尔浓度下就能有效抑制铁死亡,且具有优异的药物特性:高溶解度、适中的亲脂性、良好的血浆稳定性。
动物实验:保护肝脏及肺移植物
研究团队在猪的循环死亡后捐献肝脏模型中测试了 FXT-001 的效果。这些肝脏经历了 1 小时热缺血、4 小时冷保存以及 6 小时全血再灌注,以模拟临床上的边缘供肝条件。
令人惊喜的是,通过保存液给药 FXT-001 的治疗组表现出肝损伤标志物(AST、ALT)显著降低、胆汁分泌功能更好(胆汁量与 AST 水平呈负相关)、葡萄糖代谢改善(表明对缺血最敏感的区域得到了保护)、抗炎因子 IL-10 水平升高、灌注液中脂质过氧化产物减少,更重要的是,组织学检查显示,治疗组肝细胞死亡减少。此外,在猪的离体肺灌注模型中,FXT-001 显著减少了肺组织损伤。
人体数据验证:早期预警信号
为了验证临床相关性,研究团队进一步分析了 116 例肝移植患者的血浆样本。结果发现,丙二醛水平在再灌注后 30 分钟达到峰值,高丙二醛水平与术后 6 小时 AST>2000 IU/L 显著相关(这是预测移植物衰竭的临界值),此外,在狒狒的心脏异种移植模型中也观察到类似的早期脂质过氧化高峰。
这些数据首次证实了人类器官移植早期会发生铁死亡,从而为使用 FXT-001 等铁死亡抑制剂提供了直接依据。
升级版抑制剂:FXT-002 和 FXT-003
基于 FXT-001 的成功,研究团队进一步筛选出了两个优化版本:FXT-002 和 FXT-003。这两个新一代铁死亡抑制剂保留了 FXT-001 的效力和溶解度,同时具有更高的微粒体稳定性,无磷脂质沉积症风险(阳离子两亲性药物的常见副作用),FXT-002还表现出改善的口服生物利用度。
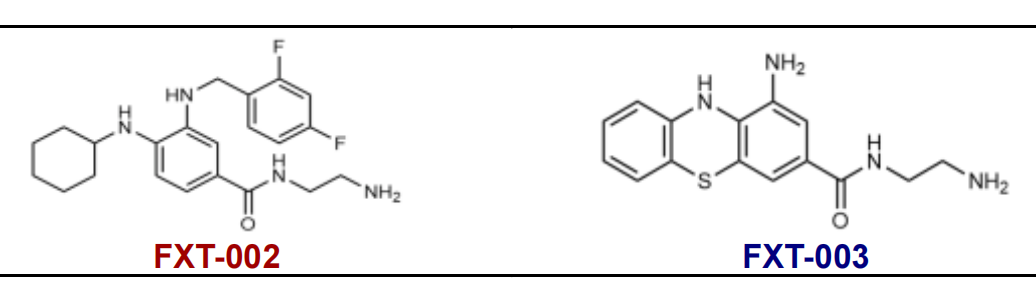
在铁过载诱导的多器官功能障碍小鼠模型中,FXT-002 和 FXT-003 与 FXT-001 疗效相当,能将小鼠存活率提高 50%-60%。
临床转化的“完美时机”:机器灌注窗口期
更重要的是,该研究还找到了理想的给药时机——器官离体机器灌注期间。随着边缘供体器官使用增加,机器灌注已成为评估和改善移植物质量的重要策略。这个灌注窗口为药物干预提供了独特机会,可以在器官植入前就抑制铁死亡介导的损伤。
研究团队在人类离体肺灌注模型中验证了这一策略。使用来自边缘供体的肺叶,FXT-001 治疗组成功保持了移植物活力,而未经治疗的肺叶则功能恶化。
这项研究虽然聚焦于器官移植,但其意义远不止于此。缺血再灌注损伤(IRI)同样发生在心肌梗死、心血管手术、中风等疾病中。通过将对铁死亡生物化学的基本认识与大型动物和人体组织模型中的临床前疗效相结合,这项工作为在广泛的缺血再灌注损伤相关疾病的治疗中靶向铁死亡奠定了基础。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00459-9





点在看,传递你的品味




