国内首个!正大天晴1类创新药上市申请获受理

晚期肿瘤患者中常见的恶性腹水,有望迎来全新的国产创新治疗方案。5月7日,中国生物制药(1177.HK)公告,核心企业正大天晴联合开发的国家1类创新药M701(CD3/EpCAM双特异性抗体)已向国家药监局药品审评中心(CDE)递交新药上市申请并获得受理,用于治疗晚期上皮性恶性肿瘤导致的恶性腹水(MA)。

截图来源:企业公告
01
国内首个自研CD3/EpCAM双抗,机制直指T细胞杀伤
M701是国内首个自主开发的CD3/EpCAM双特异性抗体,可同时靶向肿瘤细胞靶点EpCAM和免疫T细胞活化靶点CD3,通过双靶结合桥连肿瘤细胞和免疫T细胞,从而激活T细胞对肿瘤细胞进行杀伤。摩熵医药数据显示,正大天晴的注射用重组抗EpCAM和CD3人鼠嵌合双特异性抗体,2017 年2月首申临床,2022年 7 月获批临床,2024 年3月进入Ⅲ期临床(针对卵巢癌、胃癌、结直肠癌、腹水、晚期实体瘤)。
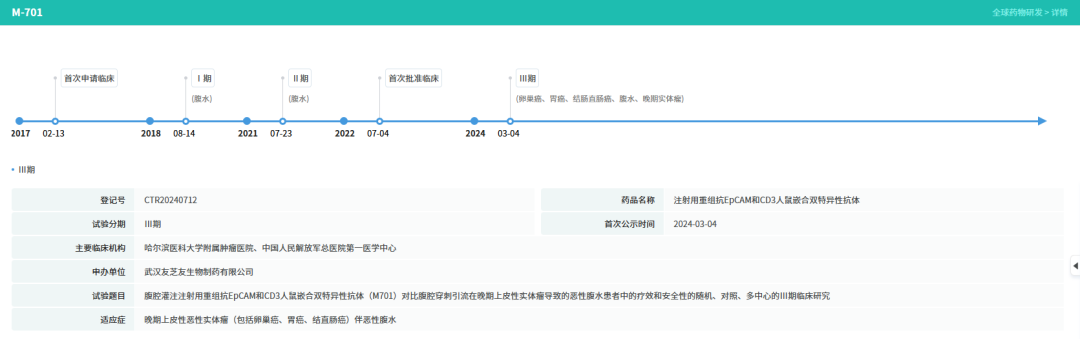
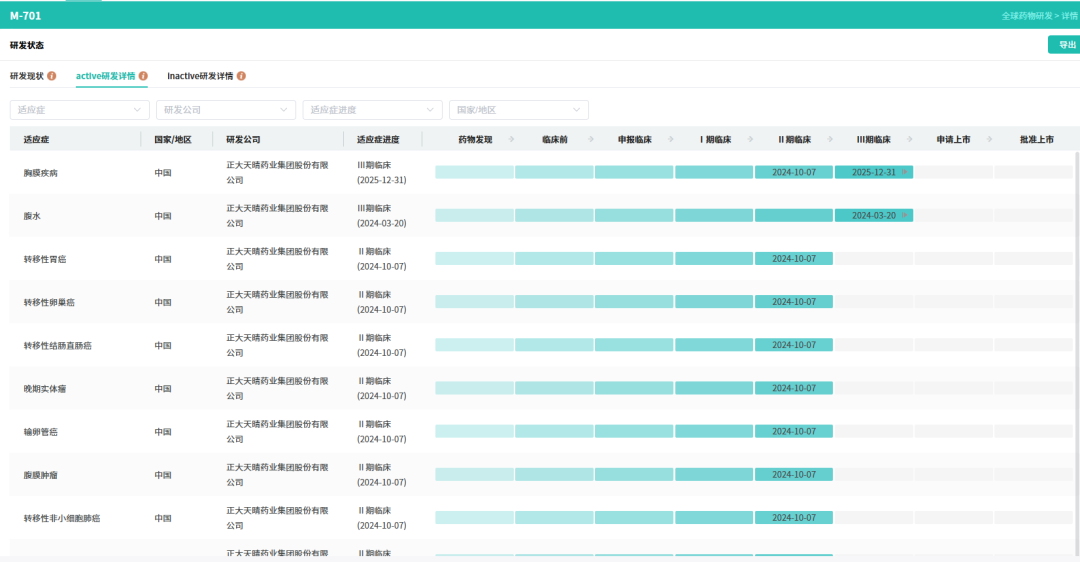
目前,M701正在中国开展多项临床试验,其中已完成一项针对上皮性实体瘤引发的恶性腹水(MA)的关键Ⅲ期临床试验,其上市申请已获CDE正式受理;另有一项针对非小细胞肺癌引发的恶性胸水 (MPE)的Ⅱ期临床试验,目前已完成受试者入组。
02
国产双抗M701安全性和疗效,恶性腹水治疗困局有望破冰
恶性积液是中晚期恶性肿瘤的常见并发症,其中以恶性胸水和恶性腹水最为常见,“腹水抽了又涨、涨了再抽”是许多癌症患者在晚期、终末期都会经历的症状。据统计,约50%的晚期恶性肿瘤患者在疾病进展过程中会出现恶性胸腹水,直接影响患者的生活质量和生存期。目前临床缺乏有效的标准治疗方案,仍以穿刺引流联合局部胸腹腔灌注药物为主,局部治疗药物选择有限,且其使用缺少专家共识指导和大型临床研究数据支持,患者生存质量差,存活期短,存在巨大的未满足需求。与目前临床主要治疗方案相比,M701安全性和疗效更优,有望成为胸腹水治疗的标准方案。
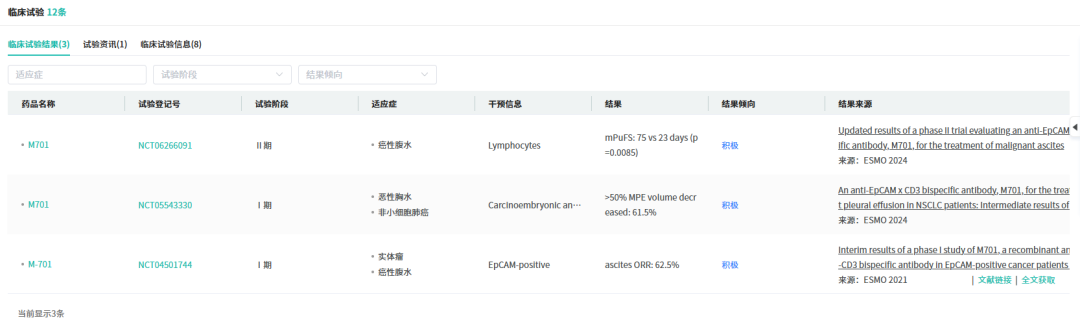
M701针对恶性腹水的Ⅲ期临床试验数据计划于2026年美国临床肿瘤学会(ASCO)大会公布。其治疗恶性胸水的II期临床研究中期数据曾在去年ESMO(欧洲肿瘤内科学会)公布,结果显示,与顺铂相比,M701胸腔灌注在治疗恶性胸水方面显示出显著疗效,且耐受性良好,并已显示出在预防胸水再次积聚方面具有可观的潜力。
M701上市申请获受理,是国内双特异性抗体赛道在实体瘤治疗领域的重要突破。若顺利获批,它不仅将填补恶性腹水靶向治疗的空白,也有望凭借其在胸水领域的拓展潜力,成为肿瘤支持治疗领域的重磅产品。随着ASCO数据的即将公布,该药的临床价值与市场前景将得到进一步验证。
END
本文为原创文章,转载请留言获取授权
近期更多摩熵咨询最新报告
识别下方二维码领取

联系我们,体验摩熵医药更多专业服务 | ||||
会议 合作 | 报告 定制 | 数据库 咨询 | 数据 定制 | 媒体 合作 |