司美格鲁肽“续命”一年
3月20日,司美格鲁肽在中国的核心专利到期,十余家国产药企早已摩拳擦掌,九源基因、丽珠集团、齐鲁制药、华东医药等至少10家企业的仿制药上市申请已获国家药监局受理。然而,一个容易被忽视的关键细节是:专利到期并不意味着仿制药马上就能上市,国产替代至少还要再等一年。
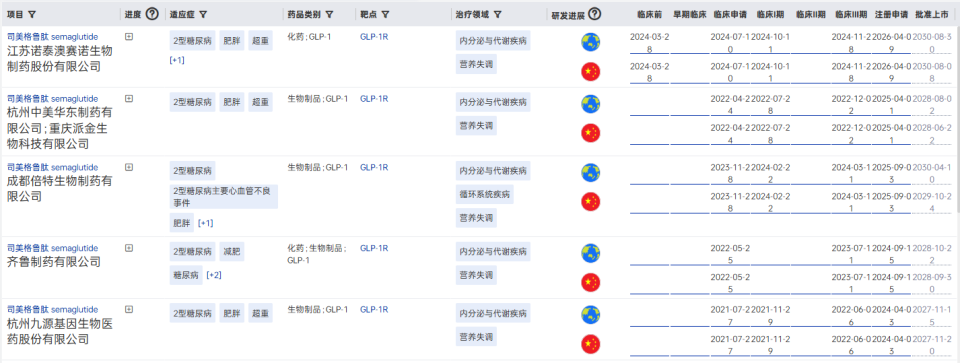
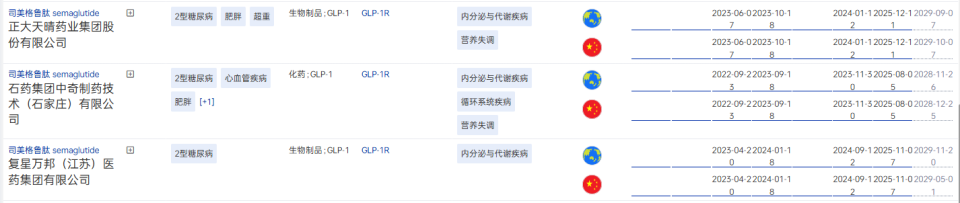
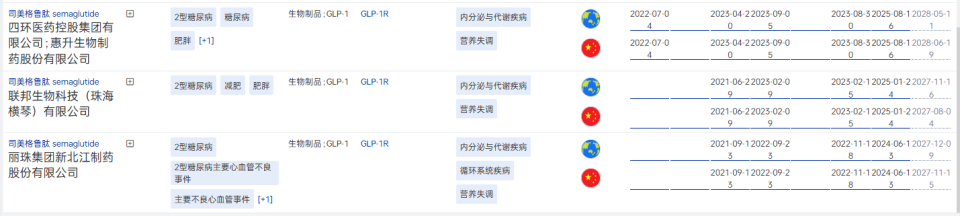
国内司美格鲁肽仿制药进展
图片来源:药智数据-全球药物分析系统
表面上看,3月20日专利届满后,国产药企已可合法使用司美格鲁肽的分子结构进行生产,此前被专利“卡住”的上市申请也集中进入审评流程。但真正的障碍在于数据保护期。
据悉,司美格鲁肽于2021年4月27日在中国获批时,上市许可持有人为注册于瑞士苏黎世的诺和诺德制药有限公司,由此可适用中瑞自贸协定的6年数据保护规则。以此计算,其数据保护期要到2027年4月27日才届满,这意味着在专利到期后,诺和诺德还将额外享受约13个月的保护期。
在此期间,仿制药企业的上市申请审评处于暂停状态。对企业而言,要么等到2027年4月窗口期过后再走流程,要么自己重新做全套临床试验——但后者的时间和费用成本几乎不现实。因此,尽管专利壁垒已拆除,数据保护的“第二道门”仍将国产仿制药挡在门外。
相反,这13个月的额外保护期对诺和诺德而言价值巨大。2025年财报显示,司美格鲁肽全球销售额高达346亿美元,占公司营收七成。中国是其仅次于美国的全球第二大市场,2025年销售额约74.9亿元(约10.33亿美元)。有测算认为,若以2025年销售数据为依据,诺和诺德在这13个月内的预计销售额或将达到约80亿元。
虽然正式获批还需等待,但国产药企的备战早已进入白热化阶段。目前申报企业主要分为两派:一派是以九源基因、丽珠集团、华东医药等为代表的生物类似药路径(3.3类申报),另一派是诺泰生物、石药中奇等选择的2.2类改良新药路径。后者因注册类别差异,可能在审评速度上占据优势。
结语:司美格鲁肽专利到期是中国GLP-1市场格局重塑的重要节点,但专利到期、仿制药还要再等一年的现实,揭示了创新药保护的复杂性——化合物专利与数据保护构成了双重壁垒。对诺和诺德而言,这13个月是宝贵的战略缓冲;对国产药企而言,则是最后的能力蓄力期。2027年4月之后,一场涉及降糖、减重两大千亿级市场的平价替代大战才真正拉开序幕。届时,价格、产能、渠道和适应症布局,将决定谁能从诺和诺德手中切走蛋糕。
参考来源:
1.药智数据-全球药物分析系统
2.http://www.cninfo.com.cn/new/disclosure/detail?orgId=9900061600&announcementId=1225161036&announcementTime=2026-04-23%2017:32
