DMD 赛道竞速:Dyne 拟 Q2 递交 BLA,细胞/基因/核酸三路并进

2026 年 5 月 13 日
医麦客新闻 eMedClub News
2026 年 5 月 11 日,Dyne Therapeutics 公布第一季度财报,披露其核心管线 z-rostudirsen(DYNE-251)针对外显子 51 跳跃杜氏肌营养不良症(DMD)已完成与 FDA 的积极 Pre-BLA 会议,双方已就加速批准 BLA 内容达成一致。公司拟于 2026 年 Q2 提交 BLA,若获优先审评,有望于 2027 年 Q1 在美国上市。
在 2026 年肌肉萎缩症协会(MDA)上,Dyne 公布了Ⅰ/Ⅱ 期试验 DELIVER 的长期数据:4 例接受 20 mg/kg(每 4 周一次)治疗至少 12 个月的患者,未调整肌营养不良蛋白产生水平平均达到正常值的 9.48%(n=4),而基线时为 0.52%(n=3);肌肉含量调整后的肌营养不良蛋白产生水平平均达到正常值的 18.33%(n=4),而基线时为 1.47%(n=3)。
在先前报告的来自 DELIVER 试验中入组并随访长达 36 个月的 86 名参与者的安全性和耐受性研究中,z-rostudirsen 耐受性良好,大多数治疗相关不良事件为轻中度。
Z-rostudirsen 是基于 Dyne 专有的 FORCE™ 平台开发的一种抗体偶联寡核苷酸(AOC)疗法。通过将一种经过验证的磷酸二氨基甲酰吗啉寡核苷酸(PMO)与一个靶向转铁蛋白受体 1(TfR1)的抗体片段(Fab)进行偶联,利用 TfR1 在肌肉组织中高度表达,实现 PMO 精准靶向肌肉组织递送,促进核内外显子跳跃,从而使肌肉细胞生成截短但功能正常的抗肌萎缩蛋白,以停止或逆转疾病进展。
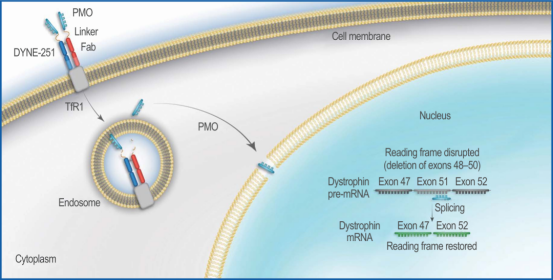
▲ z-rostudirsen 利用 TfR1 将外显子 51 跳跃的 PMO 传递到 DMD 受影响的肌肉中
除 z-rostudirsen 外,Dyne 正在推进四种开发候选药物(DYNE-253、DYNE-245、DYNE-244 和 DYNE-255),用于潜在治疗适合跳跃外显子 53、45、44 和 55 的 DMD。
DMD 是一种致命的 X 连锁隐性遗传神经肌肉疾病,由编码抗肌萎缩蛋白(dystrophin)的基因突变引起。患者因缺乏功能性抗肌萎缩蛋白,肌肉组织会进行性退化和纤维化,通常在儿童期丧失行走能力,在 20-30 岁左右因呼吸衰竭或心力衰竭早逝。
目前,糖皮质激素(如 prednisone、deflazacort)是最早用于 DMD 延缓肌肉退化的基础治疗手段。四款 ASO 外显子跳跃药物已获 FDA 批准上市,分别为:eteplirsen(外显子 51)、golodirsen(外显子 53)、viltolarsen(外显子 53)及 casimersen(外显子 45)。AAV 基因治疗药物 Elevidys 有望实现一次治疗,终生治愈,但肝毒性问题曾引发关注。在研管线中,细胞、基因与核酸三大主流技术正加速并进。
细胞疗法
细胞疗法重点不在于直接修复基因或蛋白,而是通过调节受损组织的微环境、减轻炎症和纤维化,来保护肌肉功能。
Capricor Therapeutics 的同种异体细胞疗法 deramiocel 进展最为迅速,已重新向 FDA 递交 BLA 申请,PDUFA 目标日期为 2026 年 8 月 22 日。该疗法由心脏来源细胞组成,通过释放含微 RNA、非编码 RNA 及蛋白的外泌体,改善 DMD 患者肌肉纤维化及心脏功能。
2026 年 3 月,Capricor 在 2026 年 MDA 大会上公布了 deramiocel 治疗 DMD 的 Ⅲ 期 HOPE-3 临床试验的额外分析和新的功能结局数据,进一步丰富了该疗法支持 BLA 申请的证据。
研究显示:通过心脏 MRI 上的 LGE 测量,心肌纤维化进展显著减缓(p=0.022);在基线存在心肌病的患者中,左心室射血分数(LVEF)较安慰剂显著改善(p=0.017);全球统计检验复合终点显示整体治疗获益显著;杜氏视频(DVA)评估显示疾病进展减缓约 83%(p=0.018)。
为把握时代新机,直面变局,医麦客携手 MaxCyte 于 2026 年 5 月 14 日(周四)15:00-16:30 带来主题为「818 号令时代,CGT 企业如何走通合规双轨?」的直播课,邀请了 MaxCyte 应用科学家何争诚、上药生物治疗质量与注册总监张长风等专家进行线上演讲,欢迎大家扫码预约直播课!

基因疗法
基因疗法旨在通过一次性干预,为患者提供潜在持久甚至终生的抗肌萎缩蛋白表达。目前,该领域已经形成 AAV 基因替代和基因编辑两大主要技术分支。其中,AAV 基因替代疗法已率先实现商业化突破(Elevidys),而基因编辑疗法正快速追赶。
在研管线中,Genethon 公司的 GNT0004、RegenxBio 公司的 RGX-202 等候选产品均处于关键临床阶段。这些候选产品在 AAV 衣壳选择和启动子优化上各有特色,致力于解决现有疗法转导效率不高、剂量过大等痛点。
RGX-202 是一款基于 AAV8 载体的潜在同类最佳基因疗法,搭载肌肉特异性启动子 Spc5-12,将编码微肌营养不良蛋白的转基因递送至骨骼肌和心肌。其独特之处在于保留了关键的 C 末端(CT)结构域,使产生的微肌营养不良蛋白功能更接近天然蛋白。
今年 MDA 大会上,Regenxbio 发布了 RGX-202 治疗 DMD 关键性临床试验 AFFINITY DUCHENNE 的积极中期数据。数据显示,在北极星移动评价量表(NSAA)中,大龄受试者 (n=5) 与 cTAP 模型预测的自然疾病进展相比平均提升了 5.2 分。最新的心脏 MRI 数据显示,治疗后一年 LVEF 平均维持在 61.6%。在长达两年的随访期内,所有 1 至<12 岁的关键剂量患儿均未出现肝损伤迹象。公司计划于 2026 年年中向 FDA 申请 Pre-BLA会议。
GNT0004 是一款基于 AAV8 载体的基因疗法,搭载肌肉/心脏特异性启动子 Spc5-12,递送优化的 hMD1 转基因——编码抗肌萎缩蛋白的缩短但功能性版本。其 Ⅲ 期临床采用 3×10¹³ vg/kg 剂量(远低于同类疗法),已于 2025 年 9 月启动。
今年 MDA 大会公布的随访数据显示:NSAA 评分+9 分;6 分钟步行试验多走 173 米;CPK平均降低 70%;肌肉脂肪分数差异>18%;无严重副作用。
国内信念医药、金唯科生物等已启动 AAV 基因治疗临床研究。此外,Cure Rare Disease、新芽基因、辉大基因、博雅辑因等正探索基因编辑精准修复基因突变。
小核酸疗法
已获批上市的四款 ASO 药物几乎均基于 PMO 化学结构,存在肌肉靶向性、需要频繁给药的局限,新一代的技术正通过创新递送平台(如 PepGen 的 EDO 平台、Dyne 的抗体偶联技术等)突破这一瓶颈。
前文提到的 Dyne 的 FORCE™ 平台是代表之一,PepGen 公司的 EDO(增强型寡核苷酸)平台同样致力于提升药物进入肌肉细胞的能力,并扩大作用组织范围。
另一种思路则是绕过 DMD 基因本身,通过上调其他具有类似功能的蛋白来补偿 dystrophin 的缺失。比如,中美瑞康的 RAG-18 是一款首创机制的双链小激活 RNA(saRNA)候选药物,旨在通过 RNA 激活(RNAa)技术特异性上调 UTRN 基因表达,提升 utrophin 蛋白水平,以功能性替代缺失的肌营养不良蛋白。这一策略的优势在于不依赖于特定的基因突变类型,理论上适用于所有 DMD 患者。
责任编辑丨菊
校对丨菊
参考资料:
1.https://www.globenewswire.com/news-release/2026/05/11/3291782/0/en/dyne-therapeutics-reports-first-quarter-2026-financial-results-and-recent-business-highlights.html
精彩活动
长按识别二维码立即参与↓

点点“分享”、“点赞”和“在看”
给我充点儿电吧~