8亿重磅首仿落地,国产CDK4/6抑制剂市场迎来变局
发布时间:2026-05-12来源:药事纵横
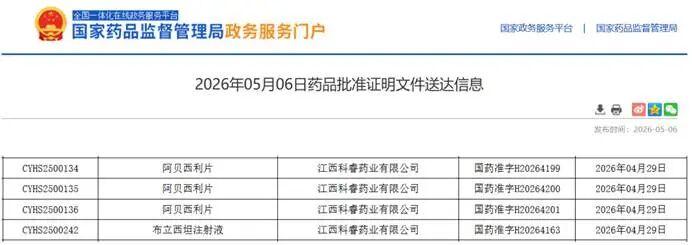
5月6日,NMPA一日之内批准了两款仿制药——阿贝西利片(首仿)和布立西坦注射液(首家)。前者是年销超8亿元的乳腺癌靶向药,后者则补齐了抗癫痫品种的剂型拼图。在首仿争夺日益白热化的当下,这不仅是两家企业的速度竞赛,更折射出本土仿制药从“跟跑”到“抢位”、从单一剂型到组合覆盖的策略升级。一、阿贝西利首仿落地——8亿蛋糕如何切?
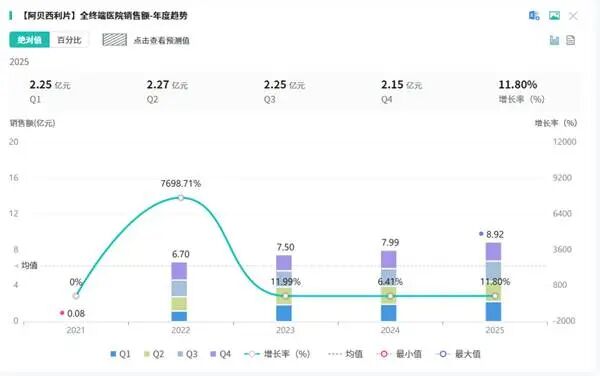
阿贝西利作为礼来研发的口服CDK4/6抑制剂,自2020年12月进入中国市场以来,凭借明确的疗效的和良好的耐受性,迅速成为HR+/HER2-晚期或转移性乳腺癌治疗的核心药物,市场规模持续扩容,成为国产仿制药企业争抢的“香饽饽”。其首仿的落地,将彻底打破原研独占的市场格局,开启8亿级市场的分蛋糕之争。从市场现状来看,阿贝西利的临床需求与市场潜力尤为突出。根据摩熵医药数据显示,2025年阿贝西利在国内全终端医院市场的销售额超8亿元,同比增长11.80%,保持稳健增长态势。这一成绩的背后,是庞大的患者基数与明确的临床定位——HR+/HER2-乳腺癌是乳腺癌中最常见的亚型,约占所有乳腺癌病例的70%以上,而CDK4/6抑制剂已成为该亚型晚期患者的标准治疗方案,能够有效阻断肿瘤细胞周期进展,诱导乳腺癌细胞衰老与凋亡,显著延长患者无进展生存期。图源:摩熵医药数据库在原研垄断时期,礼来凭借先发优势,牢牢占据国内阿贝西利市场的全部份额,患者用药成本居高不下,也为国产仿制药的替代留下了广阔空间。此次科睿药业率先获批阿贝西利片4类仿制,成为国内首仿+首家过评企业,率先切入这一8亿级市场,标志着国产替代正式启动。值得注意的是,仿制药申报领域并非科睿药业一家独大,齐鲁制药紧随其后,同样以4类仿制提交上市申请,目前处于审评审批阶段。由于两家企业报产时间差距不大,业内预计齐鲁制药将在数月内获批,拿下第二家过评,形成“双雄争霸”的初始竞争格局。价格博弈与国产替代预期,成为此次首仿落地的核心看点。通常情况下,首仿药上市后,价格有望降至原研药的50%-70%,这一价格优势将大幅提升药物可及性,尤其对于需要长期用药的乳腺癌患者而言,将显著降低用药负担。与此同时,首仿药的上市也将给原研药礼来带来巨大的医保谈判压力——若礼来不调整价格策略,其市场份额将面临被国产仿制药快速挤压的风险;而若主动降价,又将压缩自身利润空间,陷入两难境地。更深远的影响在于,阿贝西利首仿的落地,将引发整个国产CDK4/6抑制剂市场的连锁反应。目前国内CDK4/6抑制剂市场除了阿贝西利,还有哌柏西利、瑞博西利等品种,其中哌柏西利的仿制药竞争已趋于激烈,阿贝西利首仿的快速推进,将进一步加速整个赛道的仿制药竞争节奏,倒逼其他品种的仿制药企业加快申报进度,推动CDK4/6抑制剂整体价格下行,让更多患者受益。但需要明确的是,首仿获批仅仅是市场竞争的起点,而非终点。对于科睿药业而言,要想在8亿级市场中占据优势,仅凭“首仿”标签远远不够,产能、渠道覆盖与学术推广能力,才是决定后续市场放量的关键。反观齐鲁制药,作为国内肿瘤领域的头部仿制药企业,拥有成熟的销售网络与丰富的学术推广经验,即便作为第二家过评企业,也有望凭借渠道优势快速抢占市场份额,与科睿药业形成分庭抗礼的格局。未来,两家企业的竞争将从“获批速度”转向“市场运营能力”,而这也将成为国产仿制药企业抢占市场的核心竞争力。二、布立西坦“口服+注射”双剂型——是护城河还是标配?
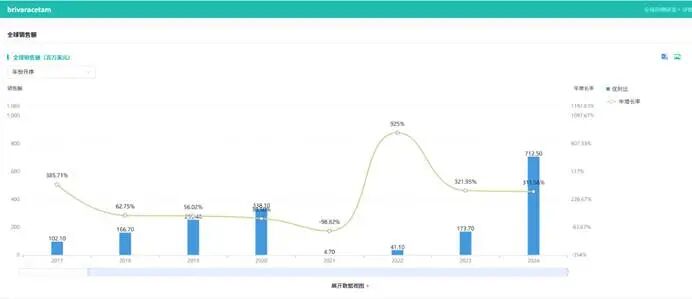
在阿贝西利首仿落地的同时,科睿药业的布立西坦注射液同步获批,成为国内首家获批该剂型的企业。结合2024年率先获批的布立西坦片,科睿药业已实现布立西坦“口服+注射”双剂型布局,这一布局既彰显了企业的研发与申报实力,也引发了行业对“双剂型布局价值”的深度思考:在仿制药竞争日趋激烈的背景下,双剂型究竟是企业的差异化护城河,还是未来市场竞争的标配?先看布立西坦的品种概况。该品种由优时比研发,属于新一代抗癫痫药物,是第二代突触小泡蛋白2A配体,与左乙拉西坦结构类似,具有起效快、耐受性好等特点,主要适用于局灶性癫痫发作的治疗。从市场规模来看,布立西坦的全球市场表现亮眼,2024年优时比的布立西坦全球销售额超7亿美元;国内市场虽目前基数较低,但增长势头迅猛,摩熵医药数据显示,2025年该品种全终端医院销售额超3000万元,随着临床应用的不断普及,未来市场潜力可期。图源:摩熵医药数据库科睿药业在布立西坦的国产化进程中始终保持领先态势:2024年,其布立西坦片率先获批上市,成为国内独家品种,并成功纳入国家医保目录,借助医保的加持快速实现市场渗透;此次布立西坦注射液的获批,进一步完善了产品剂型布局,形成“口服+注射”的完整产品组合,能够更好地满足临床多样化需求。但这种领先优势并非不可撼动,目前国内已有成都奥邦药业、成都利尔药业两家企业提交了布立西坦3类仿制药上市申请,均处于审评审批阶段。从行业惯例来看,这两家企业大概率会同时申报片剂和注射液两种剂型,这意味着科睿药业的“首家”窗口期可能仅有6-12个月,后续市场竞争将迅速加剧。图源:中国药品审评数据库从临床价值来看,布立西坦“口服+注射”双剂型布局确实具有显著的临床优势。癫痫的治疗具有明显的阶段性特征:急性期需要快速通过注射剂型控制癫痫发作,稳定期则需要通过口服剂型维持治疗,双剂型组合能够实现“急性期控制+稳定期维持”的无缝衔接,为患者提供更灵活、便捷的治疗选择,也有助于提升患者的治疗依从性。尤其对于无法口服给药的急性期患者而言,注射剂型的补充的能够填补临床治疗空白,体现出差异化的临床价值。但在国家集采常态化的背景下,双剂型布局的商业价值需要理性看待。若布立西坦未来被纳入国家集采,其定价将以“低价中选”为核心原则,双剂型未必能为企业带来额外的价格溢价,更多是体现为院内配套优势——能够满足医院不同治疗场景的需求,提升产品在院内的准入竞争力,而非单纯依靠剂型差异获取更高利润。此外,随着后续竞争者的加入,若多家企业均实现双剂型布局,那么双剂型将从“差异化优势”转变为“市场竞争标配”,届时企业的核心竞争力将回归到成本控制、制剂工艺等更核心的层面。这也引发了行业的深度思考:国产仿制药企业的差异化布局,不应仅仅局限于剂型延伸,更应聚焦于核心技术的突破。布立西坦的案例表明,独家地位是暂时的,一旦后续竞争者获批,市场将迅速转向价格竞争,单纯的剂型差异难以形成长期的竞争壁垒。真正的差异化优势,应来自于原料药自产带来的成本优势、制剂工艺优化带来的质量优势,或是复方创新、剂型改良带来的临床价值提升,唯有这样,才能在激烈的市场竞争中站稳脚跟。三、首仿竞赛背后——速度、策略与可持续性
科睿药业一日之内拿下两款重磅品种的获批,并非偶然,而是企业精准布局、高效执行的结果。今年以来,科睿药业的获批节奏明显加快,已有5个品种获批并视同通过一致性评价,其中除了阿贝西利首仿、布立西坦注射液首家获批,还包括熊去氧胆酸口服混悬液(国产第2家),展现出强劲的研发与申报能力。但科睿药业的快速发展,并非行业孤例——正大天晴、齐鲁制药、石药集团等国内头部仿制药企业,在首仿抢报领域同样动作凶猛,首仿竞赛已进入白热化阶段。但值得警惕的是,首仿的“价值衰减曲线”正在不断变陡。在过去,由于审评审批周期较长,首仿企业往往能享受1-2年的市场独占期,凭借先发优势快速抢占市场份额,获取丰厚利润;而如今,随着我国药品审评审批制度改革的持续深化,审评速度大幅提升,多家企业报产时间差不断缩短,首仿的市场独占期已被大幅压缩,部分品种的首仿窗口期甚至缩短至6个月甚至更短。以阿贝西利为例,科睿药业率先获批,但齐鲁制药紧随其后,若齐鲁在半年内顺利获批,科睿药业的首仿先发优势将大打折扣,两者的市场竞争将直接进入白热化阶段,首仿的“稀缺价值”也将大幅降低。这种变化,正推动国产仿制药行业的竞争格局从“速度之争”向“综合实力之争”演变。过去,企业的核心竞争力集中在“谁先报产、谁先获批”;而如今,随着首仿窗口期的缩短,单纯的速度优势已难以支撑企业的长期发展,竞争的核心已转向“谁更能控制成本、谁更能覆盖终端”。国家集采对仿制药的定价权日益强势,无论是首仿药还是后续仿制药,若想在集采中脱颖而出,实现市场放量,就必须具备强大的成本控制能力;同时,终端渠道覆盖、学术推广能力也成为关键——只有快速将产品推向医院、获得医生和患者的认可,才能在激烈的竞争中抢占优势份额,甚至实现对首仿企业的弯道超车。这也给国产仿制药企业带来了深刻的反思:企业不应过度沉迷于“首仿”标签,而应理性思考仿制药的长期发展定位。当前,仿制药行业的“内卷”日益加剧,扎堆抢仿成熟品种、单纯比拼获批速度的发展模式,已难以适应行业发展趋势。未来,仿制药企业的角力场将转向三个方向:一是高端难仿品种,聚焦技术门槛高、研发难度大的复杂制剂、高端仿制药,避开同质化竞争;二是差异化剂型,通过剂型改良、组合布局,满足临床未被满足的需求,形成独特的竞争优势;三是改良型新药,在仿制的基础上进行技术创新,提升药物的临床价值,实现从“仿制”到“创新”的跨越。对于科睿药业而言,此次两款重磅品种的获批,是企业发展的重要里程碑,但也只是长期发展的起点。如何借助阿贝西利首仿的先发优势,快速构建渠道与学术优势;如何依托布立西坦双剂型布局,巩固抗癫痫领域的市场地位;如何在首仿竞赛中保持优势,同时布局长期差异化发展,将是企业未来需要解决的核心问题。而对于整个国产仿制药行业而言,科睿药业的案例也提供了有益的借鉴——唯有兼顾速度与策略,聚焦差异化与可持续性,才能在激烈的市场竞争中实现高质量发展。结语
一天两款新品获批,看似是某家企业的胜利,实则是本土仿制药产业整体提速的缩影。首仿带来价格下调与可及性提升,但窗口期正在缩短;双剂型构建了短期优势,却难挡后来者的围剿。对于行业而言,真正的课题不是“谁第一个抢到”,而是“抢到之后,如何让患者和医生真正用起来”。毕竟,获批只是起点,市场才是终局。参考:NMPA官网;中国药品审评数据库;摩熵医药数据库
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。