维奈克拉之后,群雄并起:BCL-2抑制剂赛道谁主沉浮?
发布时间:2026-05-12来源:药事纵横
癌症治疗领域近年来取得了显著进展,其中靶向治疗和免疫疗法成为主流。然而,肿瘤细胞的抗凋亡机制仍是许多耐药性的关键因素。BCL-2(B细胞淋巴瘤2)蛋白作为抗凋亡的核心调控因子,在多种血液肿瘤和实体瘤中高表达,导致癌细胞逃避程序性死亡。因此,BCL-2抑制剂的研发成为癌症治疗的重要方向。自20世纪90年代BCL-2蛋白被发现以来,科学家们逐步揭示了其在肿瘤存活中的作用,并开发出多种小分子抑制剂。从早期的非选择性药物到如今的高选择性BCL-2抑制剂,这一领域经历了漫长的探索。本文将详细梳理BCL-2抑制剂的研发历程、早期药物的副作用及优化策略、临床应用案例,并介绍在该领域表现突出的企业,以期为读者提供全面的行业洞察。一、BCL-2抑制剂的研发历程
1.1 BCL-2蛋白的发现与作用机制
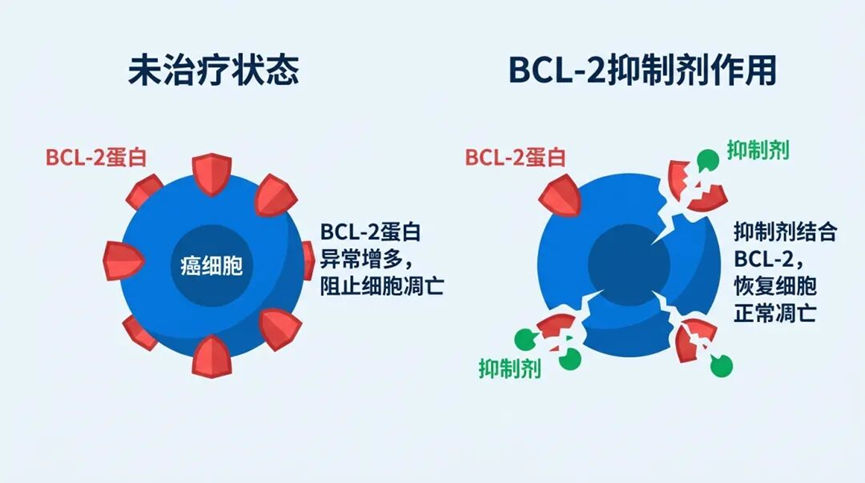
BCL-2蛋白最早于1984年在滤泡性淋巴瘤中被发现,其过表达可抑制细胞凋亡,促进肿瘤存活。BCL-2家族蛋白包括抗凋亡成员(如BCL-2、BCL-XL、MCL-1)和促凋亡成员(如BAX、BAK、BH3-only蛋白)。在正常细胞中,这两类蛋白维持动态平衡;而在癌细胞中,抗凋亡蛋白的异常表达导致凋亡信号被阻断,使癌细胞得以持续增殖。1.2 早期BCL-2抑制剂的探索
最初的BCL-2抑制剂研究集中在天然产物和化学小分子上。例如,Obatoclax(GX15-070)和AT-101(棉酚衍生物)是第一代BCL-2抑制剂,但它们对BCL-2家族多个成员均具有抑制作用,选择性较低,导致毒副作用较大。1.3 高选择性BCL-2抑制剂的突破
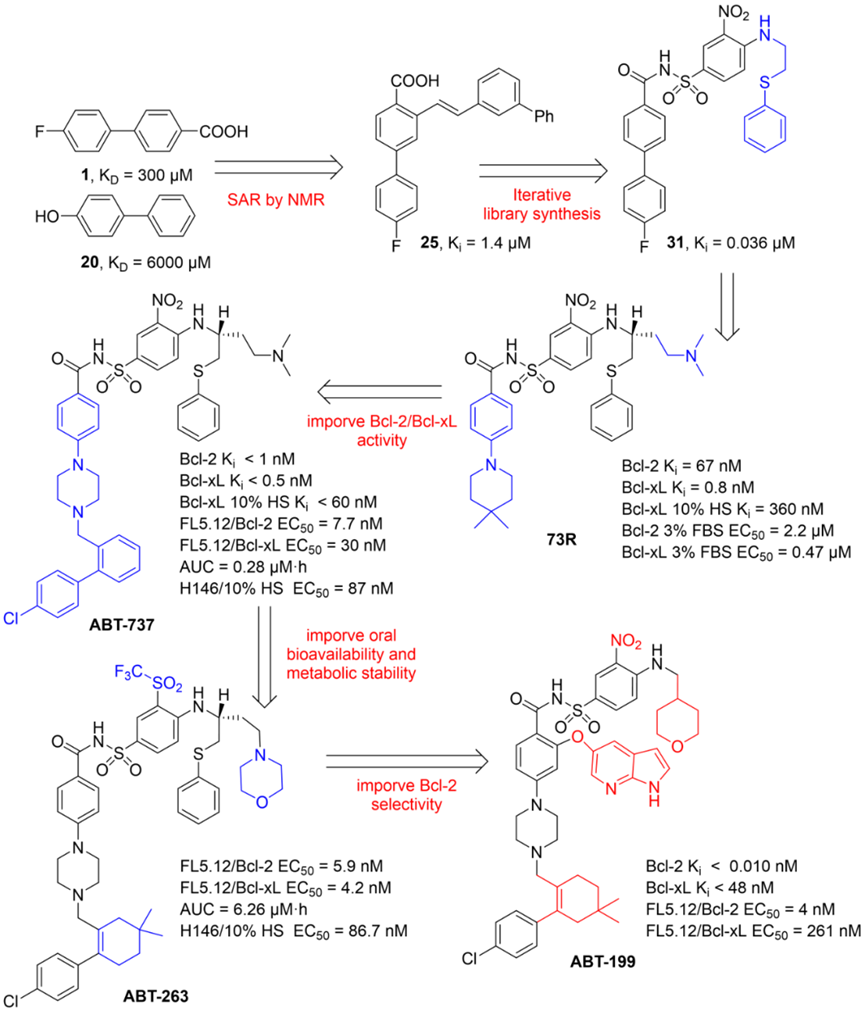
2016年,Venetoclax(维奈克拉,ABT-199)的上市标志着BCL-2抑制剂进入精准靶向时代。Venetoclax是首个高选择性BCL-2抑制剂,对BCL-2的亲和力比BCL-XL高100倍以上,显著减少了血小板减少等副作用。其成功源于结构生物学和计算机辅助药物设计的进步,使科学家能够精确优化药物与BCL-2的结合位点。图1. BCL-2选择性抑制剂维奈克拉的分子设计过程二、早期BCL-2抑制剂的副作用及其优化策略
BCL-2抑制剂的研发历程并非坦途,它始于对抗凋亡蛋白的广泛攻击,却因伴随而来的严重副作用而步履维艰。正是对这些早期挑战的深刻反思与科学应对,才最终推动了该领域向更安全、更高效的精准治疗时代迈进。2.1 早期药物的副作用:疗效与安全性的艰难平衡
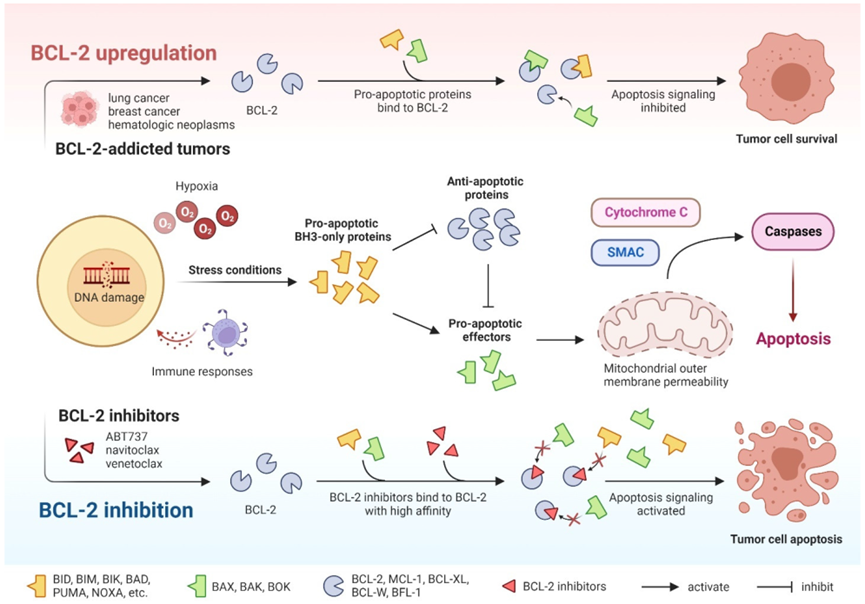
第一代BCL-2抑制剂大多属于广谱抑制剂,它们在阻断肿瘤细胞生存通路的同时,也无差别地影响了依赖相同通路的正常细胞,导致了一系列难以管理的毒性反应。(1)Obatoclax(GX15-070):初探的代价Obatoclax作为早期进入临床的代表性药物,其设计目标是模拟促凋亡蛋白BH3结构域,从而非选择性地抑制BCL-2、BCL-XL及MCL-1等多个抗凋亡蛋白。这种广谱性是其毒性的根源。血小板的存活高度依赖BCL-XL蛋白,Obatoclax对BCL-XL的抑制直接触发了血小板的程序性死亡,导致患者出现显著的血小板减少,增加了出血风险。同时,其对骨髓造血功能的干扰也引发了中性粒细胞减少,削弱了患者的免疫防线。此外,部分临床试验还观察到中枢神经系统毒性,如精神错乱和嗜睡。这些多重毒性叠加,使得Obatoclax的治疗窗口非常狭窄,最终限制了其临床应用价值。图2. BCL-2抑制剂的细胞凋亡过程及作用机制示意图AT-101是天然化合物棉酚的左旋异构体,同样被开发为一种泛BCL-2家族抑制剂。其副作用谱与Obatoclax有所不同,主要表现为常见的胃肠道反应,如恶心、呕吐和腹泻,这与其对消化道黏膜的潜在刺激有关。更值得关注的是其肝毒性,临床试验中部分患者出现转氨酶升高,提示药物可能对肝细胞造成损伤。尽管在临床前研究中展现出一定潜力,但在多项II期临床试验中,AT-101无论是单药还是联合化疗,其客观缓解率和生存获益均未达到预期。在可耐受的剂量下,其抗肿瘤活性不足,而毒性问题却持续存在,最终导致其研发进程因疗效与毒性比不佳而放缓。(3)Navitoclax(ABT-263):最接近成功,却倒在关键副作用上Navitoclax是研发过程中的一个关键里程碑,它基于对BCL-2蛋白结构的深入理解,实现了对BCL-2、BCL-XL和BCL-w的高效抑制,并在临床试验中展现出强大的抗肿瘤活性。然而,它的成功之路被一个单一但致命的副作用所阻断,即剂量限制性血小板减少症。Navitoclax对BCL-XL的高效抑制,如同切断了血小板的生命线,导致给药后血小板计数迅速下降。为了控制这一风险,研究人员不得不降低药物剂量或采用间歇给药方案,但这又使得药物浓度难以持续维持在有效抗肿瘤水平之上。这一两难困境,使得Navitoclax的单药开发计划受阻,但它的失败也为后续药物的研发指明了最关键的优化方向:必须避开对BCL-XL的抑制。2.2 优化策略:科学智慧驱动的迭代升级
面对早期药物的困境,研究人员从分子结构、临床应用和未来布局等多个维度进行了系统性优化,成功实现了BCL-2抑制剂的迭代升级。这是最核心且最成功的优化策略。通过对BCL-2、BCL-XL和MCL-1蛋白三维结构的原子级解析,科学家发现它们在关键的氨基酸残基上存在细微差异。AbbVie的研究团队正是利用了BCL-2蛋白上独特的Asp103口袋,对Navitoclax的分子结构进行了精妙改造,成功开发出Venetoclax。新分子能够特异性地与BCL-2的口袋紧密结合,而与BCL-XL的口袋则产生空间位阻。这一设计使得Venetoclax对BCL-2的亲和力比Navitoclax提高了近100倍,而对BCL-XL的亲和力则降低了数千倍。最终,Venetoclax实现了对BCL-2的亚纳摩尔级高选择性抑制,在保留强大抗肿瘤活性的同时,几乎完全规避了Navitoclax所面临的严重血小板减少症,成为理性药物设计的典范。单一靶向药物长期使用易产生耐药性,BCL-2抑制剂的主要耐药机制是其他抗凋亡蛋白(如MCL-1)的上调。联合用药策略通过不同机制的药物组合,实现了协同增效。例如,将Venetoclax与BTK抑制剂伊布替尼联用,后者能下调MCL-1的表达,形成双重打击,显著提高了慢性淋巴细胞白血病的缓解深度。在急性髓系白血病治疗中,Venetoclax与低甲基化药物阿扎胞苷的组合,也通过相似的协同机制成为老年患者的标准治疗方案。为了前瞻性地解决耐药问题,研发新一代能够同时抑制多个靶点的抑制剂成为前沿方向。BCL-2/MCL-1双靶点抑制剂的设计理念是在一个分子上整合能分别高效结合BCL-2和MCL-1的药效团,理论上可以预先阻断肿瘤细胞最常见的两条逃逸通路,从而克服或延迟耐药性的产生。尽管MCL-1抑制剂的开发难度极大,但全球多家药企的相关药物已进入早期临床研究。此外,利用PROTAC技术直接降解BCL-2蛋白,而非仅仅抑制其功能,也为克服耐药提供了全新的思路,目前正处于临床前探索阶段。表2. 早期BCL-2抑制剂与Venetoclax的对比三、BCL-2抑制剂的临床应用案例
BCL-2抑制剂的问世,特别是Venetoclax的成功,彻底改变了多种血液恶性肿瘤的治疗格局。其临床应用不仅验证了靶向凋亡通路的巨大潜力,更推动了肿瘤治疗向更加精准和个体化的方向发展。3.1 慢性淋巴细胞白血病(CLL)
Venetoclax在CLL领域的应用是其最成功的临床实践。对于复发或难治性CLL患者,Venetoclax联合抗CD20单抗利妥昔单抗的方案取得了突破性成果。关键临床试验显示,该联合治疗组的完全缓解率超过50%,这意味着半数以上的患者体内已检测不到活跃的癌细胞。更令人振奋的是,患者的无进展生存期得到显著延长,许多患者实现了长期疾病控制。这一高效组合的问世,使得大量高龄或体弱无法耐受传统化疗的CLL患者获得了高质量的治疗选择,正式开启了CLL的无化疗治疗新纪元。3.2 急性髓系白血病(AML)
在治疗难度极高的急性髓系白血病领域,尤其是对于因年龄大或合并症多而无法接受高强度化疗的老年患者,Venetoclax同样展现了革命性的价值。Venetoclax与低甲基化药物阿扎胞苷或地西他滨的联合应用,成为这类患者群体的标准一线治疗方案。临床数据表明,这一组合方案的总体缓解率超过了70%,其疗效远超传统支持性治疗或单药低强度化疗。它通过协同作用,有效诱导白血病细胞凋亡,显著延长了患者的生存期,为过去预后极差的老年AML患者带来了前所未有的生存希望。3.3 其他血液肿瘤
基于其在CLL和AML中的卓越表现,BCL-2抑制剂的应用边界正在不断向其他血液肿瘤拓展。DLBCL具有高度异质性。研究发现,Venetoclax联合标准R-CHOP化疗方案,对于生发中心B细胞样型等特定分子亚型的DLBCL患者,能够提高治疗反应率和生存获益。这体现了基于分子分型的精准治疗策略在淋巴瘤中的应用前景。在多发性骨髓瘤中,BCL-2蛋白的表达水平因细胞遗传学异常而异。临床研究证实,对于携带t(11;14)染色体易位的MM亚型患者,其肿瘤细胞高度依赖BCL-2蛋白存活。因此,Venetoclax联合蛋白酶体抑制剂(如硼替佐米)的方案,在这一特定人群中显示出显著的疗效,为MM的个体化治疗提供了新的范例。四、BCL-2抑制剂国内获批情况
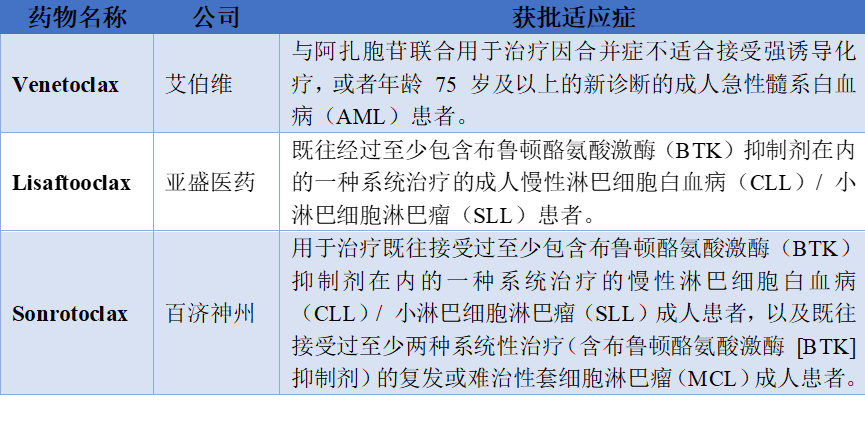
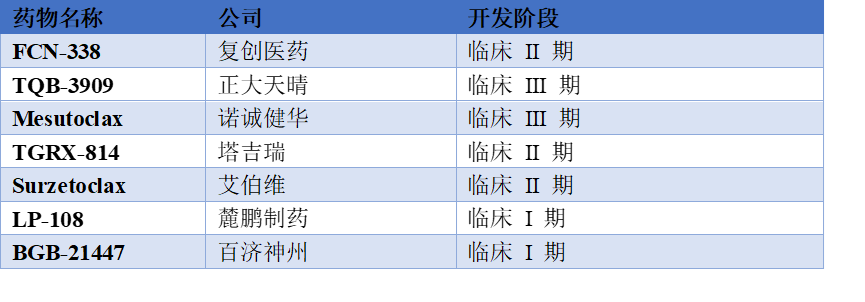
目前国内已有三款BCL-2抑制剂获批上市,分别是来自艾伯维的Venetoclax、亚盛医药的Lisaftoclax和百济神州的Sonrotoclax。它们获批的适应症分别如下表所示。表3. 国内已获批上市的三款BCL-2抑制剂及其适应症除了已获批上市的三款BCL-2抑制剂,另有多款药物处于临床开发阶段,具体如下表所示。五、BCL-2抑制剂研发领域领先企业
BCL-2抑制剂市场的繁荣背后,是多家跨国制药巨头和新兴生物技术公司的激烈竞争与协同创新。这些企业凭借各自独特的研发优势和战略布局,共同推动着该领域向更深、更广的方向发展。5.1 AbbVie开创者与持续引领
作为BCL-2抑制剂领域的绝对领导者,AbbVie凭借其首创的全球首个高选择性BCL-2抑制剂Venetoclax,奠定了其在肿瘤靶向治疗领域的地位。其研发优势在于深厚的结构生物学基础和早期布局,使得Venetoclax成功实现了从CLL到AML等多种血液肿瘤的适应症覆盖。目前,AbbVie并未止步于此,正积极探索Venetoclax与不同机制药物的联合疗法,以期攻克实体瘤这一更具挑战的领域,并致力于解决耐药性问题,持续巩固其行业领导地位。5.2 Roche全球化合作的推动
Roche通过与AbbVie的深度合作,共同开发和推广Venetoclax,充分发挥了其在全球范围内的临床推进能力和商业化网络。Roche的研发优势在于其强大的肿瘤学管线和全球化临床试验管理经验,加速了Venetoclax在世界各地的获批和应用。展望未来,Roche正尝试将BCL-2抑制剂的适应症拓展至自身免疫疾病等非肿瘤领域,探索其在调控免疫细胞凋亡中的潜在价值,展现了其广阔的战略视野。5.3 AstraZeneca攻克BCL-XL难题的挑战
AstraZeneca在BCL-2家族领域的布局颇具特色,其研发重点之一是BCL-XL抑制剂。虽然Navitoclax的开发因血小板毒性受挫,但AstraZeneca并未放弃,而是转向开发创新策略来规避这一副作用,例如开发抗体药物偶联物(ADC)形式,将BCL-XL抑制剂靶向递送至肿瘤组织,从而减少对血小板的系统性影响。这一差异化研发路径体现了其在解决核心科学难题上的决心与创新能力。5.4 Ascentage Pharma中国本土的创新力量
作为中国本土专注于靶向凋亡通路的创新药企,Ascentage Pharma凭借其自主研发的BCL-2抑制剂APG-2575,在全球BCL-2抑制剂研发梯队中占据了重要位置。其研发优势在于快速的临床推进能力和对本土患者需求的深刻理解。APG-2575是首个进入关键临床阶段的中国原研BCL-2抑制剂,其在安全性方面可能具有独特优势,目前正积极开展多项临床试验,有望为国内外血液肿瘤患者提供新的治疗选择。5.5 Novartis前瞻布局下一代抑制剂
Novartis的战略眼光聚焦于克服Venetoclax的耐药性,其代表药物S64315是一款高选择性的MCL-1抑制剂。MCL-1是导致BCL-2抑制剂耐药的关键蛋白之一。Novartis通过布局MCL-1抑制剂,旨在与BCL-2抑制剂形成互补或联合,构建下一代凋亡靶向治疗方案。目前S64315处于早期临床研究阶段,其进展备受关注,代表了行业向双靶点或更复杂凋亡调控网络进化的前沿方向。六、结语
总的来说,BCL-2抑制剂的研发历程体现了从基础科学到临床转化的完整链条。从早期的非选择性药物到如今的高选择性Venetoclax,这一领域不仅改善了血液肿瘤患者的预后,还为实体瘤治疗提供了新思路。未来,随着双靶点抑制剂和联合疗法的进一步发展,BCL-2抑制剂有望在更广泛的癌症类型中发挥作用。同时,制药企业的持续创新(如AbbVie、Ascentage Pharma等)将推动这一领域的竞争与合作,加速新药上市。尽管仍面临耐药性和毒性挑战,但BCL-2抑制剂无疑是癌症靶向治疗的重要里程碑,值得持续关注与期待![1] 张文娴,王凯丰.BCL-2抑制剂治疗多发性骨髓瘤的进展研究[J].中国现代药物应用,2025,19(21):173-176.[2] 米浩,孙道萍.维奈克拉治疗急性淋巴细胞白血病的研究进展[J].临床血液学杂志,2024,37(11):830-838.[3] Kaufman JL, Gasparetto C, Schjesvold FH, Moreau P, Touzeau C, Facon T, Boise LH, Jiang Y, Yang X, Dunbar F, Vishwamitra D, Unger S, Macartney T, Pesko J, Yu Y, Salem AH, Ross JA, Hong WJ, Maciag PC, Pauff JM, Kumar S. Targeting BCL-2 with venetoclax and dexamethasone in patients with relapsed/refractory t(11;14) multiple myeloma. Am J Hematol. 2021 Apr 1;96(4):418-427. doi: 10.1002/ajh.26083.[4] Zhang M, Abe Y, Matsushima T, Nishimura J, Nawata H, Muta K. Selective cyclooxygenase 2 inhibitor NS-398 induces apoptosis in myeloma cells via a Bcl-2 independent pathway. Leuk Lymphoma. 2005 Mar;46(3):425-33. doi: 10.1080/10428190400015691.[5] Schenk RL, Strasser A, Dewson G. BCL-2: Long and winding path from discovery to therapeutic target. Biochem Biophys Res Commun. 2017 Jan 15;482(3):459-469. doi: 10.1016/j.bbrc.2016.10.100.[6] Xu J, Dong X, Huang DCS, Xu P, Zhao Q, Chen B. Current Advances and Future Strategies for BCL-2 Inhibitors: Potent Weapons against Cancers. Cancers. 2023; 15(20):4957.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。