长效给药新范式:小核酸药物如何破解心血管疾病治疗依从性难题
发布时间:2026-05-11来源:药事纵横
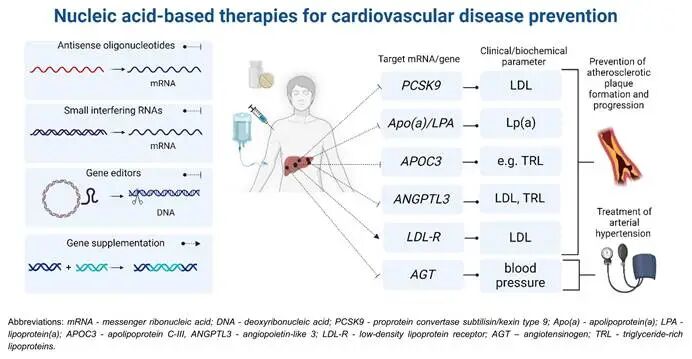
心血管疾病是全球范围内导致人类死亡的首要原因,每年约导致1790万人失去生命。在我国,心血管疾病现患人数已推算高达3.3亿,且随着人口老龄化进程加速,其发病率与死亡率仍呈上升趋势。该类疾病不仅严重威胁患者的生命安全,也极大地降低了患者的生存质量,是65岁以上老年人群最主要的致死原因。心血管疾病的防治具有病程长、需终身干预的显著特征。然而,当前临床实践中,患者血脂、血压等核心指标的达标率依然处于较低水平,以动脉粥样硬化性心血管疾病为例,其低密度脂蛋白胆固醇达标率仅为6.8%。造成这一现状的关键原因在于患者长期用药的依从性较差,而传统的给药频率成为制约依从性的瓶颈。在这一背景下,小核酸药物凭借独特的作用机制脱颖而出。小核酸药物是以寡核苷酸为活性成分的新型治疗药物,主要包括小干扰RNA和反义寡核苷酸等。这类药物通过化学修饰与适宜的递送系统进入靶细胞,利用碱基互补配对原则与特定核酸序列结合,从基因转录后水平精准调控或沉默靶基因的表达。相较于传统小分子药物和生物制剂,小核酸药物具备可编辑性、极高的靶向特异性以及优异的理化稳定性。更为重要的是,小核酸药物在组织中的药效学半衰期极长,能够实现每三个月到六个月给药一次,从根本上改变了慢性病的给药模式。基于此,本文旨在探讨心血管疾病小核酸药物的临床研发特点,并结合国内外监管进展与审评实践,对其关键技术难点提出科学客观的思考与建议。图1.基于核酸的心血管疾病预防疗法一、心血管疾病小核酸药物的作用领域与研发现状
小核酸药物在心血管领域的研发逻辑高度契合临床治疗路径,即从控制血脂、血压等危险因素切入,逐步延伸至靶器官损伤与器质性病变的治疗。根据心血管疾病的核心分类,小核酸药物的布局呈现出多维度的拓展态势。1.1血脂代谢异常类疾病是小核酸药物最核心的靶向领域
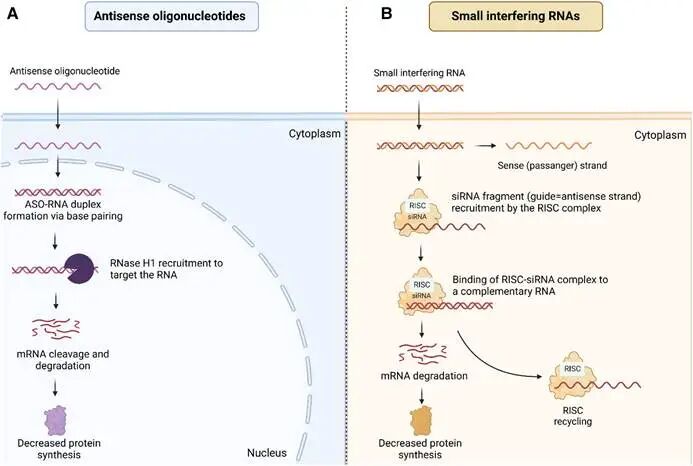
此类疾病是动脉粥样硬化的根本诱因,涵盖家族性高胆固醇血症、高脂蛋白血症以及高甘油三酯血症等。针对这些危险因素,多款小核酸药物已展现出卓越的临床潜力。例如,靶向前蛋白转换酶枯草溶菌素9的英克司兰钠已在全球多国获批上市,用于治疗成人原发性高胆固醇血症或混合型血脂异常。同时,靶向载脂蛋白C-Ⅲ、载脂蛋白及血管生成素样蛋白3的多款小干扰RNA药物正处于密集的Ⅲ期临床试验阶段,旨在解决重度高甘油三酯血症和残余心血管风险问题。值得注意的是,英克司兰钠也是中国上市的心血管疾病领域首个小干扰RNA药物。图2.反义寡核苷酸(ASO)和小干扰RNA(siRNA)的作用机制1.2心脏结构与功能异常类疾病是小核酸药物另一重要突破方向
以转甲状腺素蛋白淀粉样变性伴心肌病为代表的罕见心肌病变,既往缺乏有效的病因治疗手段。靶向人转甲状腺素蛋白mRNA的小干扰RNA药物Vutrisiran的成功研发,证明了小核酸药物在逆转或延缓心肌蛋白错误折叠沉积、改善心衰预后方面的巨大价值。此外,针对心肌缺血及心力衰竭的微小RNA抑制剂也在早期探索中。1.3血管疾病及关联遗传性疾病同样在研发布局之列
针对高血压这一首要危险因素,靶向血管紧张素原的Zilebesiran已进入Ⅱ期临床试验,有望实现长效血压控制。针对血栓性疾病,靶向凝血因子XI的反义寡核苷酸也在研发中,以期在抗栓同时降低出血风险。目前,全球已有多款小核酸药物获批用于心血管疾病,另有近10余款药物处于临床研发后期。这些药物的研发不仅覆盖了高发的常见病,也兼顾了致死率极高的罕见病,标志着心血管疾病治疗正从传统的小分子和抗体时代迈向基因沉默的精准医疗时代。表1.小核酸药物针对不同心血管疾病的临床研究



二、临床药理学及探索性研究的关键技术考量
小核酸药物的理化与生物学特性决定了其临床药理学研究不能沿用传统药物的研发思路。科学合理的早期临床设计是后续确证性试验成功的基石,其核心技术考量主要体现在对药代动力学与药效学分离特征的深入探索上。小核酸药物进入体循环后,通常会被迅速清除,血浆半衰期较短,往往在给药后数小时内即无法在血浆中测得。然而,由于其特殊的化学修饰提高了核酸酶抗性,加之在细胞内形成RNA诱导的沉默复合体后可实现循环利用、多次切割靶标信使RNA,其组织疗效作用维持时间极长。这种药代动力学与药效学明显分离的现象,是小核酸药物最核心的特征。因此,在多剂量递增及早期探索性研究中,研究终点不应局限于血浆药物浓度的监测,而必须将重心转移至药效学特征的评估上。研究人员需选择敏感且特异的生物标志物,如靶标信使RNA水平、靶蛋白浓度或反映靶蛋白调节的下游脂质指标,进行长周期的动态观察。以英克司兰钠的早期临床研究为例,单次皮下注射300毫克后,血浆浓度在约4小时达到峰值,48小时后即无法测出。但在给药后14天内,前蛋白转换酶枯草溶菌素9和低密度脂蛋白胆固醇水平出现显著下降,且这种降幅在第60天达到峰值,至第180天仍能维持超过50%的降幅。基于这种长效特征,其Ⅱ期临床试验的随访周期被延长至一年,以确保准确捕捉药效学持续时间和谷值浓度。表2.英克司兰钠的相关临床试验
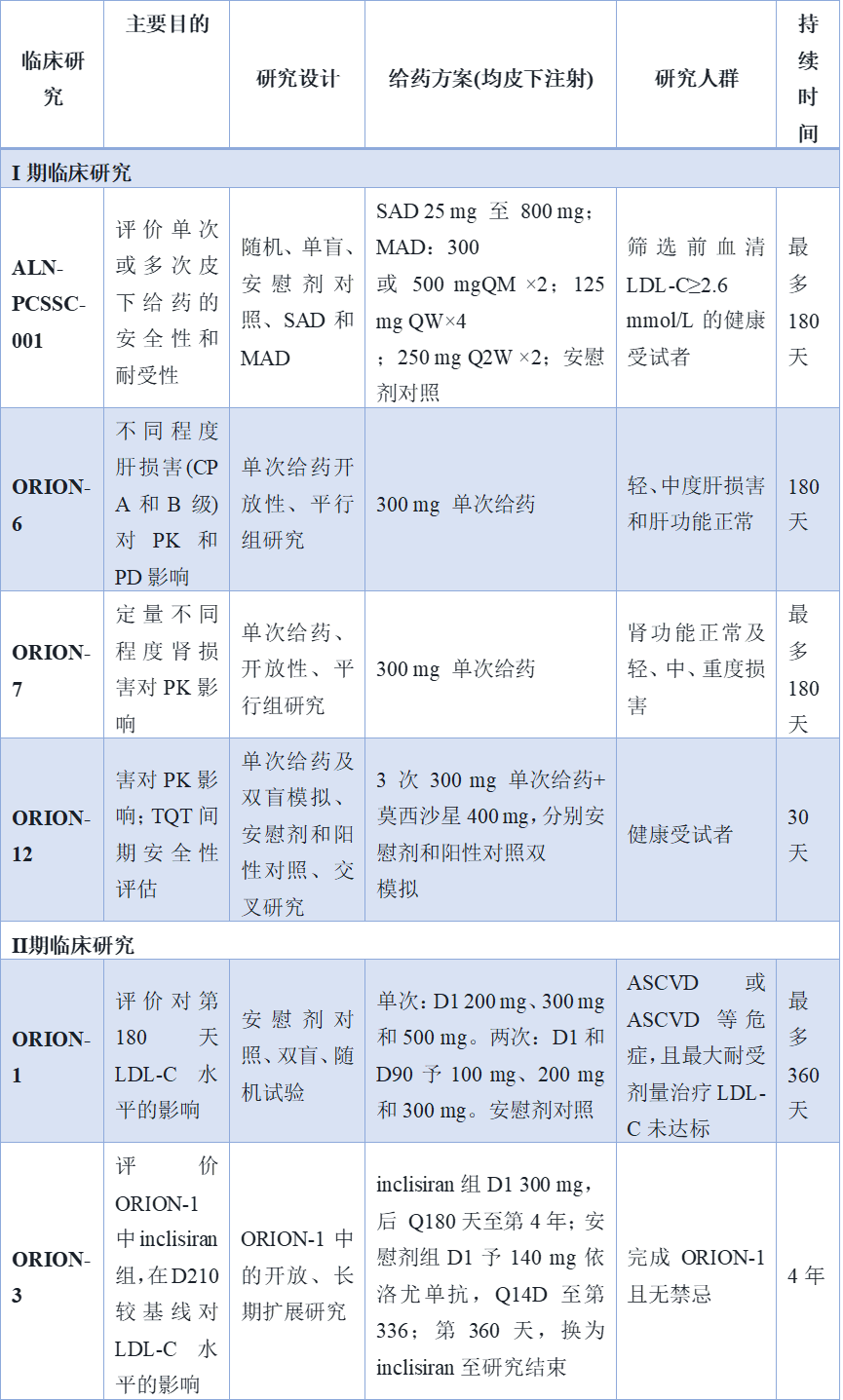

给药间隔的设计必须严格依赖于药效学持久性数据。模型引导的药物研发理念,如群体药效学建模,应贯穿早期研发全程,以精准预测不同给药方案下的长期疗效轨迹。此外,心血管疾病的高发人群为老年人,且常合并多种基础疾病,需服用多种心血管药物。因此,在早期临床阶段必须纳入足够比例的老年受试者,开展针对肝肾功能不全人群的药代动力学研究,以及与常见合并用药的药物相互作用研究,为后续广泛人群的应用提供安全保障。三、确证性临床试验设计的科学逻辑
确证性临床试验是小核酸药物获批上市的决定性环节。由于小核酸药物作用机制的特殊性,其确证性试验在研究周期、给药方案以及主要终点设置上需要综合权衡疾病特征与药效学规律。3.1研究周期的合理性设置
传统心血管药物的双盲期可能较短,但小核酸药物由于药效维持时间长,必须设置足够长的观察周期,以充分评估其有效性波动与安全性累积情况。确证性试验的周期不仅取决于预期达到的药效学稳态,还需结合疾病本身的进展规律和主要疗效终点的事件发生率。在英克司兰钠的三项Ⅲ期临床试验中,双盲持续时间被设定为18个月。其给药方案为首日与第90天进行两次负荷给药,随后在第270天和第450天进行每半年一次的维持给药。在第4针给药后继续观察3个月,从而确保在完整的给药间隔内获取稳健的有效性数据。3.2主要终点的选择需体现临床价值导向
对于已有明确替代终点的疾病,如低密度脂蛋白胆固醇降低与动脉粥样硬化性心血管疾病风险的正相关性,可以采用经安慰剂校正的脂质百分比变化作为主要终点。然而,对于部分新型靶点,如脂蛋白与心血管事件之间的因果关系尚未完全确立时,监管机构通常要求以主要不良心血管事件作为临床结局评价支持上市。这类由事件驱动的试验,如Olpasiran的Ⅲ期研究,其预计时间窗长达48个月,这对于小核酸药物的长期稳定性、生产工艺以及受试者依从性都是极大的考验。此外,对于转甲状腺素蛋白淀粉样变性伴心肌病这类进展迅速的致死性罕见病,试验周期的设计则更注重在有限时间内捕捉到具有统计学意义的临床获益。Vutrisiran的HELIOS-B研究将双盲期设定为36周,以全因死亡率与复发性心血管事件的复合终点作为主要评价指标。这一周期既能初步反映药物对心肌结构的改善,又能在合理的时间范围内积累足够的事件数以支持有效性评价。表3.小核酸药物代表性靶点全球上市或部分Ⅲ期临床试验情况

四、在全生命周期中贯穿安全性评价
安全性评价是小核酸药物研发中不可逾越的红线,必须贯穿于非临床研究、临床试验以及上市后全生命周期的各个阶段。小核酸药物独特的分子结构和作用模式,决定了其安全性风险具有高度的复杂性。4.1非临床毒性评价阶段
研究需全面覆盖寡核苷酸的内在毒性及递送系统的潜在风险。内在毒性包括基于杂交序列依赖的靶向毒性、脱靶毒性以及RNA干扰通路饱和引发的毒性;非杂交序列依赖的脱靶毒性同样不容忽视。递送系统可能引入免疫原性和化学毒性。因此,在进入临床前,必须通过计算机模拟和体外高通量筛选对脱靶效应进行充分评估,并开展涵盖心血管、呼吸及中枢神经系统的核心安全药理学研究。4.2临床安全性评价方面
早期试验必须严密监测QTc间期延长、肝肾功能损害及注射部位反应等常见风险。安全性研究的观察周期必须与药效学持续时间相匹配,防止因观察期不足而遗漏迟发性不良反应。历史教训表明,安全性问题是制约小核酸药物上市的致命因素。部分已获批的反义寡核苷酸药物,如早期获批的靶向载脂蛋白B-100的药物,因存在肝脂肪变性、肝酶升高及流感样症状等安全性隐患,未获欧洲药品管理局批准,且最终退市。另一款靶向载脂蛋白C-Ⅲ的反义寡核苷酸药物,亦因高达76%的血小板减少发生率被美国食品药品监督管理局拒绝批准。4.3上市后的全生命周期安全性监测
随着受试者样本量的扩大和暴露时间的延长,一些罕见的或长潜伏期的毒性反应可能逐渐显现。监管机构需持续追踪上市后的真实世界数据,及时更新说明书中的黑框警告和注意事项,确保药物在广泛人群中使用时的获益风险比始终处于正向区间。五、心血管疾病小核酸药物研发面临的挑战与未来展望
小核酸药物在心血管疾病领域的应用前景广阔,但其创新研发之路上仍存诸多亟待攻克的科学挑战。首先是成药性的技术壁垒。小核酸药物的稳定性高度依赖于核糖骨架、糖环及碱基的精细化学修饰,如何在不增加脱靶效应的前提下进一步优化其药代动力学特性,仍是药学开发的核心难题。其次,递送系统的局限性极大制约了适应症的拓展。目前获批或在研的心血管小核酸药物绝大多数依赖于肝靶向递送系统,如N-乙酰半乳糖胺偶联技术,这使得药物主要富集于肝脏。如何突破生理屏障,实现向心脏、血管内皮等非肝器官的高效、精准递送,同时避免递送系统分布不均带来的脱靶毒性,是未来技术突破的关键方向。此外,由于药效持续时间极长,潜在毒性及安全性的评估窗口也被迫拉长,这对传统的临床研发周期和资金投入提出了更高要求。尽管面临挑战,小核酸药物所代表的基因沉默疗法依然为心血管慢性病管理带来了革命性突破。为了加速这一领域的健康发展,药品监管机构、研究机构与工业界需形成合力。在临床研发策略上,应深刻认识药代动力学与药效学分离的客观规律,摒弃经验主义,基于翔实的药效学持久性数据,科学规划给药间隔与临床试验周期,确保有效性及安全性评估的充分性与严谨性。同时,应积极引入模型引导的药物研发等新兴技术手段,提升研发效率。六、结语
总的来说,心血管疾病作为全球重大的公共卫生挑战,亟需具备长效、精准优势的新型治疗武器。小核酸药物以其独特的作用机制,彻底打破了传统降脂、降压药物需每日服用的困境,通过每数月给药一次的极低频率,为解决长期治疗依从性这一世界级难题提供了切实可行的方案。从血脂异常到心肌淀粉样变,从危险因素干预到靶器官保护,小核酸药物已在心血管领域展现出不可替代的临床价值。然而,新分子实体带来的不仅是机遇,更是对传统临床研发逻辑的颠覆。在小核酸药物的研发与评价过程中,必须始终紧扣其组织药效学半衰期长、药代与药效学分离的核心特征。无论是在探索性阶段的剂量摸索,还是在确证性阶段的方案设计,抑或是全生命周期的安全性把控,都应基于科学的数据驱动,确保给药方案的合理性与研究周期的充足性。展望未来,随着化学修饰技术的迭代与递送系统的突破,小核酸药物必将在心血管疾病乃至更广阔的治疗领域谱写出精准医学的新篇章,为全球数以亿计的心血管疾病患者带来更长久的生存获益与更高的生命质量。1. Rodriguez F, Maron DJ, Knowles JW, Virani SS, Lin S, Heidenreich PA. Association of Statin Adherence With Mortality in Patients With Atherosclerotic Cardiovascular Disease. JAMA Cardiol. 2019 Mar 1;4(3):206-213. doi: 10.1001/jamacardio.2018.4936.2. Ray KK, Stoekenbroek RM, Kallend D, Leiter LA, Landmesser U, Wright RS, Wijngaard P, Kastelein JJP. Effect of an siRNA Therapeutic Targeting PCSK9 on Atherogenic Lipoproteins: Prespecified Secondary End Points in ORION 1. Circulation. 2018 Sep 25;138(13):1304-1316. doi: 10.1161/CIRCULATIONAHA.118.034710.3. FDA.Clinical Pharmacology Considerations for the Development of Oligonucleotide Therapeutics Guidance for Industry. 20244. Ranjbar S, Zhong XB, Manautou J, Lu X. A holistic analysis of the intrinsic and delivery-mediated toxicity of siRNA therapeutics. Adv Drug Deliv Rev. 2023 Oct;201:115052. doi: 10.1016/j.addr.2023.115052.5. Makhmudova U, Steinhagen-Thiessen E, Volpe M, Landmesser U. Advances in nucleic acid-targeted therapies for cardiovascular disease prevention. Cardiovasc Res. 2024 Sep 2;120(10):1107-1125. doi: 10.1093/cvr/cvae136.作者:栗雅,主要从事药物质量控制与分析检测等方面工作。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。