第一PROTAC药物
2026 年 5 月 1 日,FDA 正式批准 Arvinas 公司的Vepdegestrant(商品名 Veppanu,ARV-471)上市。这不是一次普通新药获批,而是靶向蛋白降解技术从实验室走向临床的里程碑。与传统 “占据抑制” 小分子不同,PROTAC 不靠持续结合阻断蛋白,而是直接触发蛋白降解,从机制上突破了传统药物的边界。
研究背景
现代药物化学长期遵循一条默会的规则:要让一个蛋白失活,就要找到一个能与它紧密结合的分子,堵住它的活性位点。这种“占据驱动”模式有效,但有结构性的边界。人体内约85%的蛋白缺乏足够深、足够特异的结合口袋,它们表面平坦或构象多变,让经典抑制剂无处锚定,因而被归入“不可成药”的范畴。另有一个困扰临床的现象是,即使某些靶点可以被有效抑制,肿瘤细胞也能通过代偿性过表达或靶点基因突变重新建立信号通路,让药物逐渐失去效力。乳腺癌内分泌治疗的困境就是典型案例:雌激素受体α驱动约七成乳腺癌的生长,芳香化酶抑制剂、他莫昔芬乃至氟维司群都针对这条通路,然而ESR1基因的获得性突变——尤其是配体结合域中的Y537S和D538G——能赋予受体不依赖配体的组成性激活能力,同时改变受体构象,降低甚至消解传统拮抗剂的亲和力。此时,药物还在,靶点已变,这就是占据模式的极限。
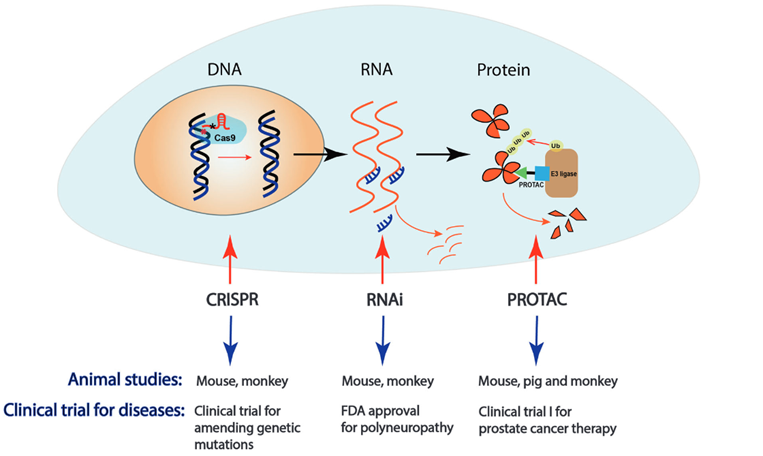
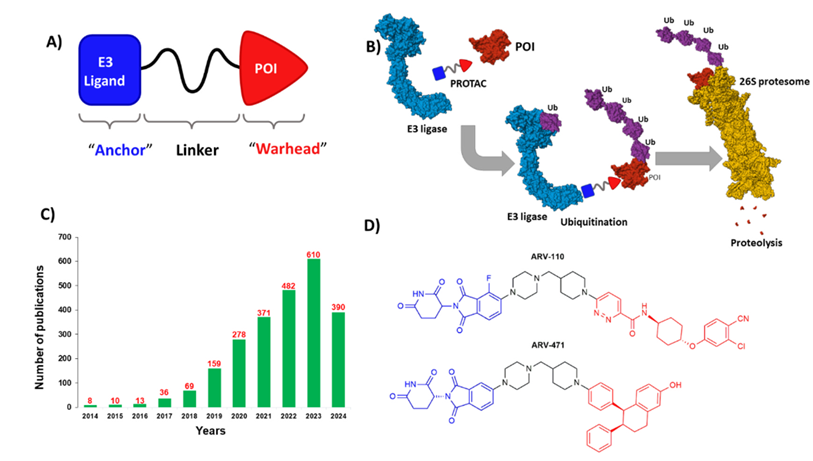
由分子到产品的进化
PROTAC的概念本身并不年轻。2001年,Craig Crews与Raymond Deshaies报道了第一个PROTAC分子Protac-1,靶向甲硫氨酸氨肽酶-2。但那是一个肽基分子,细胞穿透性差,酶解稳定性和口服生物利用度几乎为零,它更像一纸概念证明,而非药物前体。此后十四年间,研究者尝试用各种小分子模块替代肽段,逐步解决稳定性问题,可始终差临门一脚:直到2015年前后,多个课题组同时报告了全小分子、可在完整动物体内发挥药效的PROTAC,其中最关键的突破之一是沙利度胺衍生物被系统性确认为Cereblon这一E3连接酶的可靠配体——这意味着PROTAC的另一只“抓手”终于有了可成药的组装模块。
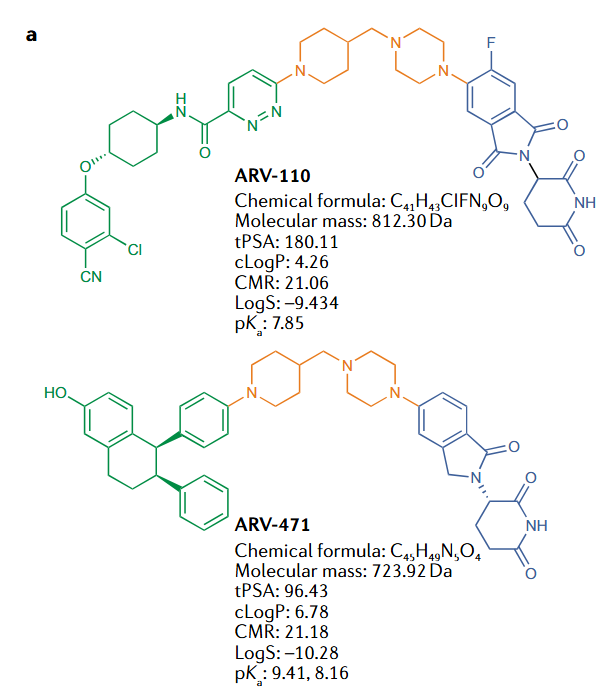
Arvinas公司正是在这个时间窗口选择了乳腺癌作为首发适应症。这不是随机的。乳腺癌的内分泌治疗有成熟的临床路径和明确的需求缺口,尤其晚期CDK4/6抑制剂联合内分泌治疗失败后出现ESR1突变的那部分患者,几乎没有高效低毒的选择。选择雌激素受体α为靶点,同时意味着可以利用过去几十年积累的ER配体化学库来设计“战斗部”,将风险集中于PROTAC的桥接而非靶点本身。Vepdegestrant即为这一策略的产物:它的ER端配体来自优化的非甾体ER调节剂骨架,保证了对野生型和突变型ER的稳健结合;E3端招募Cereblon,源自泊马度胺/来那度胺化学空间的迭代;连接子部分经过对长度、环状约束、杂原子嵌入的系统扫描,以优化三元复合物的协同性而非仅靠亲和力。三元复合物形成时的蛋白-蛋白界面协同性是决定降解效率的核心参数,具体涉及ER与Cereblon之间因空间拉近而产生的新接触面,能稳定过渡态从而提高E3的泛素转移效率,这是我们评估PROTAC活性时不能只看二元结合力,而需用三元复合物热力学和动力学参数去衡量的原因。
FDA于2025年8月8日受理Vepdegestrant的NDA,PDUFA日期设定为2026年6月5日,实际批准于5月1日,提前近五周。提前批准在FDA审评实践中一般对应几种情境:疗效信号极强且安全性清晰,或满足重大未竟需求以至于任何延迟都可能损害患者利益。这一案例中,ESR1突变亚组的疗效明确、受益风险比有利,且伴随诊断已经可及,这些因素共同推动了加速审评。
总结
Vepdegestrant的获批不是孤立的成功。它的真正分量在于完成了一条技术路径的科学验证闭环。PROTAC长期面临三重核心怀疑:异双功能分子能否口服吸收并达到有效人体暴露?降解机制能否在人体肿瘤组织中忠实再现?催化型降解剂能否转化为统计学清晰且临床可感知的疗效?VERITAC-2和背后的整个开发数据链,用严格随机对照试验回答了这些问题。这为后续难以抑制的靶点——比如转录因子、支架蛋白以及异常折叠的神经退行性疾病相关蛋白——提供了可供参考的“可能性证明”。
但必须同时看到限度。其一,PFS绝对延长仍有2.9个月,肿瘤最终会以泛素-蛋白酶体通路组分改变、CRBN下调或替代激素信号激活等方式对PROTAC产生继发耐药,这些机制已在ARV-110的前列腺癌项目中部分观察到。其二,ESR1野生型人群未获益的事实提醒我们,PROTAC并非一律优于传统SERD,对野生型ER,氟维司群介导的降解程度足以达成临床控制,增加降解深度未必能线性转化为临床优势,背后可能是信号通路完全被压制所需的最低ER阈值不同。其三,化学空间方面,分子量约724 Da、刚性的三组分骨架会持续给优化口服PK、组织分布以及中枢神经系统渗透性带来限制,对PROTAC在癌症之外的拓展是一项需要解决的工程瓶颈。
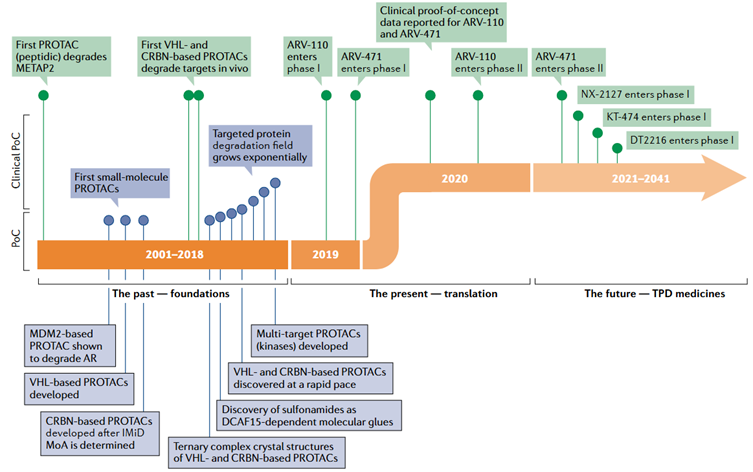
更宏观上看,Vepdegestrant打开了蛋白降解疗法的闸门,竞争格局正在急剧变化。Arvinas针对雄激素受体的下一代PROTAC——ARV-766,已在去势抵抗性前列腺癌中进入后期临床研究(其前代分子ARV-110因疗效不足已终止开发)。C4 Therapeutics、Kymera、Nurix,以及中国本土的生物技术力量正在推进不同E3配体、不同靶点的快速跟进。从方法学角度看,“泛素-蛋白酶体”降解不会是最终答案,靶向溶酶体的LYTAC、自噬体的ATTEC,乃至信号依赖的条件性降解技术,正在同步生长,这意味着Vepdegestrant所开启的,不仅是一个新药的时代,而可能是一个“诱导降解”成为常规治疗模态的时代。一个花费了二十五年从概念走向药盒的技术,它的第一个上市产品,既是终点也是起点。对那些正在实验室里摸索某个不可成药靶点的研究者来说,这个时刻给予的或许不是答案,而是一个可以继续追问下去的许可。
参考文献
Degrading proteins in animals: “PROTAC”tion goes in vivo
PROTAC unleashed: Unveiling the synthetic approaches and potential therapeutic applications
PROTAC targeted protein degraders: the past is prologue


